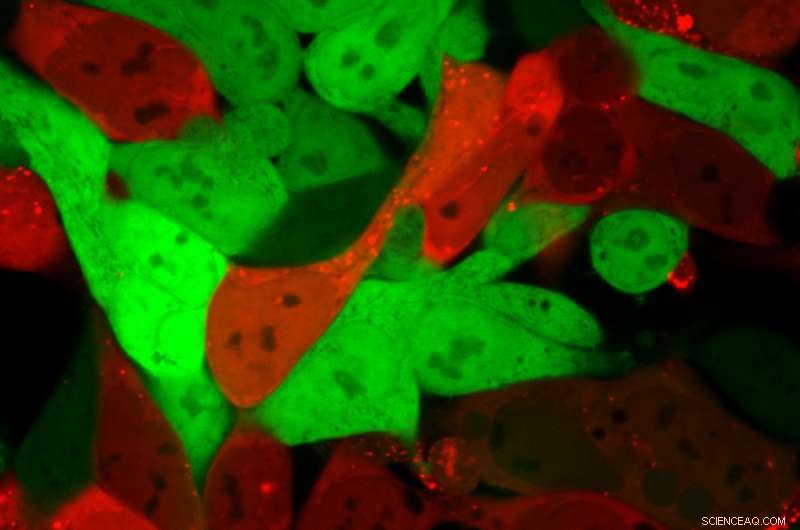
Celler som normalt är ljusgröna blir klarröda efter att lipidnanopartiklar har levererat en mRNA-last som kodar för Cre. Celler som är röda innehåller mRNA, medan gröna celler inte gör det. Kredit:Daryll Vanover, Georgia Tech
En ny screeningsprocess kan dramatiskt påskynda identifieringen av nanopartiklar som är lämpliga för att leverera terapeutiskt RNA till levande celler. Tekniken skulle tillåta forskare att screena hundratals nanopartiklar åt gången, identifiera organen där de ackumuleras – och verifiera att de framgångsrikt kan leverera en RNA-last till levande celler.
Baserat på arbete som kallas "DNA-streckkodning, " tekniken infogar unika DNA-bitar i så många som 150 olika nanopartiklar för samtidig testning. Nanopartiklarna injiceras sedan i djurmodeller och tillåts resa till organ som levern, mjälte eller lungor. Genetiska sekvenseringstekniker identifierar sedan vilka DNA-märkta nanopartiklar som har nått specifika organ.
I en artikel publicerad 1 oktober i tidskriften Proceedings of the National Academy of Sciences , ett forskarlag beskriver att ta processen ett steg längre för att verifiera att nanopartiklarna har kommit in i cellerna i de specifika organen. Förutom DNA-streckkoden, forskarna infogade i varje nanopartikel en bit av mRNA som förvandlas till ett protein som kallas "Cre". Cre-proteinet genererar ett rött sken, identifiera celler som nanopartiklarna har kommit in i och framgångsrikt levererat mRNA-läkemedlet, så att forskarna kan identifiera vilka nanopartiklar som kan leverera RNA-läkemedel till cellerna i de specifika organen.
"Denna teknik, känd som Fast Indication of Nanopartikel Discovery (FIND), kommer att tillåta oss att identifiera rätt transportör mycket snabbare och billigare än vi har kunnat göra tidigare, sade James E. Dahlman, biträdande professor vid Wallace H. Coulters avdelning för biomedicinsk teknik vid Georgia Tech och Emory University. "Som ett resultat, oddsen för att vi kommer att kunna hitta bärare för specifika vävnader bör öka dramatiskt."
FIND-tekniken skulle ersätta in vitro-screening, som har begränsad framgång med att identifiera nanopartikelbärare för de genetiska terapierna. Forskningen stöddes av finansiering från National Institutes of Health, och från Cystic Fibrosis Research Foundation, Parkinson's Disease Foundation och Bayer Hemophilia Awards Program.

James Dahlman, en biträdande professor vid Wallace H. Coulters avdelning för biomedicinsk teknik vid Georgia Tech och Emory University, har ett mikrofluidiskt chip som används för att tillverka nanopartiklar som kan användas för att leverera terapeutiska gener. Kredit:Rob Felt, Georgia Tech
Terapier baserade på RNA och DNA kan behandla ett brett spektrum av genetiskt baserade sjukdomar, inklusive åderförkalkning, där sådana terapier kan vända uppbyggnaden av plack i artärer. Nanopartiklar som används för att leverera RNA och DNA till celler är gjorda av flera ingredienser vars nivåer kan varieras, skapa potential för tiotusentals olika nanopartiklar. Att hitta den rätta kombinationen av dessa ingredienser för att rikta in sig på specifika celler har krävt omfattande försök och misstag upptäcktsprocesser som har begränsat användningen av RNA- och DNA-terapier.
Användning av DNA-streckkodningsprocessen gör att hundratals möjliga nanopartikelkombinationer kan testas samtidigt i ett enda djur, men tills nu, forskare kunde bara säga att kombinationen hade nått specifika organ. Genom att undersöka vilka celler i organen som har den röda glöden, de kan nu verifiera att nanopartiklarna bar streckkoderna och levererade funktionella mRNA-läkemedel in i cellerna.
I tidningen, forskarna rapporterar att de upptäckte två nanopartiklar som effektivt levererade siRNA, sgRNA och mRNA till endotelceller i mjälten. Forskarna tror att deras teknik kan leverera terapeutiskt RNA och DNA till en mängd olika endotelcellstyper, och kanske även till immunförsvar och andra celltyper.
"Fältet har fungerat kunna leverera genetiska läkemedel till levern, och vi försöker nu använda vår teknologi för att leverera till olika organ och celltyper för att möjliggöra behandlingar för att behandla alla celltyper som finns i levern, sa Cory Sago, tidningens första författare och en Ph.D. kandidat i Dahlmans labb. "Nu när vi har ett system som tillåter oss att undersöka dessa frågor på en mycket specifik lösningsnivå, vi vill nu gå efter andra celltyper på ett mer effektivt sätt."
Dahlman räknar med att ta den nya tekniken i bruk snabbt.

James Dahlman, en biträdande professor vid Wallace H. Coulters avdelning för biomedicinsk teknik vid Georgia Tech och Emory University, visas i hans laboratorium. Kredit:Christopher Moore, Georgia Tech
"Vi hoppas kunna ta projekt som vanligtvis skulle ta år och slutföra flera av dem inom de närmaste 12 månaderna, ", sade han. "FIND kan användas för att bära alla sorters nukleinsyraläkemedel in i celler. Det kan inkludera små RNA, stora RNA, små DNA och stora DNA - många olika typer av genetiska läkemedel som nu utvecklas i forskningslabb."
Tekniska utmaningar framöver inkluderar att visa att identifiering av en affinitet för musorgan förutsäger vilka partiklar som kommer att fungera i människokroppen, och att tillvägagångssättet fungerar för olika klasser av genetiska terapier.
Experimentellt, Dahlmans labb producerar nanopartiklarna vid tre formuleringsstationer som tar cirka 90 sekunder för att producera vart och ett av de cirka 250 prover som används. De resulterande nanopartiklarna undersöks sedan för lämplig storleksintervall - 40 till 80 nanometer i diameter - innan de renas och steriliseras för injektion i djuren.
Efter tre dagar, forskarna separerar celler som lyser rött och sekvenserar DNA-bitarna i dem för att identifiera vilka kemiska sammansättningar som var mest framgångsrika när det gällde att komma in i celler i specifika organ. De mest lovande kemiska kompositionerna används för att utveckla en ny sats av kandidat-nanopartiklar för en ny omgång av screening, som tar ungefär en vecka att slutföra.
"Vi vill utveckla de bästa partiklarna vi kan, " Sago sa. "Var och en av komponenterna är viktiga, och vi arbetar för att få varje komponent rätt för den celltyp som vi är intresserade av. Det krävs mycket optimering."