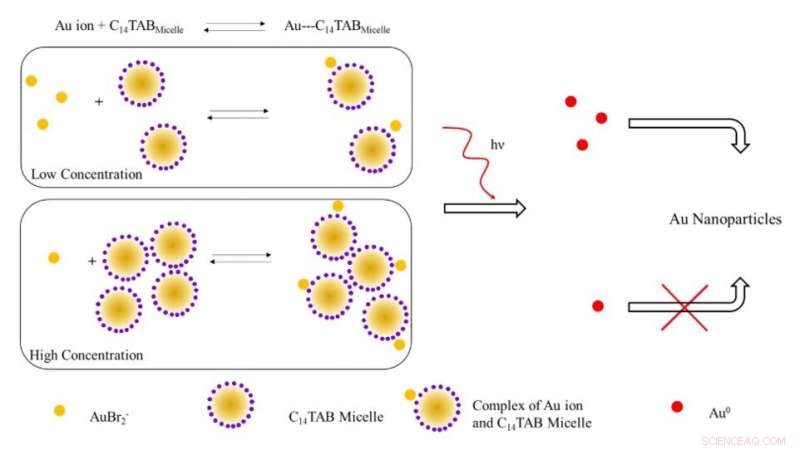
Schematisk illustration av den föreslagna mekanismen för bildning av guldnanopartiklar vid bestrålning med joniserande strålning. Vid låga ytaktiva koncentrationer, de flesta guldjoner (AuBr2- /Au1+) är sannolikt fria i lösning (obundna till miceller). Med ökande koncentration av ytaktiva ämnen, jämvikten skiftar till höger med en minskning av fria guldjoner. Vid bestrålning, antalet Au^0 -atomer som bildas på grund av minskning vid låg koncentration av ytaktiva ämnen är högre på grund av närvaron av ett högre antal fria guldjoner i motsats till systemet vid hög koncentration av ytaktiva ämnen. Det högre antalet fria guldatomer leder till ett ökat utbyte av guldnanopartiklar på grund av ytassisterad reduktion med oreagerade guldjoner. Upphovsman:Science Advances, doi:10.1126/sciadv.aaw8704.
Rutinmätningen av strålningsdoser kan vara kliniskt utmanande på grund av begränsningar med konventionella dosimetrar som används för att mäta dosupptag av extern joniserande strålning. I en ny studie, Karthik Pushpavanam och ett tvärvetenskapligt team av forskare vid avdelningarna för kemiteknik, Molekylära vetenskaper, Banner MD Anderson Cancer Center och Arizona Veterinary Oncology i USA har beskrivit en ny gelbaserad nanosensor. Tekniken möjliggör kolorimetrisk detektion och kvantifiering av topografiska strålningsdosprofiler under strålbehandling.
Vid exponering för joniserande strålning, forskarna konverterade guldjoner i gelén till guldnanopartiklar (AuNP) tillsammans med en visuell förändring av gelfärgen på grund av plasmoniska egenskaper. De använde färgintensiteten som bildades i gelen som en kvantitativ reporter för joniserande strålning och använde först gelananosensorn för att detektera komplexa topografiska dosmönster efter administrering till antropomorfa fantommodeller följt av applikationer med levande hundpatienter som genomgår klinisk strålbehandling. Enkel tillverkning, drift, snabb avläsning, kolorimetrisk detektion och relativt låg kostnad för tekniken innebar translationell potential för topografisk doskartläggning under kliniska strålterapitillämpningar. Forskningsarbetet publiceras nu på Vetenskapliga framsteg .
Framsteg inom strålterapi har lett till anmärkningsvärd sofistikering och toppmodern planeringsprogramvara för att leverera höga konforma strålningsdoser till patienter för förbättrad livskvalitet efter behandlingen. Under strålbehandling, en hög dos levereras vanligtvis till en måltumör samtidigt som strålningsdosen till omgivande vävnad minimeras. Under palliativ vård administreras patienter med större fraktionsdoser för att avsluta behandlingen inom en kort tidsram. Dock, programvarufel under sådana procedurer kan leda till överdosering och efterföljande sjuklighet.
För att minimera oavsiktlig överexponering, forskare försöker oberoende verifiera dosen av strålning som levereras vid eller nära målvävnaden för avancerad patientsäkerhet. Tekniskt, både molekylära och nanosensorer kan övervinna gränser som finns i konventionella system för att bilda praktiska alternativ som lättsensorer. Dock, deras befintliga gränser bör åtgärdas och lindras för att utveckla robusta och effektiva sensorer som kvantitativt och kvalitativt bestämmer de topografiska dosprofilerna under klinisk strålbehandling.

Digitala bilder och UV-synliga spektra av olika gel-nanosensorformuleringar som utsätts för terapeutiska doser av röntgenstrålar (A) Bilder av gel-nanosensorer tillverkade i 24-brunnars cellodlingsplattor och som innehåller olika koncentrationer av C14TAB (24,5 till 73,5 mM) vid exponering för olika doser av joniserande strålning (0- till 10-Gy röntgenstrålar); Na2S väntetid var 5 minuter efter bestrålning, och inkubationstiden var 10 min. Bilderna erhölls 1 timme efter bestrålning. En synlig ökning av intensiteten i den rödbruna färgen observeras med ökande doser av joniserande strålning för de flesta C14TAB -koncentrationer som används under gelsensorutveckling. (B till F) Absorbansspektra (300 till 990 nm) av samma gel -nanosensorer som innehåller (B) 24,5 mM, (C) 31 mM, (D) 37 mM, (E) 49 mM, och (F) 73,5 mM bestrålade med användning av olika strålningsdoser. Karakteristiska absorbanstoppar mellan 500- och 600-nm våglängder är indikativa för guldnanopartiklar som bildas i gelerna. Motsvarande strålningsdoser nämns i legenden med ökande strålningsdos (topp till botten). A.U., godtyckliga enheter. Foto:Sahil Inamdar, Arizona State University. Upphovsman:Science Advances, doi:10.1126/sciadv.aaw8704
Eftersom guldnanopartiklar (AuNP) har unika fysikaliska och kemiska egenskaper som ger en utmärkt plattform för att utveckla sensorer. Pushpavanam et al. konstruerade en kolorimetrisk sensor där joniserande strålning orsakade AuNP -bildning från färglösa saltprekursorer. Bildandet av en gelbaserad nanosensor kan möjliggöra enkel hantering och applikationer under klinisk strålbehandling.
I det nuvarande arbetet, laget demonstrerade kolorimetrisk detektion och kvantifiering av dosfördelningsprofiler med hjälp av en gel -nanosensor för att topografiskt kartlägga strålningsdoser längs vävnadsytor. Under prekliniska utvärderingar, teamet administrerade gelnanosensortekniken hos levande hundpatienter som genomgår strålbehandling. Totalt, resultaten indikerade teknikens omfattning för klinisk översättning hos mänskliga patienter och förmågan att bestämma topografiska doser för att planera behandlingar och verifiera doser under cancerstrålbehandling.
Under experimenten, omvandlingen av guldjoner till nanopartiklar åtföljdes av en rödbrun färgutveckling i den bestrålade regionen av gel -nanosensorn. Medan guld existerar i ett trevärt tillstånd i allmänhet (AuCl 4 - ) den kan reduceras till ett metastabilt +1 valenstillstånd (AuBr 2 - ) vid rumstemperatur med hjälp av askorbinsyra (vitamin C). Bestrålning av geler som innehåller terapeutiska nivåer av strålning stimulerade radiolys eller splittring av vattenmolekyler till mycket reaktiva fria radikaler. De radiolysgenererade hydrerade elektronerna reducerade i sin tur monovalent guld för att bilda guldatomer i sitt nollvärda tillstånd (Au 0 ) som kärnbildades och mognade till rödbrunfärgade AuNP. Intensiteten varierade med strålningsdosen och teamet använde intervallet linjära svar för att kalibrera gel -nanosensorn. Baserat på denna princip, Pushpavanam et al. bestämde svaret för de fullständigt bestrålade gelerna för att kalibrera absorbansen med strålningsdos.
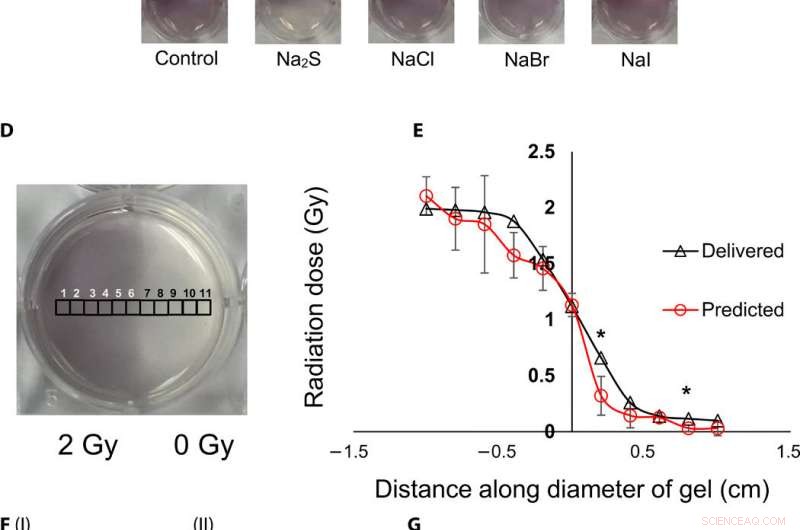
Topografisk visualisering och kvantifiering av strålningsdoser med gel -nanosensorer. (A) Gel nanosensor (vänster) före bestrålning, (mitten) övre halvan bestrålad med 4 Gy och bild förvärvad 2 minuter efter bestrålning, och (höger) bild förvärvad 1 timme efter bestrålning. En synlig ökning av färgintensiteten i den icke -bestrålade nedre halvan indikerar blödning av färg och förlust av topografisk information. (B) I:1,5% (vikt/volym) agarosgel (vänster) 2 minuter efter bestrålning och (höger) 1 timme efter bestrålning; II:2% (w/v) agarose gel (left) 2 min after irradiation and (right) 1 hour after irradiation indicates that the increase in agarose weight percentage does not preserve topographical dose information. (C) Gel nanosensor incubated with 5 mM sodium sulfide (Na2S) and various sodium halides with a wait time of 10 min and incubation time of 10 min; images were acquired after 1 hour. No loss of topographical information is observed upon incubation with sodium sulfide. All gels were fabricated in 24-well plates. (D) Colorimetric response of the gel nanosenor irradiated on one-half with a 2-Gy x-ray dose. A visible appearance of maroon color in the irradiated region illustrates the ability of the gel nanosensor to visualize topographical dose profiles. Each black square box (labeled 1 to 11) on the gel nanosensor corresponds to a grid of size ≈2 × 2 mm, whose absorbance at 540 nm is determined. Grids starting from 1 to 5 are regions exposed to ionizing radiation, 6 is the grid at the edge of the irradiation field, and grids from 7 to 11 are regions outside the field of irradiation. (E) Dose fall-off profile for the gel nanosensor irradiated by 2 Gy on one-half. The delivered and predicted radiation doses are comparable, which indicates the efficacy of the gel nanosensor in visualizing and retaining topographical information. In all cases, Na2S was added for 10-min incubation time after a wait time of 30 min. Radiation doses predicted by the gel nanosensor as compared with the delivered radiation dose as obtained from the treatment planning system. Asterisks indicate statistically significant differences (P <0.05) between the delivered dose and the dose predicted by the gel nanosensor (n =3 independent experiments). (F) Representative image of a petri dish containing the gel nanosensor formulation (≈3 mm thick and ≈10 cm diameter) irradiated with a 1 cm × 1 cm square field of x-ray radiation. Från vänster, each square indicates increasing radiation dose from (I) 0.5 Gy (red box), 1 Gy, and 1.5 Gy; (II) 2, 2.5, 3, and 3.5 Gy; and (III) 4, 4.5, and 5 Gy; the black box in image (II) shows 0 Gy. (G) Visualization of a complex topographical dose pattern (ASU letters) generated using a 2-Gy x-ray dose. The petri dish has a diameter of ≈10 cm. In (F) and (G), the gel nanosensors contain 24.5 mM C14TAB, and Na2S was added after a wait time of 30 min and incubation time of 10 min; a representative image from three independent experiments is shown. Photo credit:Sahil Inamdar, Arizona State University. Upphovsman:Science Advances, doi:10.1126/sciadv.aaw8704.
To determine intensity of the color and dose delivered within gels after irradiation, the researchers used absorbance spectroscopy and observed a decrease in the spectral profile width, with increasing radiation dose for decreased polydispersity (ratio of the percentage of the standard deviation to the average value) of the nanoparticles. The peak absorbance intensity increased with increasing radiation dose to corroborate the observed increase in color intensity.
To understand the gel nanosensor's ability to detect topographical distribution of the radiation dose, the scientists irradiated half of the gel nanosensor with a 4 gray (Gy) dose. The maroon-color only appeared in the irradiated area confirming AuNP formation, but after one hour of exposure, the color bled into the irradiated region showing loss of topographic information in the gel with time. The team observed the phenomenon to arise from reaction-controlled conditions and not based on the gel composition. By incubating the gel with sodium sulfide (Na 2 S) for 10 minutes, they suppressed the color bleed-over and reasoned that to the ability to quench unreacted gold ions in the nonirradiated region and preserve dose information accurately for dose visualization and dosimetry. The scientists adopted the sensor for wide dose ranges by modulating the time of Na 2 S addition; to achieve a level of flexibility hitherto unavailable in clinical dose detection systems.
The research team then used the gel nanosensor to visualize diverse topographical radiation patterns, where the intensity of the color increased with increasing dose while preserving topographical integrity. Som bevis på konceptet, they showed the gel nanosensor's ability to detect complex radiation patterns with a model dose patterned to form "ASU" (after Arizona State University). Then using transmission electron microscopy (TEM), the scientists characterized the generated gold nanoparticles as a function of dose to observe reduced average nanoparticle diameter and polydispersity at higher doses of radiation. They followed this with energy dispersive X-ray spectroscopy (EDS) to detect higher yields of AuNPs in the irradiated regions of the gel nanosensor as expected.

Gel nanosensor enabled topographical detection and quantification of clinical radiation doses in anthropomorphic head and neck phantoms. (A) Anthropomorphic head and neck phantom treated with an irregularly shaped x-ray radiation field below the left eye. (B) Image of the gel nanosensor positioned on the anthropomorphic phantom in the radiation field mimicking a conventional radiotherapy session. (C) Axial view of the treatment planning image along the central axis of the radiation beam representing an irregularly shaped radiation field used to deliver a complex radiation pattern under the eye of the phantom. The core of the crescent-shaped treatment region receives a radiation dose of 2.3 Gy (highlighted in red), and regions receiving lower doses are highlighted with different colors going outward (from green to light pink). (D) Visual image of the dose pattern on the gel nanosensor formed after delivery of 2.3 Gy. Only the irradiated region develops a maroon color, while the nonirradiated region remains colorless. (E) Expected topographical dose “heat map” profile of the radiation dose delivered to the gel placed in the phantom. The expected profile is generated from the treatment plan in the dose delivery system. In these figures, red and blue colors indicate higher and lower radiation doses, respektive. (F) Topographical doses predicted by the irradiated gel nanosensor. Absorbance values of ≈2 mm × 2 mm grids were quantified using a calibration curve to generate the topographical dose profile. The anticipated dose received by the core of the crescent-shaped profile (2.3 Gy) is comparable to the dose profile predicted by the gel nanosensor (2.3 Gy), which demonstrates the capability of the gel nanosensor to qualitatively and quantitatively detect complex topographical dose profiles. Photo credit:Sahil Inamdar, Arizona State University. Upphovsman:Science Advances, doi:10.1126/sciadv.aaw8704.
To investigate translational potential of the gel nanosensor and predict topographical profiles of radiation, Pushpavanam et al. first used a head and neck phantom model. They delivered an irregular crescent-shaped radiation dose near the eye to mimic clinically challenging administration modes of radiotherapy close to critical structures such as the eye during skin cancer treatment. The dose profile delivered using the treatment planning system was in excellent agreement with the predictions of the gel nanosensor. Indicating its capability to detect and predict complex radiation patterns similar to those used in clinical human radiotherapy.
During preclinical studies, the research team used two canine models undergoing radiotherapy to investigate the efficiency of gel nanosensors as independent, nanoscale radiation dosimeters for the first time and compared the efficiency with conventional clinical radiochromic films. On completion of the treatment, Pushpavanam et al. observed maroon color formation in one-half of the gel, whereas the non-irradiated region remained colorless. They showed predictions of the gel nanosensor in the irradiated region to agree excellently with the treatment planning system and the radiochromic film. The gel nanosensor also predicted for the region external to the irradiation to receive minimal radiation and their topographical dose profiles as well. The performance was comparable to clinical radiochromic films but with faster than conventional wait times (typically> 24 hours) to obtain the results. The scientists demonstrated the simplicity of fabrication, operation, readout time and cost effectiveness ($ 0.50 per gel material only) of the frugal invention. They maintained the response of the gel nanosensor for at least seven days to indicate long-term retrieval of dosing data unlike with fluorescence-based dosimeters with readouts that lasts mere minutes.
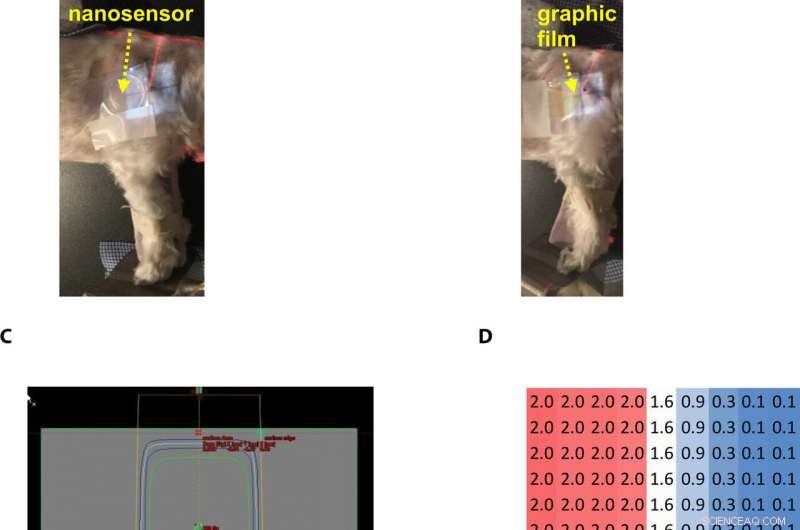
Gel nanosensor enabled topographical detection and quantification of radiation delivered to canine patient A undergoing clinical radiotherapy. Representative image of (A) half of the gel nanosensor and (B) half of the radiographic film positioned in the radiation field delivered to canine patient A. (C) Treatment planning software depicting the delivery of a 2-Gy dose delivered to the surface of patient A (neon green edge along the rectangular gray box indicates the region receiving the 2-Gy dose). (D) The irradiated region received a dose of 2 Gy (highlighted in red squares), with irradiation dose dropping to a minimal radiation 0.1 Gy (highlighted in blue squares) outside the field of irradiation. A color change is visible in both the (E) gel nanosensor whose color changes to maroon and (F) radiographic film whose color changes to dark green after irradiation. The predicted dose map in the gel nanosensor (Na2S addition wait time of 30 min and incubation time of 10 min) and radiographic film are shown below each corresponding sensor. Similarity in the dose profiles indicates the efficacy of the gel nanosensor for clinical dosimetry. The time for readout of the gel nanosensor was 1 hour after irradiation, while the radiochromic film required>24 hours of developing time before readout. All experiments were carried out three independent times. Photo credit:Sahil Inamdar, Arizona State University. Upphovsman:Science Advances, doi:10.1126/sciadv.aaw8704.
På det här sättet, Karthik Pushpavanam and colleagues developed the first colorimetric gel nanosensor as a nanoscale dosimeter to detect and distinguish regions exposed to irradiation. They optimized the platform with a chemical quenching agent (Na 2 S) to accurately reveal topographical dose distribution during clinical radiotherapy. The scientists can control the pore size distribution of the gel substrate to enhance efficacy of the nanosensor. They tested the efficiency of the gel nanosensor to predict complex topographical dose profiles in anthromorphic head and neck phantoms and in live canine patients undergoing radiotherapy. The highly disruptive and translational potential of the gel nanosensor technology will lead to improved patient safety and outcomes in clinical radiotherapy.
© 2019 Science X Network