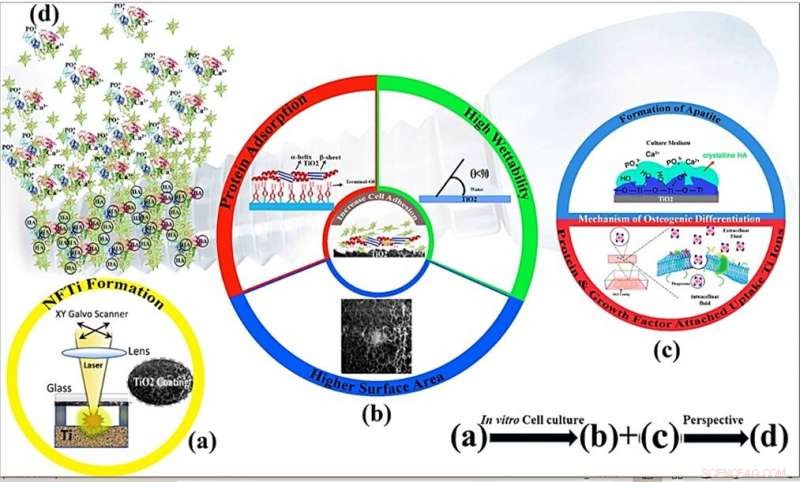
Schematiska mekanismer för cellproliferation och osteoinduktivitet av nanofibrös titanbeläggning genom ytmodifiering genom högintensiv laserinducerad omvänd överföring (HILIRT):En ny deponeringsmetod. (a) NFTi-skikt avsatt på glas med den föreslagna HILIRT-tekniken vid laserstråleskanningshastigheter. (b) Biokompatibiliteten hos titan som implantatmaterial tillskrivs ytoxid som spontant bildas i luft och/eller fysiologiska vätskor, och man tror att cellulära beteenden, t.ex., adhesion, spridning och spridning påverkas i hög grad av 1. Ytarea 2. vätbarhet 3. hydroxylgrupper på ytan (Hydroxylgrupperna på ytan av terminal OH- reglerar de initiala proteinadsorptionsbeteendena). (c) Ythydroxylgrupper och bioaktiva Ti-nanopartiklar främjar osteoblastdifferentiering genom 1. Ti-OH-grupperna som bildas på ytan av titanat efter blötläggning i osteogent odlingsmedium är negativt laddade, och därför kombineras selektivt med de positivt laddade Ca2+-jonerna i vätskan för att så småningom bilda kalciumfosfat. 2. Biokomplex (joner, protein och tillväxtfaktor) internaliseras av kaveolförmedlad endocytos. (d) Perspektiv:Benbildning och ombyggnad kring implanterade material. Kredit:Scientific Reports, doi:10.1038/s41598-019-54533-z
I en ny studie publicerad på Vetenskapliga rapporter , Mohammad-Hossein Beigi och ett forskarteam vid avdelningarna för teknik och tillämpad vetenskap och cellulär bioteknik i Kanada och Iran beskrev en ny metod för att bilda biokompatibla biomaterial för benvävnadsteknik. De konstruerade webbliknande, tredimensionella (3-D) Titania nanofibrösa beläggningar med hög intensitet laserinducerad omvänd överföring (HILIRT). Teamet demonstrerade först mekanismen för ablation och titan (Ti) avsättning på glassubstrat med hjälp av flera pikosekunders laserpulser i omgivande luft för att jämföra teoretiska förutsägelser med experimentella resultat. De undersökte prestandan hos glasprover som utvecklats genom att belägga titanoxid nanofibrösa strukturer genom olika laserpulslängder, använda metoder som svepelektronmikroskopi (SEM).
För att förstå interaktioner mellan den nya materialytan och biologiska celler, Beigi et al. utforskade interaktioner mellan mänskliga benhärledda mesenkymala stamceller (BMSCs) odlade på de nya biomaterialen. För detta, de använde en mängd olika laboratorietester inklusive en kolorimetrisk metod för att förstå cellernas metaboliska aktivitet (MTS-analys), immuncytokemi, proteinadsorption och absorptionsanalyser. Resultaten visade signifikant förbättrad biokompatibilitet i laserbehandlade prover jämfört med obehandlade substrat. Beigi et al. modifierade sin HILIRT-teknik genom att minska pulslängden och generera titananofiber med tätare strukturer under avancerad materialteknik. Enligt deras fynd, densiteten av nanostrukturer och koncentrationen av belagda nanofibrer spelade en avgörande roll för att generera bioaktivitet i de behandlade proverna genom att inducera tidig differentiering av BMSCs (benhärledda mesenkymala stamceller) för att bilda benvävnad via osteogen differentiering (benbildning).
Bioingenjörer utvecklar snabbt nya tekniker för benvävnadsteknik (BTE) för benregenerering; att förbättra de befintliga "guldstandarderna" för benautograft- och allograftmetoder inom regenerativ medicin. Nackdelar med de befintliga teknikerna inkluderar morbiditet hos givarstället och begränsade näringstillskott under benregenerering. Benvävnadsteknik (BTE) är en lovande forskningsinriktning för att underlätta bentillväxt och reparation, även vid storskaliga skelettdefekter. Forskare siktar på att använda stamceller med BTE på grund av deras självförnyande förmåga tillsammans med stamcellsdifferentiering, att bilda en mängd olika vävnadstyper. Eftersom de fysiska och kemiska egenskaperna hos en materialyta kan påverka livsdugligheten hos mänskliga mesenkymala stamceller (hMSC) för självrestaurering, differentiering och spridning. Material och celler kan därför arbeta tillsammans i tillämpningar av BTE för att tillhandahålla en önskad plattform för osseointegration under benremodellering.
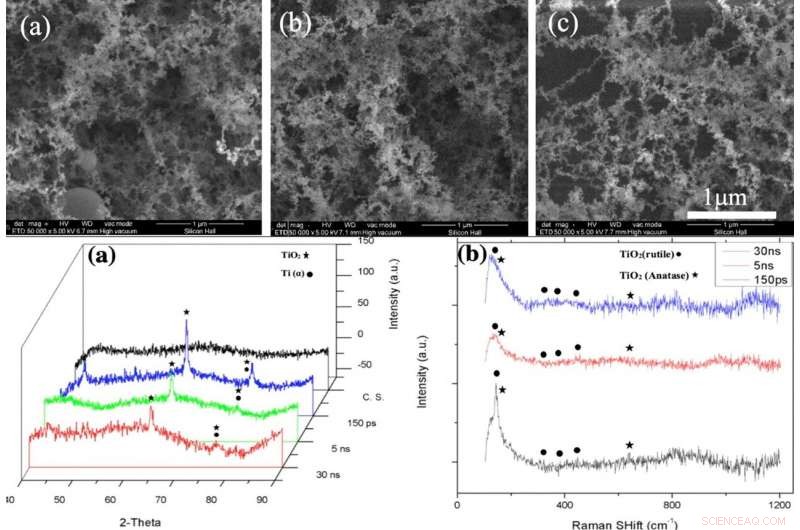
TOP:SEM-bilder av NFTi-skikt (Nanofibrous Titania) med effekt = 10 W, frekvens = 600 KHz (a) pulslängd = 150 ps, (b) pulslängd = 5 ns, (c) pulslängd = 30 ns med 50000X förstoring. NEDERST:(a) XRD-mönster, (b) Raman-spektrum av rent glas och prover belagda med titanoxid med olika pulslängder (skapat av Origin Pro 2019B (GF3S4-3089-7907079) https://www.originlab.com/). Kredit:Scientific Reports, doi:10.1038/s41598-019-54533-z.
Forskningsteam hade tidigare använt flera tekniker för att producera BTE-materialytor inklusive sol-gel, hydrotermisk 106, elektrospinning och 3D-utskrift; dock, att välja en idealisk metod är fortfarande en utmaning. Till exempel, artificiella biomaterial måste interagera utan ansträngning med fysiologiska vätskor och assimileras med hårda och mjuka omgivande vävnader för att upprätthålla cellulär aktivitet för överlägsen biokompatibilitet. Materialforskare och bioingenjörer hade använt titan och dess legeringar för ortopediska implantat, möjliggör titan-nanopartikel (NP)-baserad osteogenes av tandmassastamceller och fetthärledda stamceller. Metoder för att modifiera ytan med laser kan modifiera materialytor för förbättrad biokompatibilitet för ytan; där HILIRT-metoden tidigare hade visat potential att konstruera lab-on-a-chip komponenter och andra biokompatibla biomaterial. Forskare kan ändra laserparametrar för att manipulera materialytor för att underlätta celldifferentiering.
I detta arbete, Beigi et al. undersökte effekter av laserpulslängd på materialytor med hjälp av HILIRT-metoden och testade det biologiska beteendet hos syntetiska biomaterial med hjälp av materialkarakterisering och biologiska tester i labbet. De undersökte cell-materialkontakt på materialytor med hjälp av genuttryck, mineraliserings- och proteininteraktionsstudier. Forskarna utvecklade en nanofibrös titanoxid (NFTi) tunn film och blötlade den i simulerad kroppsvätska (SBF) för att bilda hydroxiapatit (HA)-liknande lagerstrukturer och identifierade materialytmodifieringarna med hjälp av vattenkontaktvinkel (CA), svepelektronmikroskopi (SEM), energidispersiv röntgenspektroskopi (EDS) analys, mikro-Raman och röntgendiffraktion (XRD) spektroskopier.
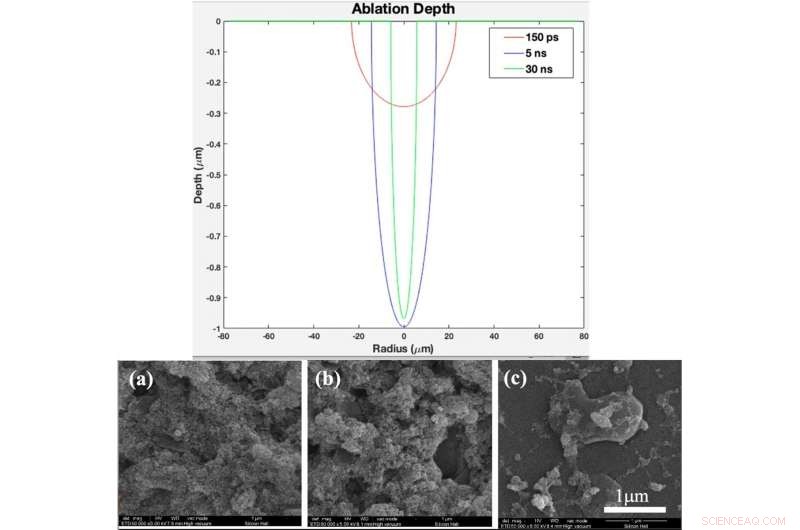
TOP:Teoretisk ablationsdjupprofil som funktion av radie för pulslängd på 150 ps, 5 ns, och 30 ns (skapat i MATLAB R2015b programvara (9.6.0.1072779) https://www.mathworks.com). NEDERST:(a) XRD-mönster, (b) Raman spectrum of bare glass and samples coated by titania with different pulse durations after 2 days immersion in SBF, (c) XRD pattern, (d) Raman spectrum of bare glass and samples coated by titania with different pulse duration after 4 days immersion in SBF Fig. 4. (a). XRD pattern, (b) Raman spectrum of bare glass and samples coated by titania with different pulse durations (created by Origin Pro 2019B (GF3S4-3089-7907079) https://www.originlab.com/). Kredit:Scientific Reports, doi:10.1038/s41598-019-54533-z.
They deposited NFTi (nanofibrous titania) structures at different pulse durations to form laser nanofiber coated smooth surfaces and tested the chemical and physical composition of the resulting advanced materials. When they decreased pulse duration, the titanium weight percentage increased, and the scientists observed the temperature of the irradiated zone to be significantly higher for a shorter pulse duration of 150 picoseconds (ps) compared with 5 nanoseconds (ns) and 30 ns. The decreased pulse duration transmitted power to the target in a shorter time, causing the heat affected zone (HAZ) to have a higher temperature, allowing a denser plasma plume to form more NFTi structures on a glass substrate. Decreasing the laser pulse duration created more biocompatible Ti nanofibers with a higher content of HA(hydroxyapatite)-like substance sedimentation on the samples.
Using phase-contrast microscopy images of fibroblast-like BMSCs on titania-coated glass surfaces, Beigi et al. observed normal cell morphology. They measured water contact angles of droplets of water on the material specimens and conducted cytotoxicity tests with MTS assays on stem cells grown on NFTi coatings. The materials coated with NFTi for 150 ps showed the highest absorbance rate (known as the S1 group) with subsequently high rates of cell viability, cell adhesion and metabolic activity. When the researchers used immunofluorescent staining to observe cell migration, the S1 sample (with NFTi coating for 150 ps) showed higher rates of cell migration. To confirm stem cell (BMSC) differentiation, the scientists investigated osteogenic-related gene expression with RUNX2, collagen I, osteopontin and osteonectin genes, using quantitative qRT-PCR. Bland proverna, S1 samples indicated significantly higher relative expression for all osteogenic-related genes.
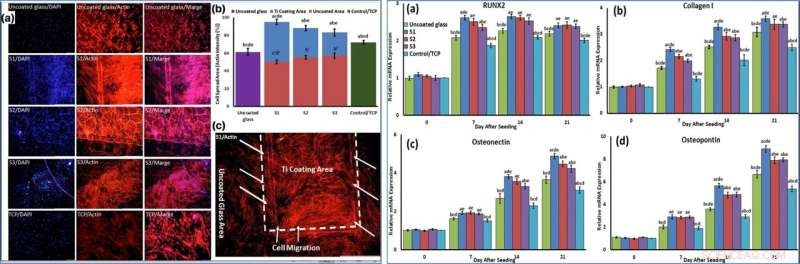
LEFT:Cells were stained by phalloidin to observe (a, c) and quantify (b) actin filament expansion and migration in all samples after 7 days. The first column in A is DAPI nuclear staining (blue), second column, phalloidin labelled F-actin (red), and third column, overlaid fluorescent image of immunostained cellular components (merge:DAPI/F-actin). The red bars in B indicate the intensity percentage of actin filament on the glass in S1, S2, and S3 samples and the blue bars describe the intensity percentage of actin filament the NFTi coated area. (c) Higher magnification of BMSCs migration from glass area toward Ti coating area in S1. RIGHT:The mRNA relative expression levels of osteogenic genes included Runx2 (a), Collagen I (b), Osteonectin (c), and Osteopontin (d) determined by qRT-PCR for all samples. Kredit:Scientific Reports, doi:10.1038/s41598-019-54533-z.
To confirm mineralization, the scientists used alizarin red followed by soluble Ca nodules color absorbance quantification, to observe high levels of mineralization on all samples on days seven and 14. The team investigated surface protein absorption potential, protein-ion biocomplex formation and biocomplex cell uptake to demonstrate highest levels of protein-ion biocomplex formation on the S1 samples.
På det här sättet, Mohammad-Hossein Beigi and colleagues used the HILIRT method to achieve high surface bioreactivity, osteogenesis and osseointregration of NFTi-BMSCs. The surface character of the new materials allowed protein and biomolecule interactions to stimulate cell adhesion, mineralization and osteogenesis for faster and more suited osseointegration in vivo and in vitro. The scientists engineered nanofiber mesh-like scaffolds using titanate to allow vascularization, protein attachment, cell proliferation and cell attachment on the substrate. Such microporous surfaces can promote nutrition diffusion, vascularization and blood flow due to improved biomechanical strength. Dessutom, the hydrophilic surface property; verified using water contact angle measurements, facilitated cell-ECM adhesion to improve cell binding and vigorous tissue growth.
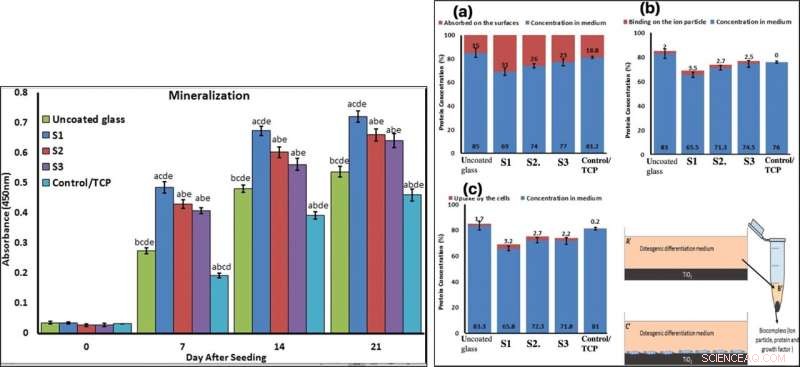
LEFT:Confirmation of osteogenic differentiation and matrix mineralization of BMSCs by quantifying alizarin red staining. RIGHT:Protein adsorption and biocomplex adsorption/absorption:concentration of protein in osteogenic differentiation medium after 6 hours of immersion (a); concentration of protein in osteogenic differentiation medium after 6 hours of immersion and then centrifuged at 14, 000 rpm for 30 min (b); concentration of protein in osteogenic differentiation medium after 6 hours of immersion with cell culture (c). Kredit:Scientific Reports, doi:10.1038/s41598-019-54533-z.
The S1 sample (NFTi, 150 ps) developed in this work generated the best surface bioreactivity for bone regeneration or bone replacement. Beigi et al. showed the advantages of using titania as an orthopedic implant material and the surface modification strategies implemented in the study improved surface bioreactivity and osteogenesis for assisted bone tissue development. The cost-effective frugal method can provide a metallic nanofiber structure surface to be coated on multiple surfaces for varied biomedical applications. The proposed technique (combining materials engineering with stem cells) will open new doors to engineer advanced biomaterials with enhanced surface bioreactivity for improved biocompatibility in vitro and in vivo. The findings demonstrate beneficial effects of an experimental scaffold in the lab with potential for medical osseointegration as a BTE implant.
© 2019 Science X Network