Intramolekylär Diels-Alder-reaktion diskuterad i forskningen. Upphovsman:Fedor Zubkov
Forskare från RUDN University och Ivan Franko National University i Lviv har hittat ett sätt att producera aromatiska ringar i organiska föreningar i tre steg. Dessa steg fortskrider successivt i en-grytförhållanden och vid rumstemperatur. Nu analoger av hormoner, steroider, några sockerarter, terpener och andra komplexa organiska ämnen kan syntetiseras snabbare och under mjukare förhållanden. Tidningen publicerades i Tetrahedron Letters.
Steroider är ämnen med hög biologisk aktivitet. De inkluderar antiinflammatoriska läkemedel (t.ex. deksametason), samt några hormoner. Dessutom, steroider används för att producera vitamin D. Sju nobelpriser delades ut mellan 1927 och 1975 för att studera dessa viktiga ämnen. Syntetisera steroider är inte alltid lätt, eftersom de är baserade på ett polysubstituerat tetracykliskt system. Kemister från RUDN University och deras ukrainska kollegor hittade ett nytt sätt att producera steroider och andra ämnen som innehåller ringar med sex led.
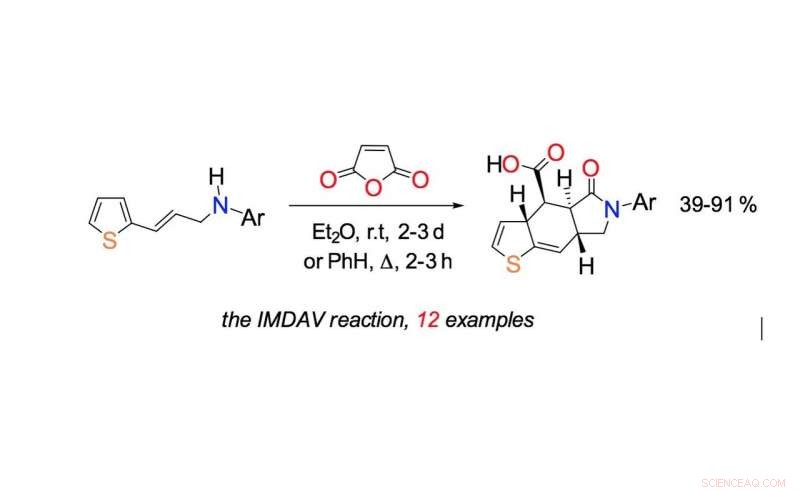
"Signaturmomentet för den syntetiska delen är en tandemkaskad av reaktioner-reaktionerna fortsätter successivt i samma kolv under samma reaktionsbetingelser:acylering av kväveatomen i utgångs-3-tienylallylaminet med maleinsyraanhydrid, den intramolekylära Diels-Alder-reaktionen och efterföljande aromatisering av cykloadditionsaddukten, "säger Fedor Zubkov, biträdande professor vid institutionen för organisk kemi vid RUDN University.
Dieensyntes (eller Diels-Alder-reaktionen) är en av de mest populära reaktionerna inom organisk kemi. Det innebär synkron bildning av två sigma-dubbelbindningar från en dubbelbindning av dienofil och två dubbelbindningar av dien; huvudprodukten är en sexledad ring med en dubbelbindning. Otto Diels och Kurt Alder fick Nobelpriset 1950 för denna reaktion. En annan nobelpristagare, Robert Woodward, inspirerades och band sitt liv med kemi efter att ha läst om Diels-Alders reaktion. Senare, han återvände till det i sina studier flera gånger. Märkligt nog, det var Robert Woodward som grundade Tetrahedron bokstäver tidning, som publicerade denna uppsats av ryska forskare.
Den intramolekylära Diels-Alder-reaktionen löper inuti en molekyl. Med denna reaktion, komplexa molekyler inklusive sexledade ringar kan syntetiseras i ett steg. Kemister kan styra hur reaktionen går och bindningarna som är involverade i den. Genom att reglera villkoren, de kan få exakt de nödvändiga isomererna - ämnena med samma antal atomer i molekylen, men med olika strukturformler. Forskarna fick reda på att vinyltiofener är lämpliga för denna uppgift.
"Vi kan se att sexledade cykler bildas-de strukturella motiv som oftast finns i naturligt biologiskt aktiva föreningar (alkaloider, sockerarter, hormoner, steroider, terpener och andra). I regel, interaktionen mellan dien och dienofil (beståndsdelarna i dien -syntesen) kräver inte svåra temperaturförhållanden eller användning av katalysatorer, och de bildade produkterna är mycket rena och lätt isolerade, "Fedor Zubkov kommenterar.
Tidigare, enligt Fedor Zubkov, syntes av liknande ämnen krävde en temperatur på 160 ° C för att producera den önskade sexledade ringen. I den nya studien, denna process tar två till tre dagar vid rumstemperatur. Reaktionen går snabbare i kokande bensen (vid 80 ° C) - det tar bara två timmar. I detta fall, dock, slutprodukten är förorenad med föroreningar. Processen körs i tre steg och utbytet av önskade reaktionsprodukter är 39 till 91 procent, vilket är tillräckligt för att snabbare syntetisera hormonliknande läkemedelskomponenter och många andra kemikalier, mer bekvämt och mer effektivt än tidigare.