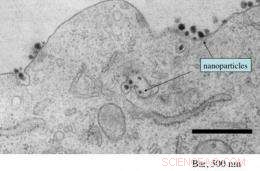
Detta elektronmikrofotografi visar närvaron av ett flertal siRNA-innehållande riktade nanopartiklar både som kommer in i och i en tumörcell. Kredit:Caltech/Swaroop Mishra
Ett team av forskare och kliniker som leds av California Institute of Technology (Caltech) har publicerat det första beviset på att en riktad nanopartikel – som används som ett experimentellt terapeutiskt medel och injiceras direkt i en patients blodomlopp – kan trafikera tumörer, leverera dubbelsträngade små störande RNA (siRNA), och stänga av en viktig cancergen med hjälp av en mekanism som kallas RNA-interferens (RNAi). Dessutom, teamet gav den första demonstrationen att denna nya typ av terapi, infunderas i blodomloppet, kan ta sig till mänskliga tumörer på ett dosberoende sätt - dvs. ett högre antal nanopartiklar som skickas in i kroppen leder till ett högre antal nanopartiklar i tumörcellerna.
Dessa resultat, publicerad i den 21 mars förhandsupplagan av tidskriften Natur , demonstrera genomförbarheten av att använda både nanopartiklar och RNAi-baserad terapi hos patienter, och öppna dörren för framtida "spelförändrande" terapier som attackerar cancer och andra sjukdomar på genetisk nivå, säger Mark Davis, Warren och Katharine Schlinger professor i kemiteknik vid Caltech, och forskargruppens ledare.
Upptäckten av RNA-interferens, mekanismen genom vilken dubbla strängar av RNA tystar gener, vann forskarna Andrew Fire och Craig Mello 2006 års Nobelpris i fysiologi eller medicin. Forskarna rapporterade först att de hittade denna nya mekanism i maskar 1998 Natur papper. Sedan dess, potentialen för denna typ av genhämning att leda till nya terapier för sjukdomar som cancer har varit mycket hyllad.
"RNAi är ett nytt sätt att stoppa produktionen av proteiner, " säger Davis. Vad gör det till ett så potentiellt kraftfullt verktyg, han lägger till, är det faktum att dess mål inte är ett protein. De sårbara områdena av ett protein kan vara dolda inom dess tredimensionella veck, vilket gör det svårt för många terapeuter att nå dem. I kontrast, RNA-interferens riktar sig mot budbärar-RNA (mRNA) som kodar för informationen som behövs för att göra ett protein i första hand.
"I princip, säger Davis, "det betyder att varje protein nu kan drogas eftersom dess hämning åstadkoms genom att förstöra mRNA. Och vi kan gå efter mRNA på ett mycket designat sätt med tanke på all genomisk data som finns och kommer att bli tillgänglig."
Fortfarande, det har funnits många potentiella vägspärrar för tillämpningen av RNAi-teknologi som terapi hos människor. En av de mest problematiska har varit att hitta ett sätt att färja terapierna, som består av ömtåliga siRNA, in i tumörceller efter direkt injektion i blodomloppet. Davis, dock, hade en lösning. Redan innan upptäckten av RNAi, han och hans team hade börjat arbeta på sätt att leverera nukleinsyror till celler via systemisk administrering. De skapade så småningom ett fyrakomponentsystem – med en unik polymer – som kan självmontera till en målinriktad, siRNA-innehållande nanopartikel. SiRNA-leveranssystemet är under klinisk utveckling av Calando Pharmaceuticals, Inc., ett Pasadena-baserat nanobioteknikföretag.
"Dessa nanopartiklar kan ta siRNA till den riktade platsen i kroppen, säger Davis. När de väl når sitt mål – i det här fallet, cancercellerna i tumörer – nanopartiklarna kommer in i cellerna och frigör siRNA.
De vetenskapliga resultaten som beskrivs i Natur papper är från en klinisk fas I-prövning av dessa nanopartiklar som började behandla patienter i maj 2008. Fas I-studier är, per definition, säkerhetsförsök; Tanken är att se om och på vilken nivå läkemedlet eller annan behandling blir skadlig eller giftig. Dessa försök kan också ge ett vetenskapligt bevis på begreppet inom människan – vilket är exakt vad som rapporteras i Nature-tidningen.
Denna riktade nanopartikel som används i studien och som visas i detta schema är gjord av en unik polymer och kan ta sig till mänskliga tumörceller på ett dosberoende sätt. Kredit:Caltech/Derek Bartlett
Med hjälp av en ny teknik utvecklad på Caltech, teamet kunde upptäcka och avbilda nanopartiklar inuti celler biopsierade från tumörer från flera av försökets deltagare. Dessutom, Davis och hans kollegor kunde visa att ju högre nanopartikeldos som administrerades till patienten, ju högre antal partiklar som finns inuti tumörcellerna – det första exemplet på denna typ av dosberoende respons med riktade nanopartiklar.
Ännu bättre, Davis säger, bevisen visade att siRNA hade gjort sitt jobb. I de tumörceller som analyserats av forskarna, mRNA som kodar för celltillväxtproteinet ribonukleotidreduktas hade brutits ned. Denna försämring, i tur och ordning, ledde till förlust av proteinet.
Mer relevant, mRNA-fragmenten som hittades var exakt den längd och sekvens de borde ha om de hade klyvts på den plats som siRNA:t riktade mot, konstaterar Davis. "Det är första gången någon har hittat ett RNA-fragment från en patients celler som visar att mRNA klipptes vid exakt rätt bas via RNAi-mekanismen, " säger han. "Det bevisar att RNAi-mekanismen kan hända med siRNA i en människa."
"Det finns många cancermål som effektivt kan blockeras i laboratoriet med hjälp av siRNA, men att blockera dem på kliniken har varit svårfångade, säger Antoni Ribas, docent i medicin och kirurgi vid UCLA:s Jonsson Comprehensive Cancer Center. "Detta beror på att många av dessa mål inte kan blockeras av traditionellt utformade anticancerläkemedel. Denna forskning ger det första beviset på att det som fungerar i labbet skulle kunna hjälpa patienter i framtiden genom den specifika leveransen av siRNA med hjälp av riktade nanopartiklar. Vi kan börja fundera på att rikta in oss på det omålbara."
"Även om dessa data är mycket tidiga och mer forskning behövs, detta är en lovande studie av ett nytt cancermedel, och vi är stolta över vårt bidrag till den initiala kliniska utvecklingen av siRNA för behandling av cancer, " säger Anthony Tolcher, chef för klinisk forskning vid South Texas Accelerated Research Therapeutics (START).
"Lovande data från de kliniska prövningarna validerar vår år av forskning vid City of Hope om ribonukleotidreduktas som mål för nya genbaserade terapier för cancer, " tillägger medförfattare Yun Yen, biträdande direktör för translationell forskning vid City of Hope. "Vi ser för första gången användbarheten av siRNA som cancerterapi och hur nanoteknik kan rikta sig mot cancerceller specifikt."
Fas I-studien – sponsrad av Calando Pharmaceuticals – pågår vid START och UCLA:s Jonsson Comprehensive Cancer Center, och de kliniska resultaten av prövningen kommer att presenteras vid ett senare tillfälle. "Åtminstonde, vi har bevisat att RNAi-mekanismen kan användas i människor för terapi och att den riktade leveransen av siRNA möjliggör systemisk administrering, " säger Davis. "Det är en mycket spännande tid."