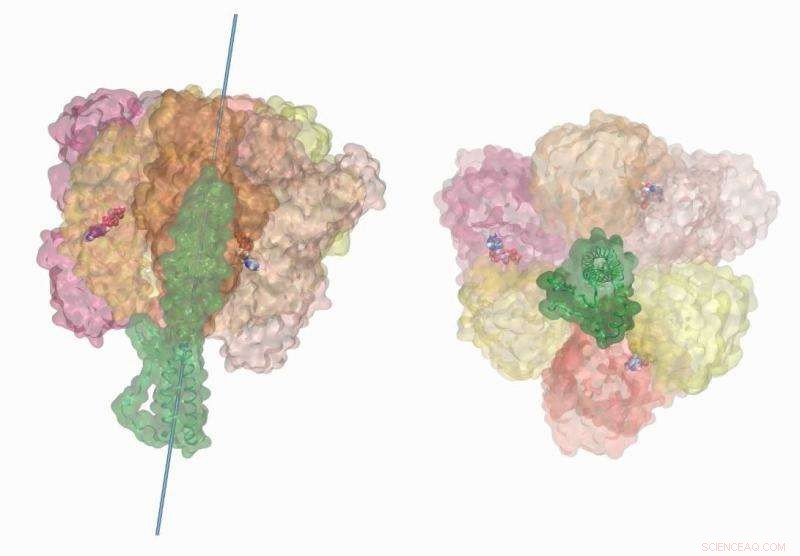
ATP-hydrolysdriven rotation av den centrala stjälken i ATP-syntaset av V-typ av bakterierna Enterococcus hirae skildrar kemo-mekanisk koppling av den molekylära motorn. Dessa simuleringar utfördes på Titan superdator med NAMD2.12. Visualisering och filmrendering slutfördes på VMD1.9.3. Kredit:Barry Isralewitz, University of Illinois i Urbana-Champaign
Trots den stora mångfalden bland levande organismer, molekylen som används för att lagra och överföra energi inom aerob, eller syreanvändande, celler är anmärkningsvärt lika. Från bakterier till svampar, växter, och djur, adenosintrifosfat (ATP) fungerar som livets universella energivaluta, bränsle till de processer som cellerna behöver för att överleva och fungera.
Under loppet av en dag, en individ kommer vanligtvis att använda motsvarande hans eller hennes kroppsvikt i ATP; dock, människokroppen bär bara en liten mängd av molekylen åt gången. Det betyder att celler ständigt måste återvinna eller fylla på sin begränsade kapacitet, förlitar sig på en mycket effektiv molekylär motor som kallas ATP-syntas för att göra jobbet.
Som en del av ett projekt dedikerat till att modellera hur encelliga lila bakterier förvandlar ljus till mat, ett team av beräkningsforskare från University of Illinois i Urbana-Champaign (UIUC) simulerade en komplett ATP-syntas i detalj av alla atomer. Arbetet bygger på projektets första fas – en fotosyntetisk organell med 100 miljoner atomer som kallas en kromatofor – och ger forskare en aldrig tidigare skådad inblick i en biologisk maskin vars energieffektivitet vida överträffar den hos alla konstgjorda system.
Föreslog först under ledning av avlidne Klaus Schulten, en pionjär inom området beräkningsbiofysik och grundaren av Theoretical and Computational Biophysics Group vid UIUC, forskningen har framskridit under ledning av Abhishek Singharoy, co-rektor utredare och en National Science Foundation postdoktor vid UIUC:s Center for the Physics of Living Cells.
Förutom Singharoy, teamet inkluderar medlemmar från grupperna av UIUC-professorerna Emad Tajkhorshid, Zaida Luthey-Schulten och Aleksei Aksimentiev; forskaren Melih Sener; och utvecklarna Barry Isralewitz, Jim Phillips, och John Stone. Den experimentella samarbetspartnern Neil Hunter från University of Sheffield i England deltog också i projektet.
Det UIUC-ledda teamet byggde och testade sin megamodell under en flerårig tilldelning som tilldelades genom programmet Innovative and Novel Computational Impact on Theory and Experiment på Titan superdator, en Cray XK7 som förvaltas av det amerikanska energidepartementets (DOE:s) Oak Ridge Leadership Computing Facility (OLCF), en DOE Office of Science User Facility belägen vid DOE:s Oak Ridge National Laboratory.
Med hjälp av Titan, teamet producerade ett virtuellt verktyg som i exakta detaljer kan förutsäga den kemiska energiproduktionen från ett fotosyntetiskt system baserat på mängden solljus som absorberas. Forskningen kan en dag bidra till avancerad ren energiteknik som innehåller biologiska koncept.
"Naturen har designat kromatoforen på ett sådant sätt att den kan generera tillräckligt med ATP för att dessa bakterier ska överleva i miljöer med svagt ljus som botten av dammar och sjöar, "Singharoy sa. "Vårt arbete fångade denna energiomvandlingsprocess i detalj i alla atomer och tillät oss att förutsäga dess effektivitet."
Ljus i rörelse
Benämns ofta som cellens kraftverk, ATP-syntas är ett komplext enzym som påskyndar syntesen av dess molekylära prekursorer, adenosindifosfat (ADP) och fosfat. Inbäddad i kromatoforens inre och yttre membran, den enzymatiska motorn består av tre huvuddelar - en jondriven rotor, en central stjälk, och en proteinring.
Liknar ett vattenhjul som vrids av kraften från en strömmande ström, ATP-syntasrotorn utnyttjar den elektrokemiskt sporrade rörelsen av joner, såsom protoner eller natrium, från hög koncentration till låg koncentration över membranet. Den resulterande mekaniska energin överförs till den centrala stjälken, som hjälper proteinringen att syntetisera ATP.
Anmärkningsvärt, processen fungerar lika bra omvänt. När för många joner byggs upp på utsidan av kromatoforen, ATP-syntasproteinringen kommer att bryta ner ATP till ADP, en process som kallas hydrolys, och joner kommer att flöda tillbaka till insidan.
"I vanliga fall, du kan förvänta dig mycket energiförlust under denna process, som i alla konstgjorda motorer, men det visar sig att ATP-syntas har väldigt lite avfall, "Singharoy sa. "Hur denna motor är designad för att minimera energiförlusten är frågan vi började ställa."
På samma sätt som en pysslare som tar isär en motor för att bättre förstå hur den fungerar, Singharoys team bröt ner 300, 000-atoms enzym i dess beståndsdelar. Utifrån årtionden av forskning om ATP-syntas, tidigare modeller, och nya experimentella data från ett japanskt team ledd av Takeshi Murata från RIKEN Center for Life Science Technologies, teamet konstruerade och simulerade bitarna i ATP-syntaspusslet oberoende och tillsammans på Titan.
För att fånga viktiga processer som utspelar sig över millisekunders tidsskalor, Singharoy, i samarbete med Christophe Chipot från French National Centre for Scientific Research och Mahmoud Moradi vid University of Arkansas, använde den molekylära dynamikkoden NAMD strategiskt. Teamet genomförde en ensemblestrategi, spåra rörelsen på cirka 1, 000 kopior av ATP-syntas samtidigt med tidssteg på 2 femtosekunder, eller 2, 000 biljondelar av en sekund. Totalt, laget samlade på sig 65 mikrosekunder (65 miljondelar av en sekund) av simuleringstid, använda denna information för att extrapolera rörelser som inträffar under loppet av en millisekund (1 tusendels sekund).
Som ett resultat, teamet identifierade tidigare odokumenterade vridningsrörelser i proteinringen som hjälper till att förklara den molekylära motorns effektivitet. Liknande, lagets simuleringar fångade den gummibandsliknande elasticiteten hos enzymets centrala stjälk. Singharoys team uppskattade att när de parades med proteinringen, stjälken absorberar cirka 75 procent av den energi som frigörs vid hydrolys.
Dessutom, simuleringar av proteinringen i sig avslöjade en enhet som kan fungera oberoende, ett fynd som rapporterats i experiment men inte i beräkningsdetaljer. "Även i frånvaro av mittskaftet, proteinringen i sig är kapabel till ATP-hydrolys. Det är inte särskilt effektivt, men den har förmågan, " sa Singharoy.
Den stora bilden
Efter att ha simulerat dess kompletta ATP-syntasmodell, UIUC-teamet införlivade enzymet i sin tidigare konstruerade kromatoformodell för att få den mest omfattande bilden av ett fotosyntetiskt system hittills.
Med denna virtuella biologiska solpanel, teamet kunde mäta varje steg i energiomvandlingsprocessen – från ljusskörd, till elektron- och protonöverföring, till ATP-syntes – och bättre förstå dess mekaniska grund.
Naturens kromatofor är designad för svag ljusintensitet, absorberar bara mellan 3 och 5 procent av solljuset en vanlig dag. Laget, genom ansträngningar av Sener, fann att denna absorptionshastighet översätts till cirka 300 ATP per sekund, vilket är mängden en bakterie behöver för att överleva.
Efter att ha studerat naturens design, laget ville nu se om det kunde förbättra det. Om man antar samma mängd ljusintensitet, teamet designade en konstgjord kromatofor med en avgjort onaturlig proteinsammansättning, öka närvaron av två typer av specialiserade proteiner. Analys av den nya designen förutspådde en tredubbling av det fotosyntetiska systemets ATP-produktion, öppnar upp möjligheten för kromatoforens människostyrda optimering.
"Du kan potentiellt genetiskt modifiera en kromatofor eller ändra dess koncentration av proteiner, ", sade Singharoy. "Dessa förutsägelser lovar att föra fram nya utvecklingar inom artificiell fotosyntes."
Under sin senaste INCITE-tilldelning, UIUC-teamet vänder sig till energiomvandling i en annan livsform:djur. Med det som den har lärt sig från modellering av fotosyntes i lila bakterier, teamet modellerar cellandning, den process som djurceller använder för att omvandla näringsämnen till ATP.
"Du har minst två proteiner gemensamma mellan andning och fotosyntes, sa Singharoy, som fortsätter sitt engagemang i projektet som biträdande professor vid Arizona State University. "Frågan är vilka designprinciper som överförs till högre organismer?"
Livet på plats
Simulering av kromatoforen – komplett med ATP-syntas – markerar ett pågående skifte i beräkningsbiofysik från att analysera enskilda celldelar (t.ex. enskilda proteiner och hundratals atomer) för att analysera hela cellsystem (t.ex. hundratals proteiner och miljontals atomer).
Schulten, som dog i oktober 2016, förstod bättre än de flesta andra betydelsen av att använda datorer för att simulera naturen. I en intervju 2015, han lade ut sin motivering för att modellera kromatoforen. "Motivationen är att förstå ett mycket viktigt steg i livet på jorden som allt liv beror på idag. Energimässigt beror 95 procent av livet på jorden på fotosyntes, inklusive människor, " han sa.
Schulten förstod också milstolpen som en specialiserad organell representerade på vägen mot att simulera en komplett encellig organism. "Vi har inget mindre än en cell som vi skulle kalla levande, " sa han. "Det är den minsta levande varelsen, och vi vill förstå det."
Med nästa generations superdatorer, inklusive OLCF:s toppmöte, kommer att komma online 2018, forskargruppen Schulten som grundades 1989 förbereder sig för att ta sig an den stora utmaningen att simulera en cell.
Under ledning av Tajkhorshid, teamet planerar att simulera den första miljardatomcellen, inklusive de grundläggande komponenterna en cell behöver för att överleva och växa. Förbättringar av NAMD och arbete som görs under OLCF:s program Center for Accelerated Application Readiness hjälper till att förverkliga Schultens och andras vision.
"Vi fortsätter att gå framåt, "Sade Singharoy. "Vår uttömmande studie av en komplett organell i detalj i alla atomer har öppnat dörren för en hel cell i detalj i alla atomer."