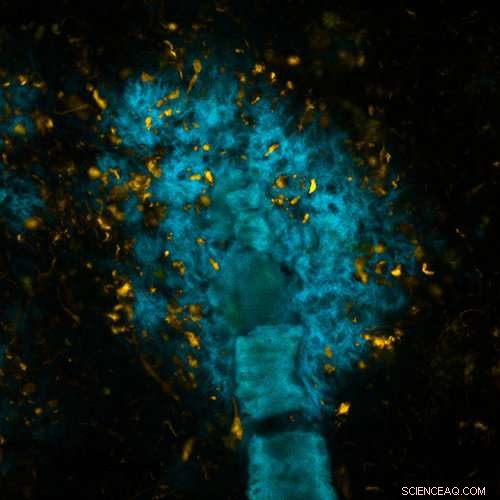
Hjärnvävnad med Alzheimers patologi, färgad med en av de nya tau-specifika molekylerna (orange) och en av de molekyler som tidigare utvecklats av gruppen vid LiU (blå). Bilden är tagen i ett fluorescensmikroskop. Kredit:Peter R Nilsson
Små lysande molekyler utvecklade av forskare vid Linköpings universitet i Sverige kan designas för att skilja mellan plack av olika proteiner i hjärnan. De kan bana väg för bättre diagnos av neurodegenerativa sjukdomar, som Alzheimers sjukdom, där plack bildas från amyloid beta- eller tau-proteinerna.
Forskare vid Linköpings universitet, LiU, har upptäckt att små förändringar i strukturen hos kända spårmolekyler kan göra det möjligt för dem att känna igen antingen amyloid beta eller tau. Dessa små molekyler, som tidigare har utvecklats av forskarna, binder till ett specifikt målprotein. När molekylerna är upplysta, de avger en signal i form av ljus med en annan våglängd.
"Detta öppnar möjligheten att utveckla mer avancerade diagnostiska verktyg för sjukdomar där amyloid beta och tau är involverade, säger Peter Nilsson, professor vid institutionen för fysik, Kemi och biologi. Han har lett studien, som nu har presenterats i den vetenskapliga tidskriften Kemi – En europeisk tidskrift .
Vid flera sjukdomar i hjärnan, långa proteinfibrer, och så småningom trasslas ihop för att bilda täta kroppar som kallas "plack" eller "aggregat". Alzheimers sjukdom, som orsakar demens, är ett välkänt exempel, där placket vanligtvis består av felaktiga varianter av två proteiner:amyloid beta och tau. Men avlagringar av tau-proteinet i hjärnan ses också i en grupp av mindre vanliga tillstånd som kallas "tauopatier".
På senare år har flera fall av hjärnskador hos relativt unga människor med en professionell idrottskarriär har det skrivits mycket om. Kronisk traumatisk encefalopati (CTE) kan förekomma hos personer som har fått slag mot huvudet vid upprepade tillfällen, som kan förekomma i kontaktsporter som boxning, ishockey och amerikansk fotboll. En annan riskgrupp är yrkessoldater. Det enda sättet som för närvarande är tillgängligt för att nå en fast diagnos är under en obduktion. Således, det finns ett akut behov av diagnostiska verktyg som kan användas för att undersöka levande människor, och som kan skilja mellan avlagringar av amyloid beta och tau i hjärnan.
Det som gör dessa molekyler unika är att de har flexibla ryggrader och anpassar sig till strukturen hos det protein som de är bundna till. När molekylen ändrar sin konfiguration, färgen på ljuset som den avger ändras. Forskarna började med en spårmolekyl som bara binder till och känner igen aggregat av amyloid beta. De anpassade denna molekyl för att bli mer lik molekyler som hade utvecklats av andra forskargrupper och som binder till tau. De gjorde två varianter, och det visade sig att en av molekylerna binder väldigt hårt och uteslutande till tau, medan den andra varianten var helt olämplig.
"Vi ser att extremt små förändringar, bara flytta ett par atomer, kan få spårämnesmolekylen att företrädesvis binda till en annan typ av aggregat. Detta innebär att vi kan skräddarsy molekyler för att känna igen olika aggregat, baserat på vilket protein som finns, säger Peter Nilsson.
Forskarna planerar nu att vidareutveckla spårmolekylerna genom att märka dem med radioisotoper, används under positronemissionstomografi (PET). En stor fördel med PET-utredningar är att de kan utföras på levande människor.
"Om vi kan utveckla mer avancerade diagnostiska verktyg som kan skilja mellan amyloid beta och tau, det skulle vara möjligt att avgöra vilket proteinaggregat som bildas först och hur aggregaten interagerar. Det skulle också vara möjligt att undersöka om olika behandlingsformer är effektiva mot en typ av ballast utan att påverka den andra, säger Peter Nilsson.