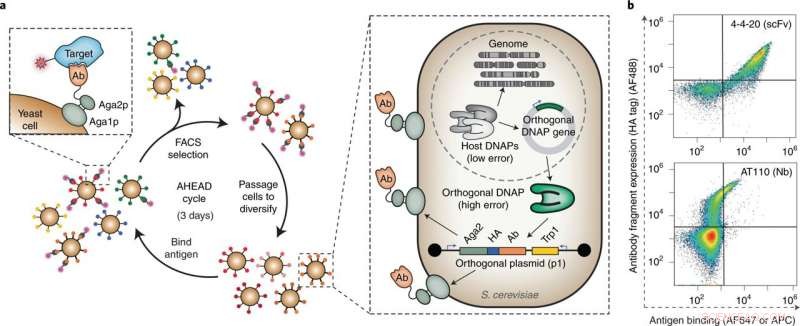
Fig. 1:Autonom hypermutation jäst yta display (AHEAD). a, Schema för den snabba utvecklingen av bindning med hög affinitet med hjälp av AHEAD. Ab, antikroppsfragment; DNAP, DNA-polymeras; HA, hemagglutinin-tagg. b, Cytometriplot som visar detektion av ett funktionellt ytuppvisat enkelkedjigt antikroppsfragment (scFv) och en funktionellt ytvisad nanokropp (Nb) kodad på den ortogonala p1-plasmiden, replikeras av en associerad ortogonal DNAP. Den ortogonala DNAP som användes i det här fallet var wt TP-DNAP1 (metoder) snarare än den felbenägna TP-DNAP1-4-2-varianten som användes för alla efterföljande AHEAD-evolutionsexperiment. Besläktade antigener för 4-4-20 (fluorescein) och AT110 (AT1R) märktes med biotin och FLAG-tagg, respektive, och detekteras med AF647-konjugerad streptavidin och allofykocyanin-konjugerad anti-FLAG, respektive. HA-taggen detekterades med mus-anti-HA och en get-anti-mus AF488-konjugerad sekundär antikropp. Från:Snabb generering av potenta antikroppar genom autonom hypermutation i jäst
När skadliga bakterier eller virus kommer in i kroppen, immunceller upptäcker kontrollanta proteiner som kallas antigener på inkräktarnas ytor och skickar ut arméer av antikroppar för att avvärja dem. Om några av dessa antikroppar har precis rätt form, de kan haka på och blockera antigenerna som nyckeln till ett hänglås.
Men vårt immunsystem har inte alltid de rätta antikropparna för att bekämpa en viss inkräktare. Så under de senaste decennierna har forskare lärt sig att arbeta med djur som kameler och lamor, och att använda syntetiska designtekniker i labbet, att generera antikroppar som kan omvandlas till läkemedel.
Mer än 85 antikroppsterapier har godkänts av FDA hittills, inklusive två beviljade akuttillstånd för behandling av covid-19.
Trots deras framgångar, nuvarande tillvägagångssätt har nackdelar. I ett försök att hoppa över dessa hinder, forskare vid Harvard Medical School och University of California, Irvine, har utvecklat en snabbare, enklare, och billigare adaptiv teknologi för att generera högt specialiserade antikroppar.
De har redan använt plattformen, dubbat AHEAD, att utveckla antikroppar mot viruset som orsakar covid-19. Andra grupper undersöker nu dessa antikroppar som grund för diagnostiska tester och terapier.
"Vi tror att AHEAD kommer att vara ett kraftfullt verktyg för att snabbt upptäcka och optimera antikroppar, speciellt för att ta itu med snabbt utvecklande patogener, sa Andrew Kruse, professor i biologisk kemi och molekylär farmakologi vid Blavatnik Institute vid HMS och co-senior utredare av studien med Chang Liu vid UC Irvine.
Snabbare upptäckt av antikroppar kan påskynda läkemedelsutveckling, diagnostiska tester, och grundläggande vetenskapliga experiment.
Som rapporterats 24 juni in Naturens kemiska biologi , metoden använder jäst för att göra hundratals miljoner olika syntetiska antikroppsfragment som kallas nanokroppar. Forskare kan släppa sitt intressanta antigen – som spikproteinet som SARS-CoV-2 använder för att komma in i och infektera mänskliga celler – i en flaska med jäst och se vilka nanokroppar som sitter fast.
Teamet konstruerade jästen så att nanokropparna utvecklas med varje generation. Det gör att forskare kan ta första omgångens vinnare, lägg dem i en ny flaska, och genomföra en andra sorts för att få nanokroppar som låser sig på antigenet ännu mer framgångsrikt. De kan köra ytterligare rundor tills de är nöjda med att de har en eller flera nanokroppar som binder väl, och bara binder, till det sjukdomsframkallande antigenet, maximera chansen att utveckla en terapi som är effektiv och har minimala biverkningar.
Hela processen använder standardtekniker för laboratoriejästodling och tar bara en och en halv till tre veckor. Forskare kan jaga nanokroppar mot många olika antigener samtidigt.
"Vi kan utveckla antikroppar i tidigare otillgänglig hastighet och skala, " sa Kruse. "Det är ett nytt sätt att göra kombinatorisk proteinteknik."
AHEAD är en förkortning för Autonomous Hypermutation yEast SurfAce Display.
Arbetet bygger på en tidigare plattform ledd av Kruse och en kollega vid University of California, San Francisco. Den nya versionen skiljer sig i sin autonoma utvecklingsförmåga, som efterliknar hur antikroppar naturligt utvecklas i lamadjur och kameler.
"Det är spännande att föra denna kraftfulla immunprocess hos djur till jästceller, " sa Conor McMahon, co-första författare av tidningen med Alon Wellner i Liu-labbet. McMahon utförde arbetet medan han var postdoktor i Kruse-labbet. Han är nu Vertex Fellow på Vertex Pharmaceuticals.
Pandemipotential
Medan AHEAD har potential att producera antikroppar mot hot som cancer och proteiner involverade i autoimmuna tillstånd, Kruse och kollegor är för tillfället fokuserade på att använda tekniken för att bekämpa covid-19.
"Vi ville få det här projektet att gå så fort vi kunde, sa Kruse, "och vi hoppas att vi nu kan agera ännu snabbare om något liknande den här pandemin skulle hända igen."
När forskarna introducerade SARS-CoV-2-antigener i jästflaskorna, de avslöjade nanokroppar som neutraliserade dem minst lika bra som, och i vissa fall bättre än, befintliga antikroppar genererade från mänskliga patienter, djur, och labbexperiment.
Nanokropparna hade varierande framgång med att övertyga antigenerna att binda till dem istället för till ACE2-receptorn, som SARS-CoV-2 använder för att komma in i mänskliga celler.
Vissa kollegor som gick vidare med de mest lovande nanobody-kandidaterna har börjat se liknande resultat i djurmodeller, medan andra använder nanokropparna för att försöka utveckla bättre verktyg för att upptäcka SARS-CoV-2 och relaterade coronavirus, enligt Kruse och medförfattare.
AHEAD kan också hjälpa experter att reagera snabbare när nya SARS-CoV-2-varianter eller helt nya patogener uppstår.
"Om SARS-CoV-2 utvecklas på ett sätt som undgår nuvarande antikroppsterapier för akut användning, vi borde kunna utveckla nya om cirka två veckor för att blockera flyktvarianterna, sa Kruse.
Eftersom "nästan alla biologilabb" är utrustade för att använda den enkla utrustningen och tekniken, AHEAD borde ge många grupper möjlighet att arbeta med att hitta lösningar på framtida utbrott "i ett distribuerat svar som möter problemets brådska, " tillade Kruse.
Debora Marks labb, biträdande professor i systembiologi vid HMS, och Jonathan Abraham, biträdande professor i mikrobiologi vid HMS, bidragit till arbetet. Teamet publicerade en relaterad artikel i Naturkommunikation beskriver de nya beräkningstekniker som de utvecklade för att möjliggöra AHEAD.