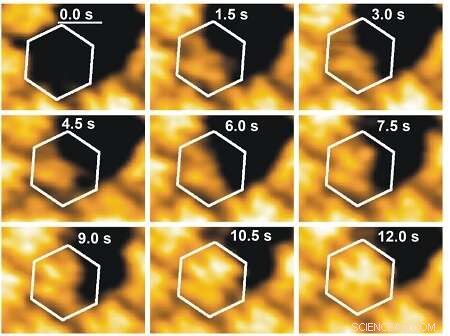
Dynamik för självmontering av en viral proteinstruktur. Den vita sexkanten markerar positionen där en hexamer vid kanten av det växande gallret gradvis bildas från de enda virala proteinsubenheterna. Upphovsman:Wouter Roos
Virusets reproduktionscykel kräver självmontering, mognad av viruspartiklar och, efter infektion, utsläpp av genetiskt material till en värdcell. Ny fysikbaserad teknik gör det möjligt för forskare att studera dynamiken i denna cykel och kan så småningom leda till nya behandlingar. I sin roll som fysisk virolog, Wouter Roos, fysiker vid universitetet i Groningen, tillsammans med två gamla kollegor, har skrivit en översiktsartikel om dessa nya tekniker, som publicerades i Naturrecensioner Fysik den 12 januari.
"Fysik har använts länge för att studera virus, "säger Roos." Fysikens lagar styr viktiga händelser i deras reproduktionscykel. "De senaste framstegen inom fysikbaserade tekniker har gjort det möjligt att studera självmontering och andra steg i reproduktionscykeln för enstaka viruspartiklar och vid sub-sekund tidsupplösning. "Med denna nya teknik kan vi se dynamiken i virus, "Tillägger Roos.
Energi
År 2010, han publicerade först en översiktsartikel om fysologiska aspekter av virologi tillsammans med två av hans kollegor. "Då, nästan all forskning om virus var relativt statisk, till exempel utöva tryck på en viruspartikel för att se hur den reagerade. "Vid den tiden, studier om dynamiska processer, som självmontering, utfördes i bulk, utan möjlighet att zooma in på enskilda partiklar. "Detta har förändrats under de senaste åren och därför vi tyckte att det var dags för en ny granskning. "Den här artikeln, "Physics of Viral Dynamics, "var medförfattare av Robijn Bruinsma från University of California i Los Angeles (USA) och Gijs Wuite från VU Amsterdam (Nederländerna).
Virus kapar celler och tvingar dem att göra proteinets byggstenar för nya viruspartiklar och att kopiera deras genetiska material (antingen RNA eller DNA). Detta resulterar i en cellulär soppa full av virusdelar, som självmonteras för att producera partiklar av inkapslat RNA eller DNA. "Ingen extern energi krävs för denna process. Och även in vitro, de flesta virus kommer att samlas snabbt. "Denna process studerades traditionellt i massmaterial, medelvärde för beteendet hos ett stort antal viruspartiklar. "Så, vi hade ingen aning om variansen i sammansättningen av enskilda partiklar. "
Skanningar under andra sekunden
Under de senaste åren, teknik har utvecklats för att studera dessa enskilda partiklar i realtid. En av dem är snabb Atomic Force Microscopy (AFM). Ett atomkraftmikroskop skannar ytor med en atomstor spets och kan därför kartlägga deras topologi. "Nyligen, AFM:s skanningshastighet ökade dramatiskt och nu kan vi utföra undersökningar på andra sekunder av ytor som mäter mindre än 1 mikrometer i kvadrat med höghastighets-AFM, säger Roos, som själv använder en AFM. "Detta gör att vi kan se hur virusunderenheter samlas på en yta. Det är en mycket dynamisk process, med byggstenar som fäster och släpper. "
Enmolekylär fluorescens används också för att studera virus, till exempel, bindning av virala proteiner till DNA. "Med optisk pincett, vi håller två små pärlor i vardera änden av en DNA -molekyl. När virala proteiner binder till DNA, detta kommer att rinna upp och föra de två pärlorna närmare varandra. Detta visualiseras av fluorescerande markörer fästa på pärlorna. "Alternativt, proteiner med fluorescerande markörer kan observeras medan de fäster vid viralt DNA eller andra proteiner. En tredje teknik är att använda ett optiskt mikroskop för att mäta störningar av ljus som sprids av viruspartiklar. Dessa mönster avslöjar partiklarnas struktur under montering.
Bli tuffare
Andra steg i viruscykeln kan också studeras. "Efter att de har monterat sig själv, partiklar måste hårdna för att klara förhållanden utanför värdcellen, "säger Roos. Andra ändringar sker också, som förbereder partiklarna för att infektera andra celler. Dynamiken i denna mognadsprocess är viktig för vår förståelse av hur virus fungerar. "Och efter att ha infekterat nya celler, viruspartikeln måste gå isär för att släppa sitt genetiska material. "
Ny teknik avslöjar nu den fysiska dynamiken hos virus. Det gör det möjligt för forskare som Roos och hans kollegor att studera hur genetiskt material införlivas och vilka fysiska principer som styr denna process. De flesta antivirala läkemedel stör de första stegen i infektionen, såsom bindning av viruspartiklar till deras värdceller. Med hjälp av denna nya dynamiska information, vi kan utveckla läkemedel som blockerar självmontering eller andra viktiga steg i virusets reproduktionscykel.
Nanoteknik
Insikt i viruspartiklarnas fysik är också viktigt för deras användning i forskning, till exempel som byggstenar inom nanoteknik eller som bärare för antigener i vacciner. Flera av de ledande COVID-19-vaccinerna använder adenovirus för att leverera genen för SARS-CoV-2-spikproteinet till celler, som sedan uttrycker denna gen och följaktligen genererar ett immunsvar. "Att förstå hur adenoviruset går ihop och går sönder kan hjälpa till att skapa mer stabila vacciner."