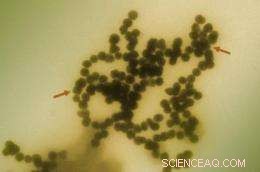
Transmissionselektronmikrofotografi av guldnanopartiklar som samlas i lösning. Avståndet mellan de två röda pilarna är cirka 280 nanometer, cirka 200 gånger mindre än diametern på ett människohår. De individuella nanopartiklarna är cirka 15 nanometer i diameter, ungefär avståndet över tre sida vid sida natriumatomer. Kredit:A. Keene, US Food and Drug Administration
Samma egenskaper som gör konstruerade nanopartiklar attraktiva för många tillämpningar - små som ett virus, biologiskt och miljömässigt stabila, och vattenlösliga - orsakar också oro för deras långsiktiga effekter på miljöhälsa och säkerhet (EHS). En speciell egenskap, tendensen för nanopartiklar att klumpa ihop sig i lösning, är av stort intresse eftersom storleken på dessa kluster kan vara nyckeln till huruvida de är toxiska för mänskliga celler eller inte. Forskare vid National Institute of Standards and Technology har för första gången demonstrerat en metod för att producera nanopartikelkluster i en mängd olika kontrollerade storlekar som är stabila över tid så att deras effekter på celler kan studeras ordentligt.*
I sina tester, NIST-teamet gjorde prover av guld, silver, ceriumoxid och positivt laddade polystyren-nanopartiklar och suspenderade dem separat i cellodlingsmedium, så att klumpar kan uppstå i varje. De stoppade klumpningen genom att tillsätta ett protein, bovint serumalbumin (BSA), till blandningarna. Ju längre nanopartiklarna fick klumpa ihop sig, ju större storleken på det resulterande klustret. Till exempel, en rad klustringstider med 23 nanometer silvernanopartiklar gav en fördelning av massor mellan 43 och 1, 400 nanometer i diameter. Liknande storleksfördelningar för de andra tre nanopartikeltyperna producerades med denna metod.
Forskarna lärde sig att användningen av samma "frysningstider" - de punkter där BSA lades till för att stoppa processen - gav konsekventa storleksfördelningar för alla fyra nanopartikeltyper. Dessutom, alla de BSA-kontrollerade dispersionerna förblev stabila i 2-3 dagar, vilket är tillräckligt för många toxicitetsstudier.
Efter att framgångsrikt ha visat att de kunde kontrollera produktionen av nanopartikelklumpar av olika storlekar, forskarna ville sedan bevisa att deras skapelser kunde användas. Nanopartikelkluster av olika storlekar blandades med hästblod i ett försök att studera effekten av klumpstorlek på röda blodkroppars toxicitet. Förekomsten av hemoglobin, den järnbaserade molekylen i röda blodkroppar som transporterar syre, skulle berätta för forskare om cellerna hade lyserats (uppbrutits) av silverjoner som släppts ut i lösningen från klustren. I tur och ordning, mätning av mängden hemoglobin i lösning för varje klusterstorlek skulle definiera toxicitetsnivån - möjligen relaterad till nivån av silverjonfrisättning - för den specifika medelstorleken.
Vad forskarna fann var att förstörelsen av röda blodkroppar minskade när klustret ökade. De antar att stora nanopartikelkluster löses upp långsammare än små, och därför, släpper ut färre silverjoner i lösningen.
I framtiden, NIST-teamet planerar att ytterligare karakterisera de olika klusterstorlekarna som kan uppnås genom deras produktionsmetod, och använd sedan dessa kluster för att studera effekten på cytotoxicitet av beläggningar (som polymerer) applicerade på nanopartiklarna.