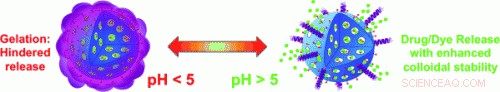
(Phys.org)—Hur kan läkemedel säkert transporteras genom den sura miljön i magen och in i tarmarna? Ett team av kanadensiska och australiensiska forskare har utvecklat en ny nanotransporter som består av porösa partiklar av kiseldioxid stabiliserade med ett vassleprotein. I sura miljöer bildar proteinet en gel som stänger av porerna; vid högre pH-värden, porerna öppnas.
För läkemedel, både läkemedlet i sig och dess leveransform är viktiga, eftersom det senare avgör var och när läkemedlet blir aktivt i kroppen. Till exempel, Formuleringar med förlängd frisättning är utformade för att bibehålla en stabil nivå av läkemedlet under en längre tidsperiod och antitumörläkemedel är avsedda att bli aktiva i sjuka celler så selektivt som möjligt för att minimera biverkningar. För att få detta att fungera måste läkemedlen "förpackas" korrekt. Förpackningar krävs också ofta för mediciner som administreras oralt eftersom många läkemedel förstörs av magsyra innan de kan nå tarmen för att absorberas i blodomloppet. Dock, skyddet mot syra måste också frigöra läkemedlet under de förhållanden som finns i tarmen.
En mycket lovande typ av "läkemedelspaket" är den mesoporösa nanopartikeln av kiseldioxid. Dessa är biokompatibla och lätta att tillverka med de por- och partikelstorlekar som krävs. Kemin hos deras inre och yttre ytor kan lätt modifieras, de kan lätt laddas med läkemedelsmolekyler av olika storlekar, och dessa kan i sin tur släppas ut på ett kontrollerat sätt. Dock, dessa partiklar har en tendens att aggregera under fysiologiska förhållanden, som helt kan förändra deras egenskaper. Också, nya metoder måste utvecklas för att säkerställa selektiv frisättning vid önskat mål. Förändringen i pH i övergången från mage till tarm är en potentiell trigger.
Ett team ledd av Shi Zhang Qiao vid University of Queensland (Brisbane, Australien) och Freddy Kleitz vid Université Laval (Quebec, Kanada) har nu förfinat några nanotransportörer av kiseldioxid, de rapporterar i tidskriften Angewandte Chemie. Deras framgång beror på deras användning av β-laktoglobulin, ett vassleprotein som används som kosttillskott. Forskarna fäste detta på den yttre ytan av de porösa nanopartiklarna, förhindrar deras aggregering och ökar deras biokompatibilitet. Vid pH-värden under 5, som de som finns i magen, β-laktoglobulin geler:det sväller upp och bildar ett gelatin "skal" runt nanopartiklarna, som täpper till porerna och hindrar läkemedlet från att komma ut. Vid högre pH-värden som de i tarmarna, proteinet antar formen av diskreta molekyler, öppnar porerna och frigör läkemedlet.
Förutom magen och tarmen, andra organ har också olika pH-värden — och det finns till och med pH-skillnader mellan vissa tumörer och den omgivande friska vävnaden. Ytterligare utveckling av denna nya procedur kan möjligen användas för att göra nanotransportörer kapabla att reagera på sådana subtilare pH-gradienter.