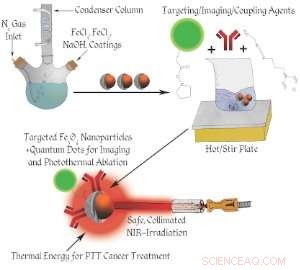
Schematisk konstruktion av nanopartiklar.
Konventionell behandling syftar till att utrota cancerceller genom läkemedel och terapi som levereras utifrån cellen, vilket också kan påverka (och potentiellt skada) närliggande normala celler.
I motsats till konventionell cancerterapi, ett team från University of Cincinnati har utvecklat flera nya konstruktioner för järnoxidbaserade nanopartiklar som detekterar, diagnostisera och förstöra cancerceller med hjälp av fototermisk terapi (PTT). PTT använder nanopartiklarna för att fokusera ljusinducerad värmeenergi endast inom tumören, skadar inga närliggande normala celler.
Resultaten av UC-arbetet kommer att presenteras på Materials Research Society Conference i Boston 30 november-dec. 5 av Andrew Dunn, doktorand i materialvetenskap vid UC:s Tekniska Högskola. Donglu Shi arbetar med Dunn i denna studie, professor i materialvetenskap vid UC:s högskola för teknik och tillämpad vetenskap; David Mast, docent i fysik vid UC:s McMicken College of Arts and Sciences; och Giovanni Pauletti, docent vid James L. Winkle College of Pharmacy.
UC-studien använde levande celler från möss för att framgångsrikt testa effektiviteten av deras tvåsidiga nanopartikeldesigner (en sida för cellinriktning och den andra för behandlingsleverans) i kombination med PTT. Dock, U.S. Food and Drug Administration har nu godkänt användningen av järnoxidnanopartiklar hos människor. Det betyder att den fototermiska effekten av järnoxidnanopartiklar kan visa, under nästa decennium, ett starkt löfte inom human cancerterapi, troligen med lokaliserade tumörer.
Hur nanopartiklarna fungerar med fototermisk terapi
Med denna teknik, en laserstråle med låg effekt riktas mot tumören där en liten mängd magnetiska järnoxidnanopartiklar finns närvarande, antingen genom att injicera partiklarna direkt i tumören eller injicera dem i blodomloppet varvid partiklarna hittar och binder till de onormala cancercellerna via cellspecifik målinriktning.
Tillräcklig värme genereras sedan lokalt av laserljuset, höjer tumörtemperaturen snabbt till över 43 grader Celsius, och därigenom bränna de onormala cancercellerna. Denna speciella PTT-behandling involverar ingen medicin, men genererar bara lokal värme i tumören, orsakar därför mycket mindre biverkningar än de traditionella kemo- eller strålbehandlingarna.
"Denna behandling är mycket mer idealisk eftersom den går direkt till cancercellen, " säger Shi. "Nanomaterialen kommer bara in i de onormala cellerna, belysa dessa celler och sedan göra vad du än har designat dem för att göra. I detta fall, det är att värma upp tillräckligt varmt för att bränna och döda cancercellerna, men inte skada de omgivande normala cellerna."
Shi tillade att läkare ofta är frustrerade över de nuvarande konventionella sätten för tidig avbildning av cancerceller genom medicinsk resonanstomografi eller datoriserad tomografi, eftersom tumörerna vanligtvis är i stadium tre eller fyra innan de kan upptäckas. Han uttalade, "Med nanomaterialteknik, vi kan upptäcka tumören tidigt och döda den samtidigt."
Cellinriktning
Varje tumör har ett motsvarande protein som är cancerspecifikt som kallas en tumörspecifik ligand eller en antikroppsantigenreaktion som endast har uttryck för den specifika cancern som bröst- eller prostatacancer.
Forskare identifierar denna speciella biomarkör som är specifik för en viss tumör, konjugerar sedan denna biomarkör på ytan av nanobäraren som bara har uttrycket för den specifika typen av cancercell.
Den riktar sig då bara mot den onormala cancercellen, inte normal, friska celler, och eftersom den är så liten kan den bryta membranet och komma in i den konjugerade cancercellen och frigöra PTT.
Nanoteknikbärarna går in i kroppen genom en ven i blodomloppet, söka de onormala cancercellerna, hitta biomarkören eller cancercellerna och fästa vid dessa celler och låsa upp deras fluorescerande partiklar så att de kan detekteras av ett fotonlaserljus.
Laserljuset värmer nanopartiklarna till minst 43 grader Celsius för att döda cancercellerna, i slutändan lämnar alla andra celler i kroppen oskadda.
Potentiell DIY-cancerbehandling
Proceduren kan slutligen utföras av patienten efter träning för att rikta en liten laserljusanordning till det drabbade området under en viss tid två till tre gånger om dagen. Denna metod kan i slutändan förbättra framgångsfrekvensen, samt minska kostnader för patienten. Detta ger "peka och skjuta" en helt ny innebörd.
Framtida forskning inom nanopartikel-PTT kommer att titta på toxicitet, problem med biologisk nedbrytbarhet och kompatibilitet. Shi sa att teamet för närvarande letar efter andra olika biologiskt nedbrytbara material att använda för bärarna som växtklorofyller som de i kål som är både ätbara och fototermiska. Detta material är biokompatibelt och biologiskt nedbrytbart och kan potentiellt stanna i tumörcellerna tills dess jobb är klart, löses sedan upp och leds ut genom matsmältningssystemet.