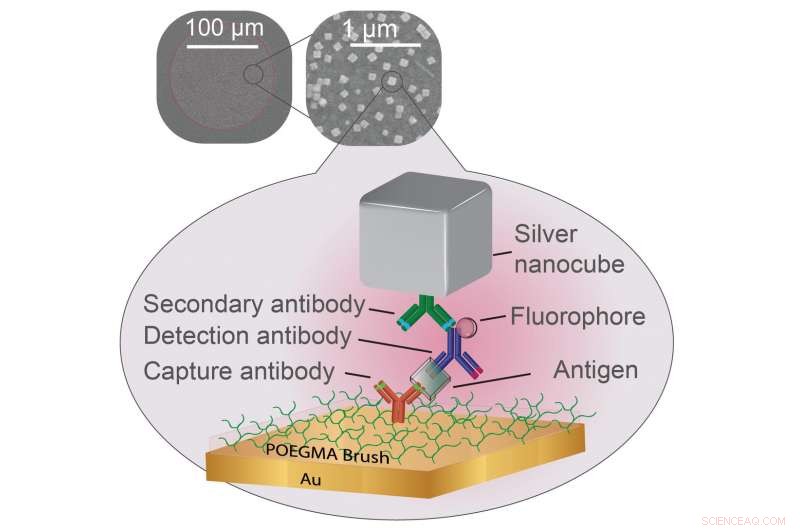
Forskare har visat att plasmonik kan förbättra de fluorescerande markörer som används för att signalera positiva prover i vissa typer av tester för sjukdomar. En polymerborstbeläggning håller oönskade biomolekyler borta medan en infångningsantikropp (röd) fångar biomarkörer för sjukdom (klar). En detektionsantikropp (blå) låser sig sedan på biomarkören och avger ljus från en fäst fluorofor (sfär). Allt detta är inklämt av ett tunt lager av guld och en silver nanokub som är fäst med en tredje antikropp (grön), skapa förutsättningar för fluoroforen att avge starkare ljus. Kredit:Daniela Cruz, Duke University
Ingenjörer vid Duke University har visat att silverkuber i nanostorlek kan göra diagnostiska tester som bygger på fluorescens lättare att läsa genom att göra dem mer än 150 gånger ljusare. Kombinerat med en framväxande diagnostisk plattform för vård som redan visats kunna upptäcka små spår av virus och andra biomarkörer, tillvägagångssättet skulle kunna göra det möjligt för sådana tester att bli mycket billigare och mer utbredda.
Resultaten dök upp online den 6 maj i tidskriften Nanobokstäver .
Plasmonik är ett vetenskapligt fält som fångar energi i en återkopplingsslinga som kallas en plasmon på ytan av silvernanokuber. När fluorescerande molekyler är inklämda mellan en av dessa nanokuber och en metallyta, interaktionen mellan deras elektromagnetiska fält gör att molekylerna avger ljus mycket kraftigare. Maiken Mikkelsen, James N. och Elizabeth H. Barton docent i elektro- och datateknik vid Duke, har arbetat med sitt laboratorium på Duke för att skapa nya typer av hyperspektrala kameror och supersnabba optiska signaler med plasmonik i nästan ett decennium.
På samma gång, forskare i laboratoriet för Ashutosh Chilkoti, Alan L. Kaganov framstående professor i biomedicinsk teknik, har arbetat på en fristående, punkt-av-vård diagnostiskt test som kan plocka ut spårmängder av specifika biomarkörer från biomedicinska vätskor som blod. Men eftersom testerna förlitar sig på fluorescerande markörer för att indikera närvaron av biomarkörerna, att se det svaga ljuset av ett knappt positivt test kräver dyr och skrymmande utrustning.
"Vår forskning har redan visat att plasmonik kan öka ljusstyrkan hos fluorescerande molekyler tiotusentals gånger om, ", sa Mikkelsen. "Att använda det för att förbättra diagnostiska analyser som begränsas av deras fluorescens var helt klart en mycket spännande idé."
"Det finns inte många exempel på människor som använder plasmonförstärkt fluorescens för point-of-care diagnostik, och de få som finns har ännu inte implementerats i klinisk praxis, " lade Daria Semeniak till, en doktorand i Chilkotis laboratorium. "Det har tagit oss ett par år, men vi tror att vi har utvecklat ett system som kan fungera."
I den nya tidningen, forskare från Chilkoti-labbet bygger sin superkänsliga diagnostiska plattform kallad D4 Assay på en tunn film av guld, den föredragna yin till nanokubens yang av plasmoniskt silver. Plattformen börjar med ett tunt lager av polymerborstbeläggning, vilket hindrar allt från att fastna på guldytan som forskarna inte vill fästa där. Forskarna använder sedan en bläckstråleskrivare för att fästa två grupper av molekyler skräddarsydda för att låsa fast den biomarkör som testet försöker upptäcka. Ett set fästs permanent på guldytan och fångar en del av biomarkören. Den andra tvättas bort från ytan när testet börjar, fäster sig vid en annan bit av biomarkören, och blinkar för att indikera att den har hittat sitt mål.
Efter flera minuter för att reaktionerna ska kunna inträffa, resten av provet tvättas bort, lämnar bara de molekyler bakom sig som har lyckats hitta sina biomarkörer, svävande som fluorescerande fyrar bundna till ett gyllene golv.

En forskare har en testversion av D4-analysen, som har visat sig kunna detektera spårmängder av sjukdomsbiomarkörer. Upphovsman:Michaela Kane, Duke University
"Den verkliga betydelsen av analysen är polymerborstens beläggning, ", sa Chilkoti. "Polymerborsten gör att vi kan lagra alla verktyg vi behöver på chipet samtidigt som vi behåller en enkel design."
Medan D4 -analysen är mycket bra på att fånga små spår av specifika biomarkörer, om det bara finns spårmängder, de fluorescerande beacons kan vara svåra att se. Utmaningen för Mikkelsen och hennes kollegor var att placera sina plasmoniska silver -nanokuber ovanför fyrarna på ett sådant sätt att de överladdade fyrarnas fluorescens.
Men som vanligt, detta var lättare sagt än gjort.
"Avståndet mellan silvernanokuberna och guldfilmen bestämmer hur mycket ljusare fluorescerande molekylen blir, sa Daniela Cruz, en doktorand som arbetar i Mikkelsens laboratorium. "Vår utmaning var att göra polymerborstbeläggningen tillräckligt tjock för att fånga biomarkörerna - och bara biomarkörerna av intresse - men tillräckligt tunna för att fortfarande förbättra diagnosljusen."
Forskarna försökte två metoder för att lösa denna Goldilocks-gåta. De lade först till ett elektrostatiskt lager som binder till detektormolekylerna som bär de fluorescerande proteinerna, skapa ett slags "andra våningen" som silver -nanokuberna kunde sitta ovanpå. De försökte också att funktionalisera nanokuberna i silver så att de skulle hålla sig direkt till individuella detektormolekyler på en-mot-en-basis.
Medan båda tillvägagångssätten lyckades öka mängden ljus som kom från beacons, den förra visade den bästa förbättringen, öka dess fluorescens med mer än 150 gånger. Dock, denna metod kräver också ett extra steg för att skapa en "andra våning, "vilket lägger till ytterligare ett hinder för att konstruera ett sätt att få detta att fungera på en kommersiell diagnostisk punkt för vård snarare än bara i ett laboratorium. Och medan fluorescensen inte förbättrades så mycket i det andra tillvägagångssättet, testets noggrannhet gjorde.
"Att bygga mikrofluidiska lab-on-a-chip-enheter genom båda metoderna skulle ta tid och resurser, men de är båda genomförbara i teorin, sa Cassio Fontes, en doktorand i Chilkoti-laboratoriet. "Det är vad D4 -analysen går mot."
Och projektet går framåt. Tidigare under året, forskarna använde preliminära resultat från denna forskning för att säkra ett femårigt, $3,4 miljoner R01 forskningspris från National Heart, Lunga, och Blodinstitutet. Medarbetarna kommer att arbeta med att optimera dessa fluorescensförbättringar samtidigt som de integrerar brunnar, mikrofluidkanaler och andra lågkostnadslösningar till en enstegsdiagnosenhet som kan köra igenom alla dessa steg automatiskt och läsas av en vanlig smartphonekamera i en lågkostnadsenhet.
"En av de stora utmaningarna i point-of-care tester är förmågan att läsa ut resultat, som vanligtvis kräver mycket dyra detektorer, ", sade Mikkelsen. "Det är en stor vägspärr för att ha engångstester för att låta patienter övervaka kroniska sjukdomar hemma eller för användning i låga resurser. Vi ser den här tekniken inte bara som ett sätt att komma runt den flaskhalsen, men också som ett sätt att öka noggrannheten och tröskeln för dessa diagnostiska enheter. "