Dr. Petr Cígler och hans medarbetare arbetar med att förfina molekylära system för att transportera ribonukleinsyra (RNA) molekyler in i celler. Frågan om hur man effektivt levererar RNA till en anvisad plats i kroppen för att tysta en felaktig gen är en av de största utmaningarna inom det snabbt växande området genmedicin.
Nu har forskare från Institutet för organisk kemi och biokemi vid Tjeckiska vetenskapsakademin (IOCB Prag) tagit ännu ett viktigt steg mot att uppnå detta mål. De har i detalj beskrivit framställningen av ett nytt sammansatt vektornanomaterial för transport av RNA, där de främst fokuserade på att säkerställa dess icke-toxicitet för celler. Anledningen är att skadligheten hos hittills kända nukleinsyravektorer utgör ett allvarligt hinder för utbyggnaden av genterapi.
En artikel om ämnet har publicerats i Advanced Functional Materials .
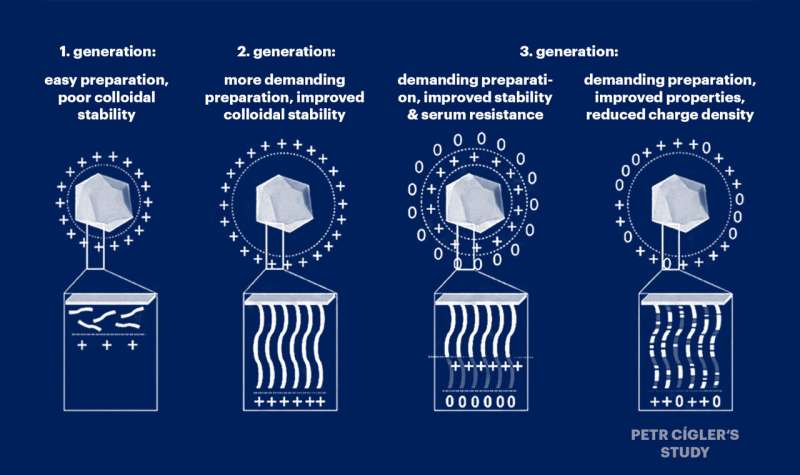
Petr Cígler och hans kollegor arbetade med antagandet att toxiciteten hos nukleinsyravektorer orsakas av en överdriven ackumulering av positiva laddningar längs kedjorna av bärarpolymerer som binder nukleinsyror. Därför spädde de systematiskt ut denna positiva laddning med oladdade monomerer och fann att dess lätta utspädning inte försämrade systemets förmåga att transportera nukleinsyror.
I sin grundliga studie beskriver de också under vilka omständigheter nya material kan förberedas för användning inom genmedicin. Forskarna ägnade stor uppmärksamhet åt de förhållanden under vilka dessa substanser binder nukleinsyror mest effektivt och i vilken stökiometrisk proportion.
Celler kan reglera översättningen av gener från mRNA till proteiner på flera sätt. En av dem är att tysta en gen med hjälp av en siRNA-molekyl (small interfering RNA). Detta blockerar produktionen av målproteinet, vilket är särskilt användbart om genen som kodar är muterad eller på annat sätt defekt. Dessutom är det möjligt att ingripa om översättningsregleringens medfödda mekanismer försämras. I ett sådant fall produceras för mycket av ett protein i kroppen, vilket är skadligt för dess hälsa.
"Genterapi är inte bara mycket effektiv, utan också akut målinriktad. Dess största fördel ligger i det faktum att den exakt riktar in sig på individuella mutationer eller störningar utan risk att missa målet. Med siRNA är det möjligt att träffa även en enda muterad ' bokstaven i en gen", säger Marek Kindermann, studiens första författare, och listar de viktigaste fördelarna med genterapi. För närvarande är fem läkemedel baserade på siRNA godkända för användning över hela världen, och det finns ungefär ett dussin fler på "väntelistan."
Den terapeutiska användningen av siRNA hindras av det faktum att siRNA-molekyler är instabila och därför bryts ner mycket snabbt i kroppen. Experter runt om i världen tar därför upp problemet med hur man levererar siRNA till en angiven plats och låter den göra sitt jobb, vilket är att stoppa eller begränsa produktionen av ett visst oönskat protein genom att tysta genen för det.
Denna uppgift togs också upp av Petr Cíglers team vid IOCB Prag, tillsammans med kollegor från Institutet för mikrobiologi vid den tjeckiska vetenskapsakademin, ledd av chefen för nanomedicingruppen, Dr. Veronika Benson.
"Varje transportsystem är utformat för att uppfylla två grundläggande mål:För det första har det till uppgift att skydda molekylen från att sönderfalla, och för det andra måste det säkerställa dess transport in i cellen så att den når cytosolen och fullgör sitt uppdrag som en drog där", förklarar Petr Cígler.
"I vår studie behandlar vi transportsystemets egenskaper i stor detalj. Vi går ner hela vägen ner till nivån av strukturella detaljer hos molekyler som interagerar med nukleinsyror. Vi beskriver de villkor som krävs för att siRNA ska kunna binda till transportera nanosystemet och sedan nå det intracellulära utrymmet."
Forskare från IOCB Prag banar därmed vägen för användningen av partiklar som kallas icke-virala vektorer, som inte använder virus för att bära RNA. De har placerat hela transportsystemet, inklusive nukleinsyran, på ytan av diamantnanopartiklar. Dessa är markant stabila bärarpartiklar, som också avger en speciell typ av fluorescens. Detta gör det möjligt att spåra deras resa genom vävnader och övervaka hur de beter sig inuti celler.
En komplikation är att det är svårt för kroppen att bli av med nanodiamanter, så denna genterapimetod lämpar sig främst för behandling av svårläkta ytliga sår. Det är för dessa typer av terapi, med fokus på att läka bensår hos patienter med diabetes, som de nya transportnanomaterialen, som presenteras i detta och andra verk av teamet av Dr. Cígler och medarbetare, är avsedda.
Deras senaste djupstudie möjliggjordes också tack vare AMULET-projektet, som fokuserar på utvecklingen av nanomaterial i flera skala och samlar åtta partners under ledning av Jaroslav Heyrovský Institute of Physical Chemistry.
Mer information: Marek Kindermann et al, Design Rules for the Nano-Bio Interface of Nanodiamonds:Impplications for siRNA Vectorization, Advanced Functional Materials (2024). DOI:10.1002/adfm.202314088
Journalinformation: Avancerat funktionsmaterial
Tillhandahålls av Institute of Organic Chemistry and Biochemistry i CAS