Flera typer av konventionella cancerterapier, såsom strålbehandling eller kemoterapi, förstör friska celler tillsammans med cancerceller. I avancerade stadier av cancer kan vävnadsförlust från behandlingar vara betydande och till och med dödlig. Banbrytande cancerterapier som använder nanopartiklar kan specifikt rikta sig mot cancerceller och skona frisk vävnad.
Nyligen genomförda studier har visat att växtbaserade nanopartiklar (pdNP) som har terapeutiska effekter kan vara ett effektivt alternativ till traditionella cancerbehandlingar. Emellertid har inga pdNPs godkänts som terapeutiska medel mot cancer hittills.
Riskli är en biprodukt som genereras under risraffineringsprocessen som har begränsad användbarhet och lågt kommersiellt värde. Den innehåller dock flera föreningar med anticanceregenskaper, såsom γ-oryzanol och γ-tokotrienol.
För att utforska dessa terapeutiska egenskaper hos riskli utvecklade ett team av forskare under ledning av professor Makiya Nishikawa från Tokyo University of Science (TUS) i Japan nanopartiklar från riskli och testade deras effektivitet i mössmodeller. Deras studie, publicerad i Journal of Nanobiotechnology den 16 mars 2024, var medförfattare av Dr Daisuke Sasaki, Hinako Suzuki, docent Kosuke Kusamori och biträdande professor Shoko Itakura från TUS.
"Under de senaste åren har ett ökande antal nya läkemedelsmodaliteter utvecklats. Samtidigt har utvecklingskostnader förknippade med nya terapier ökat dramatiskt, vilket bidrar till bördan av medicinska utgifter. För att lösa detta problem använde vi riskli, ett industriavfall med anticanceregenskaper för att utveckla nanopartiklar", förklarar prof. Nishikawa.
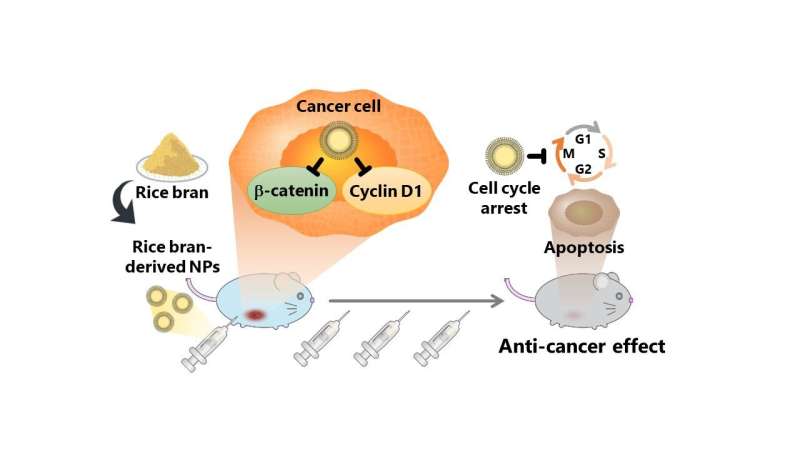
Studien utvärderade anticancereffekterna av nanopartiklar som härrör från riskli (rbNP), som erhölls genom att bearbeta och rena en suspension av Koshihikari riskli i vatten. När en cancercellinje vid namn colon26 behandlades med rbNPs, stoppades celldelningen och programmerad celldöd inducerades, vilket tyder på starka anticancereffekter av nanopartiklarna. Den observerade anticanceraktiviteten hos rbNP kan tillskrivas γ-tokotrienol och γ-oryzanol, som lätt tas upp av cancerceller vilket resulterar i cellcykelstopp och programmerad celldöd.
Dessutom minskade rbNPs uttrycket av proteiner, såsom β-catenin (ett protein associerat med Wnt-signalväg involverad i cellproliferation) och cyklin D1, som är kända för att främja cancerrecidiv och metastaser. Dessutom minskade rbNP:erna uttrycket av β-catenin endast i colon26-celler utan att påverka de icke-cancerceller.
"En viktig fråga i samband med pdNPs är deras låga farmakologiska aktivitet jämfört med farmaceutiska läkemedel. Emellertid uppvisade rbNPs högre anticanceraktivitet än DOXIL, en liposomal farmaceutisk formulering av doxorubicin. Dessutom är doxorubicin cytotoxiskt för både cancerceller och icke-cancerceller , medan rbNP är specifikt cytotoxiska för cancerceller, vilket tyder på att rbNP är säkrare än doxorubicin", säger professor Nishikawa.
För att bekräfta anticanceregenskaperna hos rbNPs i den levande kroppen injicerade forskarna rbNPs i möss med aggressivt adenokarcinom i deras bukhåla (omsluten av diafragman, bukmusklerna och bäckenet och inrymmer organ som tarmar, lever och njurar). De observerade betydande undertryckande av tumörtillväxt utan negativa effekter på mössen. Dessutom hämmade rbNP:erna signifikant metastatisk tillväxt av murina melanom B16-BL6-celler i en lungmetastasmusmodell.
Riskli har flera egenskaper som gör det till en utmärkt källa till terapeutiska pdNPs. För det första är det ekonomiskt jämfört med många andra källor till pdNP. Nästan 40 % av risklidet kasseras i Japan, vilket ger en lättillgänglig råvara. För det andra är beredningseffektiviteten för rbNPs högre än den för tidigare rapporterade pdNPs.
Förutom att vara praktiskt och säkert som ett anticancerläkemedel, är de fysikalisk-kemiska egenskaperna hos rbNP mycket stabila. Emellertid måste några parametrar, såsom etablering av separationsteknologier på läkemedelsnivå, bedömning av produktionsprocesskontrollparametrar och utvärdering av effektivitet och säkerhet i humana cancercellinjer och xenograft-djurmodeller, undersökas innan kliniska prövningar på människor.
Sammanfattningsvis är riskli, en avfallsprodukt från jordbruket, en källa till terapeutiska pdNP:er som är prisvärda, effektiva och säkra och har potential att revolutionera cancerbehandling i framtiden.
"Genom att etablera en tillverkningsmetod för nanopartiklar av riskli med stabil kvalitet och bekräfta deras säkerhet och effektivitet kan vi utveckla läkemedel för cancerbehandling som är hållbara, miljövänliga och prisvärda. Följaktligen kan vi kanske hjälpa fler cancerpatienter att behålla god fysisk och mental hälsa efter behandling", avslutar Prof. Nishikawa.
Mer information: Daisuke Sasaki et al, Utveckling av nanopartiklar härrörande från riskli med utmärkt anti-canceraktivitet och deras tillämpning för peritoneal spridning, Journal of Nanobiotechnology (2024). DOI:10.1186/s12951-024-02381-z
Tillhandahålls av Tokyo University of Science