Översikt över den aktuella forskningen Kredit:Kanazawa University
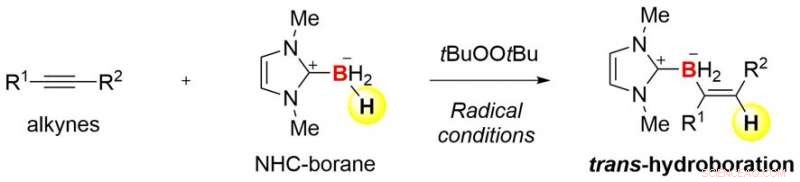
En kombination av organoboron och radikalkemi genererar ovanlig transselektivitet vid hydroborering av alkyner. Användningen av N-heterocykliska karbenboraner är nyckeln till framgången för denna kemiska transformation. Denna studie förväntas öppna dörren till utvecklingen av nya borinnehållande material.
Organoboronföreningar har använts i stor utsträckning för att skapa nya organiska molekyler sedan Prof. Suzuki, 2010 års nobelpristagare i kemi, utvecklat palladiumkatalyserade korskopplingsreaktioner med organoboronföreningar (Suzuki-koppling). Dessutom, många borinnehållande föreningar är själva lovande material. De kan användas som läkemedel och organiska elektroluminescensmaterial på grund av bors unika elektroniska natur.
Boran (BH3) och dess derivat stabiliserade av ligander är de enklaste borföreningarna. De kan reagera med en kol-kol trippelbindning (alkyn, C-C) för att ge en insättningsprodukt (H-C=C-BH 2 ). Denna reaktion, kallas hydroborering, är en kraftfull metod för att framställa organoboronföreningar. Dock, reaktionen ger vanligtvis bara en cis-produkt, vilket betyder att H och BH 2 införs på samma sida av trippelbindningen. Det är, det är svårt att syntetisera en transhydroborationsprodukt med den motsatta geometriska konfigurationen. Tidigare, det har funnits mycket begränsade exempel på transhydroborering av alkyner.
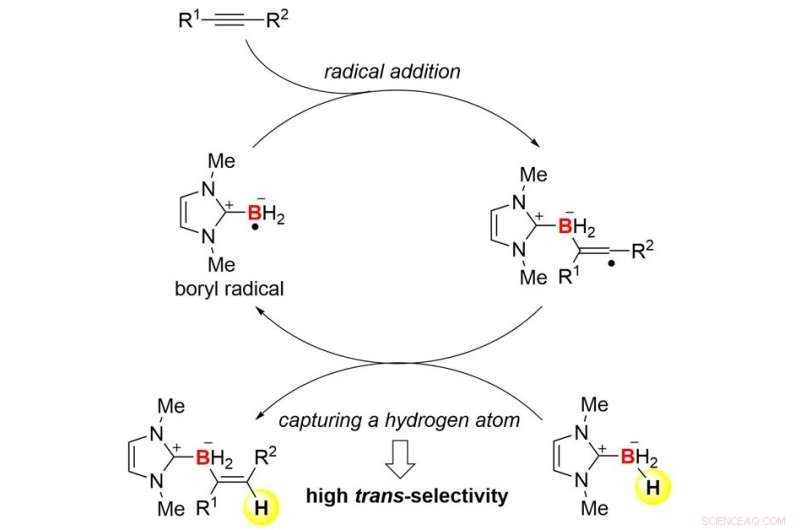
Översikt över reaktionsmekanismen. Upphovsman:Kanazawa University
Samarbetsteamet mellan Kanazawa University och University of Pittsburgh lyckades utveckla trans-hydroboreringsreaktioner av alkyner baserade på radikal kemi (Figur 1). Teamet använde N-heterocykliska karbenboraner (NHC-boraner) för att kombinera hydroborering med radikal kemi. NHC-boraner kan hanteras lätt på grund av deras stabilitet, och de är bra föregångare till borylradikaler (borcentrerade radikaler). Verkligen, en NHC-borylradikal kan lätt bildas genom enkel termolys i närvaro av billig kommersiell di-tert-butylperoxid. Radikalen kan adderas till en alkyn för att bilda en kol-bor (C-B) bindning och en ny kolradikal (Figur 2). Transselektivitet vid hydroborering induceras kinetiskt när den mycket reaktiva kolradikalen fångar en väteatom från utgångs-NHC-boranen. Som ett resultat, den övergripande processen etablerar en radikal kedjecykel. Denna mekanism skiljer sig ganska mycket från den för kända hydroborationsreaktioner.
Från lättillgängliga alkyner, föreliggande protokoll tillhandahåller olika bänkstabila alkenylboranföreningar som inte är lättillgängliga med kända metoder. Några av dem kan omvandlas till retinoidmimiker, som är drogkandidater, genom modifierad Suzuki-koppling (Figur 3).
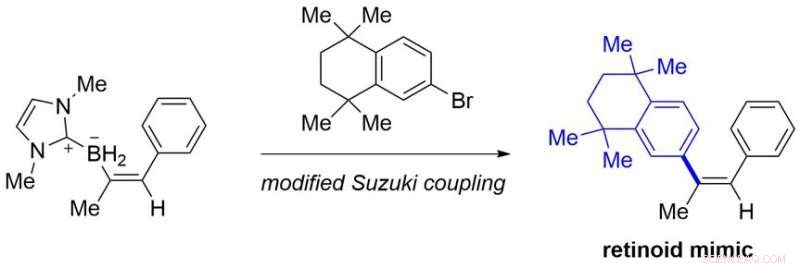
Appliceringen av en syntetiserad produkt. Upphovsman:Kanazawa University
Organoborföreningar syntetiserade med föreliggande metod kommer att ge tillgång till nya borinnehållande π-system genom ytterligare kemisk omvandling. Därför, denna typ av trans-hydroboreringsreaktion kommer att underlätta framsteg inom medicinsk kemi och materialvetenskap. Ur ren kemisynpunkt, denna studie utökar potentialen för radikaler i syntetisk kemi. Kortfattat, vi illustrerar att radikaler är kapabla att kontrollera kemiska reaktioner exakt trots sin extrema reaktivitet.
Dennis Curran (University of Pittsburgh), en medarbetare i denna studie, säger, "Det har varit ett nöje att få vara delaktig i detta samarbete, som leddes av Kanazawa-teamet. Den nya reaktionen som vi har upptäckt är unik, och jag är exalterad över möjligheterna att förlänga det i både grundforskning och praktiska tillämpningar. "