Det stora komplexet av genredigerande molekyler är svårt att leverera till celler från externa en externa applikationer. Biologiskt nedbrytbara lipidnanopartiklar levererar mRNA som kodar för de genredigerande molekylerna in i cellen. Kredit:Från animation av Visual Science och Skoltech, visual-science.com/crispr
Ett forskningssamarbete mellan Tufts University och den kinesiska vetenskapsakademin har lett till utvecklingen av en avsevärt förbättrad leveransmekanism för genredigeringsmetoden CRISPR/Cas9 i levern, enligt en studie som nyligen publicerades i tidskriften Avancerade material . Leveransen använder biologiskt nedbrytbara syntetiska lipidnanopartiklar som bär de molekylära redigeringsverktygen in i cellen för att exakt ändra cellernas genetiska kod med så mycket som 90 procents effektivitet. Nanopartiklarna representerar ett av de mest effektiva CRISPR/Cas9 leveransverktygen som rapporterats hittills, enligt forskarna, och skulle kunna hjälpa till att övervinna tekniska hinder för att möjliggöra genredigering i ett brett spektrum av kliniska terapeutiska tillämpningar.
CRISPR/Cas9-genredigeringssystemet har blivit ett kraftfullt forskningsverktyg som avslöjar funktionen hos hundratals gener och utforskas för närvarande som ett terapeutiskt verktyg för behandling av olika sjukdomar. Dock, Vissa tekniska hinder återstår innan det kan vara praktiskt för kliniska tillämpningar. CRISPR/Cas9 är ett stort molekylärt komplex, som innehåller både ett nukleas (Cas9) som kan skära igenom båda strängarna i en målinriktad genomisk sekvens, och ett konstruerat "single-guide" RNA (sgRNA) som skannar genomet för att hjälpa nukleaset att hitta den specifika sekvensen som ska redigeras. Eftersom det är ett stort molekylärt komplex, det är svårt att leverera CRISPR/Cas9 direkt in i cellens kärna, där den kan göra sitt arbete. Andra har packat redigeringsmolekylerna i virus, polymerer, och olika typer av nanopartiklar för att få in dem i kärnan, men den låga effektiviteten av överföring har begränsat deras användning och styrka för kliniska tillämpningar.
Lipidnanopartiklarna som beskrivs i studien kapslar in budbärar-RNA (mRNA) som kodar för Cas9. När innehållet i nanopartiklarna – inklusive sgRNA – släpps in i cellen. Cellens proteintillverkningsmaskineri tar över och skapar Cas9 från mRNA-mallen, slutföra genredigeringssatsen. En unik egenskap hos nanopartiklarna är gjorda av syntetiska lipider som består av disulfidbindningar i fettkedjan. När partiklarna kommer in i cellen, miljön i cellen bryter upp disulfidbindningen för att demontera nanopartiklarna och innehållet släpps snabbt och effektivt ut i cellen.
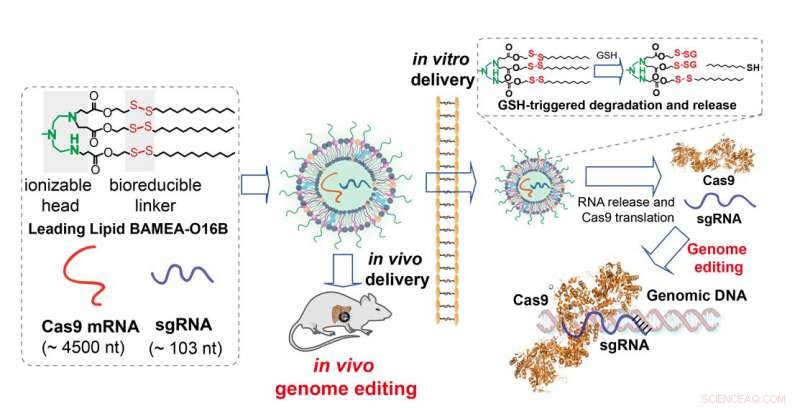
Lipider formulerade med en bioreducerbar linker bildar väggen av nanopartiklar som inkapslar mRNA från Cas9 plus sgRNA. När du går in i cellen, in vitro eller in vivo, länkarna bryts och partiklarna sönderfaller för leverans av innehåll och översättning av mRNA till aktivt enzym för CRISPR/Cas9-genomredigering. Kredit:Qiaobing Xu, Tufts universitet
"Vi har precis börjat se mänskliga kliniska prövningar för CRISPR-terapier, sa Qiaobing Xu, medmotsvarande författare till studien och docent i biomedicinsk teknik vid Tufts University. "Det finns många sjukdomar som länge har varit svårbehandlade för vilka CRISPR-terapier skulle kunna erbjuda nytt hopp - till exempel sicklecellssjukdom, Duchennes muskeldystrofi, Huntingtons sjukdom, och till och med många cancerformer. Vår förhoppning är att detta framsteg kommer att ta oss ytterligare ett steg mot att göra CRISPR till ett effektivt och praktiskt tillvägagångssätt för behandling."
Forskarna tillämpade den nya metoden på möss, försöker minska närvaron av en gen som kodar för PCSK9, vars förlust är förknippad med lägre LDL-kolesterol, och minskad risk för hjärt-kärlsjukdom. "Lipidnanopartiklarna är en av de mest effektiva CRISPR/Cas9-bärarna vi har sett, sa Ming Wang, också motsvarande författare till studien och professor vid den kinesiska vetenskapsakademin, Beijing National Laboratory for Molecular Science. "Vi kan faktiskt slå ner PCSK9-uttrycket hos möss med 80 procent effektivitet i levern, föreslår ett verkligt löfte för terapeutiska tillämpningar."