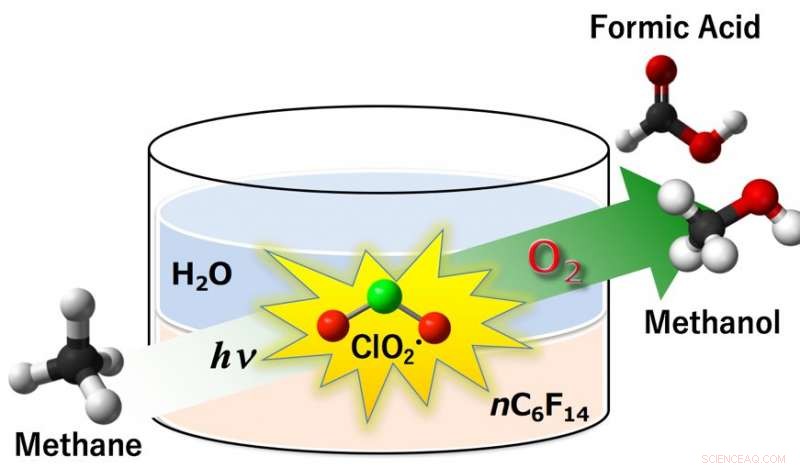
Fig 1:Klordioxidradikal (ClO2 •) befanns fungera som ett effektivt oxidationsmedel vid aerob syresättning av metan till metanol och myrsyra under fotobestrålning. Utbytena av metanol och myrsyra var 14% och 85%, respektive, med en metanomvandling på 99% under omgivande förhållanden (298 K, 1 atm) i ett tvåfassystem innefattande perfluorohexan och vatten. Upphovsman:Osaka University
Fria radikaler får inte den bästa pressen. Dock, medan de är kända som skadliga oxidanter i kroppen, dessa ultrareaktiva kemikalier är oumbärliga i laboratoriet. Radikala reaktioner spelar en roll i nyckelteknologi som avlägsnande av föroreningar och splittring av vatten.
Nu, forskare vid Osaka University har använt radikaler för att omvandla en växthusgas, metan, till användbara kemikalier. Drivs av ljus, denna miljövänliga process uppnår ett mål som förblev svårfångat i årtionden.
Metan (CH4) är relaterat till metanol och myrsyra, som behövs i stora mängder av den kemiska industrin. Bakterier kan oxidera CH4 till metanol nästan utan problem med hjälp av naturliga enzymer. Samma förvandling i labbet, dock, kräver kemiskt hög temperatur, högt tryck och dyra reagenser för att klyva de extremt starka C — H -bindningarna. Som rapporterats nyligen, den nya processen använder kraftfulla kloradikaler för att aktivera dessa bindningar. Detta gör att reaktionen kan ske vid rumstemperatur, under lampan, med enkelt syre som oxidationsmedel.
Fria radikaler är kemikalier med oparade elektroner - deras skenande reaktivitet kommer från det akuta behovet av de ensamma elektronerna för att hitta partners i en annan molekyl. I Osaka -processen, kloritdioxid (ClO2 •) aktiveras under fotostrålningen för att ge kloradikaler (Cl •) och singlet -syre. Den mycket reaktiva radikalen, Cl •, abstraherar sedan en väteatom av CH4 för att ge metylradikaler, CH3 •, som i sin tur reagerar med syre för att producera värdefull metanol och myrsyra. Denna tydligen enkla process, dock, förlitar sig på en subtil design twist.
"Metanaktivering av radikala arter har testats tidigare, "studera en huvudförfattare Prof. Kei Ohkubo säger." Men CH3 • mellanprodukter tenderar att reagera med det kolväteorganiska lösningsmedlet vilket ger deaktivering av reaktiva radikala mellanprodukter. Detta förekommer inte i vatten, men tyvärr löser sig metan knappt i vatten. "Forskarna hittade ett snyggt sätt kring detta:två lösningsmedel i ett enda system, en för varje steg i processen. Den första ClO2 • bildningen sker i en vattenfas, där natriumklorit är lösligt. Sedan, ClO2 • överförs till en perfluorohexan (PFH) fas, där metan och O2 löser sig för att reagera med dem.
"PFH är idealiskt för det andra steget:det löser metan, men reagerar inte med CH3 • radikaler, "förklarar Ohkubo." Detta skapar ett utrymme för oxidation av CH3 •, att ge önskade produkter. Sedan, efter att metanol och myrsyra bildats, de korsar lösningsmedelsgränsen i motsatt riktning, in i vattenfasen. Här skyddas de mot ytterligare oxidation till oönskade CO eller CO2 som växthusgaser. "
Hela processen är imponerande effektiv, omvandla över 99% av metan till målprodukterna, utan behov av hög temperatur eller tryck.
"Detta är den första framgångsrika användningen av syre i luften för att oxidera metan under omgivande förhållanden, "Säger Ohkubo." Energikrävande metoder för kemisk produktion måste fasas ut-vi behöver snabbt smarta lösningar för att bearbeta råvaror i en skonsam, miljövänligt sätt. Vår studie visar hur detta kan göras för metan. Det tvåfasiga lösningsmedelskonceptet, där instabila mellanprodukter skyddas av ett lösningsmedel som PFH, kan eventuellt utökas i hela branschen. "