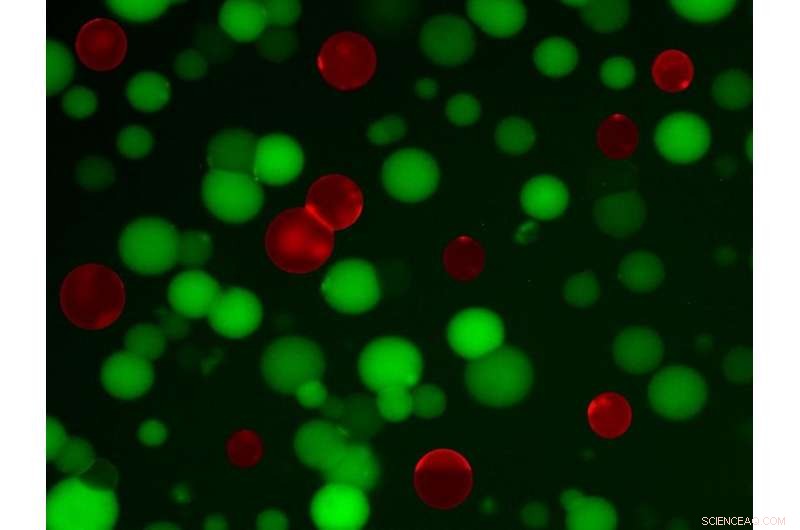
Biomedicinska ingenjörer vid UC Davis har skapat som efterliknar några av egenskaperna hos levande celler. De konstgjorda cellerna växer inte och delar sig, men kunde upptäcka, reagera på och förstöra bakterier i en labbskål. Kredit:Cheemeng Tan, UC Davis
"Legoblock" konstgjorda celler som kan döda bakterier har skapats av forskare vid University of California, Davis Institutionen för biomedicinsk teknik. Arbetet rapporteras 29 augusti i tidskriften ACS tillämpade material och gränssnitt .
"Vi konstruerade konstgjorda celler nerifrån och upp – som legoklossar – för att förstöra bakterier, " sa assisterande professor Cheemeng Tan, som ledde arbetet. Cellerna är byggda av liposomer, eller bubblor med ett cellliknande lipidmembran, och renade cellulära komponenter inklusive proteiner, DNA och metaboliter.
"Vi visade att konstgjorda celler kan känna av, reagerar och interagerar med bakterier, samt fungera som system som både upptäcker och dödar bakterier med litet beroende av sin miljö, " sa Tan.
Teamets konstgjorda celler efterliknar de väsentliga egenskaperna hos levande celler, men är kortlivade och kan inte dela sig för att reproducera sig själva. Cellerna designades för att svara på en unik kemisk signatur på E. coli-bakterier. De kunde upptäcka, attackera och förstöra bakterierna i laboratorieförsök.
Konstgjorda celler hade tidigare bara varit framgångsrika i näringsrika miljöer, sa Tan. Dock, genom att optimera de konstgjorda cellernas membran, cytosol och genetiska kretsar, teamet fick dem att arbeta i en mängd olika miljöer med mycket begränsade resurser som vatten, betonar deras robusthet i mindre än idealiska eller föränderliga förhållanden. Dessa förbättringar breddar avsevärt den övergripande potentiella tillämpningen av artificiella celler.
Antibakteriella konstgjorda celler kan en dag infunderas i patienter för att hantera infektioner som är resistenta mot andra behandlingar. De kan också användas för att leverera droger på den specifika plats och tid, eller som biosensorer.
Medförfattare på tidningen är Yunfeng Ding, Eliza Morris, Luis Contreras-Llano och Michelle Mao. Arbetet stöddes av NSF, ett Branco-Weiss Fellowship till Tan och av ett UC MEXUS-CONACYT Doctoral Fellowship till Contreras-Llano.