Det var avgörande för denna studie att designa platsspecifika enatomskatalysatorer, eftersom denna enatomstruktur direkt efterliknar strukturen hos enzymer (gjorda av enstaka metallatomer och omgivande proteiner). Kredit:Cube3D Grafik / Designer:Younghee Lee
Tänk om det inte fanns några tunnlar i de schweiziska alperna? Den som försöker resa genom dem skulle behöva gå upp och ner för kullar och sicksacka runt fälten. Mycket mer energi och tid sparas genom att passera en tunnel än att bestiga ett berg. Detta liknar hur katalysatorer fungerar:de påskyndar kemiska reaktioner genom att sänka energin som krävs för att nå önskat fysiskt tillstånd.
I industriella tillverkningsprocesser, heterogen katalys, som vanligtvis involverar användningen av fasta katalysatorer placerade i en vätske- eller gasreaktionsblandning, har många potentiella tillämpningar. Att vara i en annan fas, heterogena katalysatorer kan lätt separeras från en reaktionsblandning. På det här sättet, katalysatorerna kan effektivt återvinnas och återvinnas, vara ganska miljövänlig. Dessutom, de uppvisar mycket stabil aktivitet även under hårda reaktionsbetingelser. Trots sådana fördelar, heterogen katalys har ansetts möjliggöra mindre interaktion och kontrollerbarhet än homogen katalys på grund av en dålig förståelse av dess reaktionsprocess.
Forskare vid Center for Nanopartikelforskning (ledd av direktör Taeghwan Hyeon) inom Institute for Basic Science (IBS) i samarbete med professor Ki Tae Nam vid Seoul National University och professor Hyungjun Kim vid KAIST visade för första gången enzymliknande heterogen katalys . De utvecklade en mycket aktiv heterogen TiO 2 fotokatalysator inkorporerad med många enkla kopparatomer. De använde denna katalysator för fotokatalytisk väteproduktion, och fann att katalysatorn är lika aktiv som den mest aktiva och dyrbara Pt-TiO 2 katalysator.
Forskarna var engagerade i att modellera katalysatorstrukturen på ett liknande sätt som de mest effektiva och reaktiva katalysatorerna som är biologiska enzymer. Enzymer består av katalytiskt aktiva metallatomer och omgivande proteiner som arbetar mycket nära för att hålla sina återkopplingar rörliga fram och tillbaka. Tack vare denna samarbetsvilliga interna kommunikation, enzymer kan snabbt anpassa sin struktur så att den passar optimalt för önskade reaktioner (allmänt känd som induced-fit-modellen). Under anpassningen, enzymer återgår intermittent till sina ursprungliga former och omvandlas. Professor Hyeon säger, "För första gången, vi fann att en enzymliknande reversibel och kooperativ aktiveringsprocess inträffar även i heterogena katalysatorer. Detta är en aldrig tidigare skådad plattform som kombinerar fördelarna med både heterogena katalysatorer och biologiska enzymer. Samtidigt som de har den robusta stabiliteten hos heterogena katalysatorer, samverkande och reversibla egenskaper hos enzymer ger betydande kontrollerbarhet, vilket i slutändan ger hög aktivitet för produktion av väte (det mest effektiva och ideala bränslet) från fotokatalytiska vattenspjälkningsreaktioner."
Biologiska enzymer har ansetts vara en central modell för att utveckla artificiella katalysatorer. De har framgångsrikt använts för att utforma homogena katalysatorer för olika reaktioner. Fortfarande, det hade inte funnits någon rapport om industriellt viktiga heterogena katalysatorer med dessa enzymliknande egenskaper på grund av bristen på atomär förståelse för heterogena katalysatorer. Denna nya studie visar att heterogena katalysatorer kan fungera som enzymer, bekräftar den grundläggande principen att samverkan mellan atomkatalysatorer och närliggande miljöer har betydande inflytande på övergripande materialegenskaper och katalytisk aktivitet.
Kombinera teoretiska simuleringar och nanomaterialsyntesteknologier, forskarna syntetiserade en enzymliknande heterogen katalysator. (Fig. 2) De täckte en rundformad TiO 2 substrat med enatomig koppar. De lindade TiO 2 och kopparatomer tillsammans. Efterföljande bakning stabiliserade framgångsrikt enkla kopparatomer uteslutande på titanplatser. Det var avgörande för denna studie att designa platsspecifika enatomskatalysatorer, eftersom denna enkelatomstruktur direkt efterliknar strukturen hos enzymer (gjorda av enatoms metalljoner och omgivande proteiner).
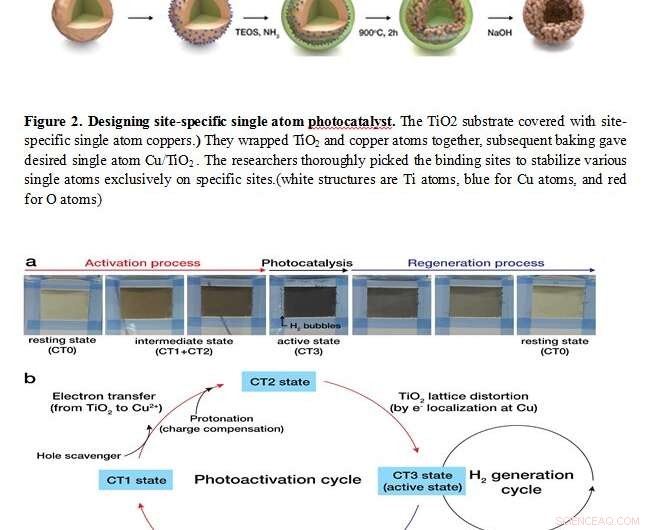
Kredit:IBS
Intressant, den syntetiserade platsspecifika enkelatomen Cu/TiO 2 katalysatorer genomgick en unik fotoaktiveringsprocess. Genom att absorbera ljus, TiO 2 exciterar en elektron. Den exciterade elektronen överförs till en enda kopparatom genom en enkel förändring av oxidationstillståndet. Överföringen av en elektron ändras i sin tur tillbaka kring TiO 2 strukturer (precis som induced-fit-modellen av ett enzym). Detta aktiva tillstånd återgår sedan till det initiala vilotillståndet när en elektron överförs tillbaka till TiO 2 från en metallatom. Faktiskt, denna interaktiva och reversibla mekanism bekräftades med den vita Cu/TiO 2 blir snabbt svart under ljus bestrålning, och tillbaka till sin ursprungliga vita färg när den rensas med luft. Tack vare dessa enzymatiska egenskaper, enkelatom Cu/TiO 2 katalysator förvandlade 40% av ljusenergin till H 2 , en exceptionellt hög katalytisk aktivitet, som är lika aktiv som den mest aktiva och dyraste Pt-TiO 2 fotokatalysator. Väte är känt för att vara det mest effektiva och idealiska bränslet eftersom det genererar vatten som den enda biprodukten.