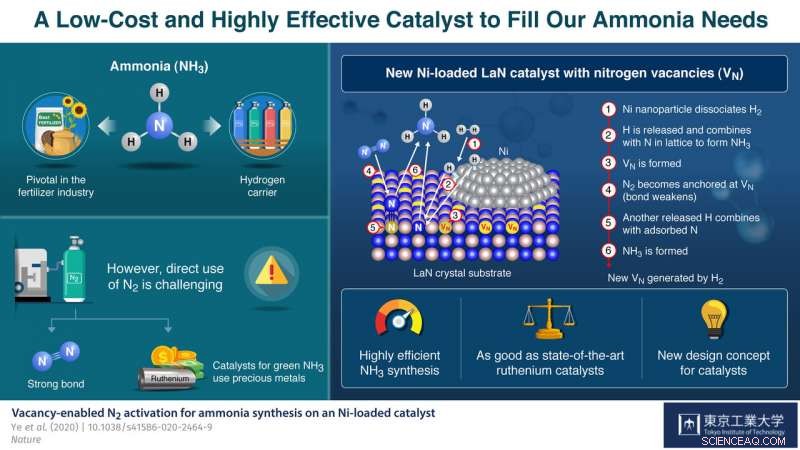
Nickel-laddad lantannitrid (LaN) möjliggör stabil och mycket effektiv ammoniaksyntes. Kvävevakanser genereras på LaN med låg formationsenergi, och effektivt binda och aktivera N2. Upphovsman:Tokyo Tech
Ammoniak (NH 3 ) är en av de vanligaste kemikalierna i världen, på grund av dess användning som en viktig ingrediens i ett brett spektrum av industriella tillverkningsprocesser. Till exempel, det är avgörande för produktion av gödningsmedel, och över 150 miljoner ton av den appliceras varje år för att öka avkastningen på olika grödor. Ammoniak produceras naturligt av många levande organismer, men syntetisera det artificiellt med kväve (N 2 ) och väte (H 2 ) gaser är utmanande eftersom den starka bindningen mellan N -atomer är svår att bryta.
Medan en metod för att producera NH 3 i industriell skala, kallad Haber-Bosch-processen, har funnits sedan början av 1900 -talet, dagens metod med bäst resultat innebär användning av rutenium, en dyr och knapp metall, som katalysator för att utlösa de nödvändiga reaktionerna. Nyligen, Prof Hideo Hosono och kollegor från Tokyo Institute of Technology (Tokyo Tech), Japan, har utvecklat en ny strategi för att producera NH 3 med lantan (La), ett mycket rikare element, i kombination med nickel (Ni).
I deras papper, publicerad i Natur , de förklarar hur de drog inspiration från ett tidigare rapporterat NH 3 produktionskatalysator med formeln Co 3 Mo 3 N, som har kvävevakanser - platser där närvaron av en kväveatom kan förväntas men som faktiskt är tomma. Dessa lediga platser observerades för att göra splittringen av N 2 molekyler lättare, vilket ledde Hosonos team neråt en ny utforskningsriktning för mer lättillgängligt och effektivt NH 3 synteskatalysatorer. Han förklarar:"Kvävevakansernas kritiska roll i Co 3 Mo 3 N inspirerade oss att överväga andra kvävehaltiga material på vilka lediga platser enkelt kunde genereras som grund för nya Ni-baserade katalysatorer. "
Katalysatorn de utvecklade består av LaN -kristaller laddade med Ni -nanopartiklar. Ni dissocierar enkelt H 2 till H -atomer. Således, förbehandling av katalysatorn med H 2 genererar lätt H -atomer, som sedan reagerar med N -atomerna i kristallstrukturen för att bilda NH 3 och skapa N lediga tjänster på LaN -stödet. Var och en av dessa tomma platser fångar sedan upp en N -atom från ett N 2 molekyl från den ingående kvävgas, vilket gör att molekylens N-N-bindning försvagas. En annan dissocierad H-atom bryter den försvagade N-N-bindningen för att producera mer NH 3 , lämnar en N -atom bakom för att fylla den ursprungliga vakansen. Dessa cykler upprepar sig själva, därigenom kontinuerligt generera kvävevakanser och upprätthålla syntesprocessen.
Detta koncept med en "dubbel aktiv plats" -katalysator visade sig vara mycket lovande. Den föreslagna katalysatorns prestanda överstiger långt den hos mer konventionella kobolt- och nickelbaserade katalysatorer och är jämförbar med även den hos ruteniumbaserade:Den ger inte bara konsekvent höga utbyten av ammoniak vid måttlig temperatur och tryck, dess struktur bibehålls även efter 100 timmars kontinuerlig reaktion, visar sin höga stabilitet.
Hosono säger, "Vi räknar med att vårt arbete kommer att stimulera ytterligare utforskning av katalysatordesigner som använder mer rikliga element. I synnerhet våra resultat illustrerar möjligheten att använda lediga platser i reaktionscykler och pekar på ett nytt designkoncept för katalysatorer för ammoniaksyntes. "
Den nya strategin kan göra produktionen av ammoniak enklare och billigare, vilket underlättar en mängd betydande industriella processer.