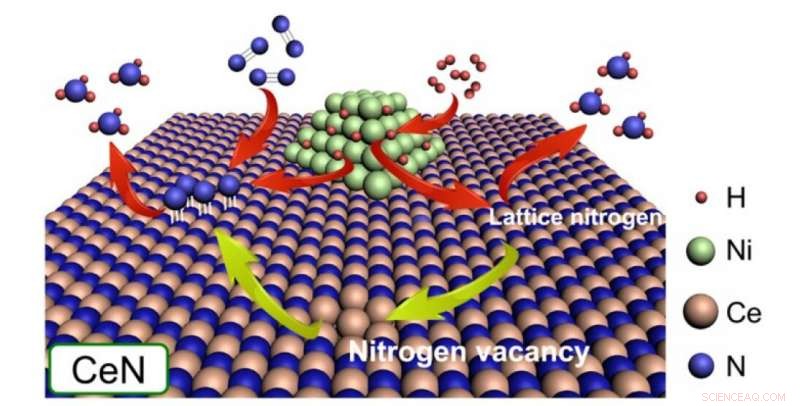
Nickelpartiklar dissocierar H2 för att ge H-atomer till antingen N-atomer från själva CeN-kristallgittret eller utskjutande N-atomer från N2-molekyler som fyller en kvävevakans. I den här studien, det visade sig att CeN utan Ni också kan dissociera H2-molekyler. Kredit:2020 American Chemical Society
Forskare vid Tokyo Institute of Technology (Tokyo Tech) utforskar hur vakans kväve i katalysatorer deltar i syntesen av ammoniak, en central kemikalie i gödselindustrin. De tog fram en allmän regel för smart design av nitridbaserade katalysatorer baserat på deras kvävevakansbildningsenergi och skapade en högpresterande katalysator för ammoniaksyntes med cerium, en riklig övergångsmetall.
Ammoniak (NH 3 ) är en naturligt förekommande kemikalie i miljön, men dess utbredda användning som en viktig ingrediens i olika tillverkningsprocesser har gjort den till en av de mest producerade kemikalierna. Det är centralt i produktionen av gödningsmedel och hjälper till att öka utbytet av olika grödor. På grund av sin höga efterfrågan, långt över 150 miljoner ton NH 3 produceras årligen. Inte överraskande, kemister har aktivt letat efter miljövänliga och energieffektiva sätt att syntetisera NH 3 .
Det konventionella sättet att producera NH 3 är genom att direkt använda kväve (N 2 ) och väte (H 2 ) gaser. Men, att bryta den starka bindningen mellan N-atomer är utmanande. Det är här katalysatorer (material som underlättar nödvändiga reaktioner) kommer in i bilden. Tyvärr, dagens bäst presterande katalysator för NH 3 syntes kräver rutenium, en sällsynt och dyr metall. I ett försök att hitta alternativ, forskare från Tokyo Tech, inklusive Dr. Tian-Nan Ye, Prof Masaaki Kitano, och Prof Hideo Hosono, har nyligen försökt ta reda på exakt vad som gör en bra katalysator för att bryta N 2 och producerar NH 3 .
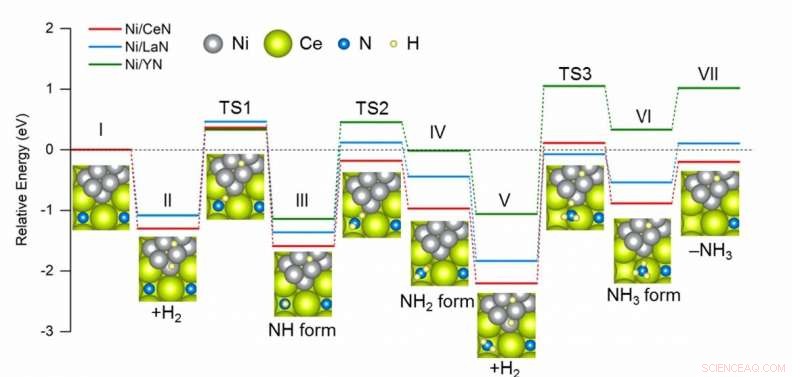
Jämförande diagram över energin som krävs i varje steg under NH3-syntes med olika katalysatorer. Ni/CeN har den mest gynnsamma energiprofilen för bildning av nya kvävevakanser, vilket resulterar i bättre katalytisk prestanda. Kredit:2020 American Chemical Society
I en tidigare tidning publicerad i Natur , Hosono och kollegor hade presenterat en ny strategi för att producera NH 3 som involverade användningen av lantannitrid (LaN) i kombination med nickel (Ni) nanopartiklar. Det viktigaste bidraget från denna studie var insikten att vakanser för kväve spelar en viktig roll i den katalytiska processen, vilket gjorde det möjligt för dem att designa en La-baserad katalysator med en prestanda som är jämförbar med den hos ruteniumbaserade. I en nyligen genomförd studie, publiceras i Journal of the American Chemical Society , forskargruppen tog sina resultat ännu längre och undersökte om energin som krävs för att producera dessa kvävevakanser är det som i slutändan definierar katalysatorernas prestanda under NH 3 produktion.
Kvävevakanserna i katalysatorns yta kan lätt fånga N 2 och försvaga dess N-N-bindning, varefter atomer dissocierade från H 2 vid Ni hoppar nanopartiklar på den utskjutande N-atomen för att producera NH 3 . Dessutom, dissocierade H-atomer kan också bilda NH 3 direkt med hjälp av N-atomer från själva katalysatorns kristallina gitter, skapar därmed nya kvävevakanser i processen. Efter framgången med deras tidigare Ni/LaN-katalysator, i den här studien, de skapade och jämförde liknande katalysatorer med olika kvävevakansbildningsenergier (ENV).
Bland de testade katalysatorerna, Ni-laddad ceriumnitrid (CeN) uppvisade den bästa katalytiska prestandan på grund av dess relativt låga ENV. Prestandan för de andra testade materialen var också direkt relaterad till deras respektive ENV. Spännande över resultatet, Prof Hosono anmärker, "Vi kan nu föreslå en generell regel för utformningen av nitridbaserade katalysatorer för NH 3 syntes, där deras ENV dominerar deras katalytiska prestanda." den katalytiska aktiviteten hos Ni/CeN var jämförbar med den hos ruteniumbaserade katalysatorer, representerar ett potentiellt miljövänligt alternativ som består av material som är mer rikligt.
Vad mer, teamet noterade också att Ni-laddning på CeN inte ens var nödvändig; kvävevakanser i CeN kan också utlösa dissociationen av H 2 molekyler. "CeN i sig självt och med Ni-laddning visade sig producera de mest effektiva och stabila katalysatorerna för ammoniaksyntes bland de olika nitridkatalysatorerna vi undersökte, " förklarar Ye. Teamet är hoppfullt att insikten från denna studie kan vara användbar i andra tillämpningar än ammoniaksyntes också. Kitano avslutar, "Att förstå nitriders roll kan kasta ljus över design och utveckling av effektiva övergångsmetallbaserade katalysatorer för andra kemiska processer."