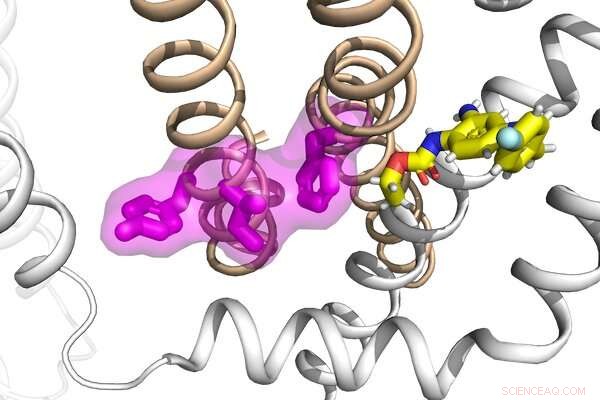
Forskare i Jianmin Cuis labb har tittat på mekanismerna bakom funktionen och dysfunktionen hos en grupp proteiner, såväl som deras interaktioner med ett antiepileptiskt läkemedel, för att utveckla en potentiell ny strategi för att behandla epilepsi. Kredit:Cui lab
Epilepsi är en neurologisk störning som uppstår från onormal elektrisk aktivitet i hjärnan som leder till anfall. Dessa anfall kan ha en mängd olika orsaker, inklusive genetiska varianter i en familj av proteiner som reglerar kaliumjoner i hjärnan. Forskare vid Washington University i St Louis har lett ett internationellt team för att ta en närmare titt på mekanismerna bakom funktionen och dysfunktionen hos dessa proteiner, samt deras interaktioner med ett antiepileptiskt läkemedel, för att utveckla en potentiell ny strategi för att behandla epilepsi.
Jianmin Cui, professor i biomedicinsk teknik vid McKelvey School of Engineering, och Nien-Du Yang, en doktorand i biomedicinsk teknik som bedriver forskning i Cuis labb, slog sig ihop med Harley Kurata, docent i farmakologi vid University of Alberta, och undersökte arbetsmekanismen för två kaliumjonkanaler, KCNQ2 och KCNQ3. Deras fynd avslöjar en konserverad mekanism för KCNQ-kanalaktivering som är ett mål för både epilepsikopplade mutationer och en liten molekylförening.
Verket publicerades den 20 juli i Science Advances .
KCNQ-kaliumkanalfamiljen har flera funktioner, från att reglera hjärtslag (genom KCNQ1) till att kontrollera nervcellers excitabilitet (genom KCNQ2-5). Dessa kanaler är spänningsaktiverade så att de känner av spänningsförändringar över cellmembranet och öppnar och stänger som svar. Kommunikationen mellan spänningsavkänning och kanalporöppning är känd som elektromekanisk koppling, en process som involverar konformationsförändringar av proteinet under spänningsberoende aktivering.
Cuis team har tidigare visat att KCNQ1, hjärt-KCNQ-isoformen, har en tvåstegsprocess i elektromekanisk koppling som leder till två distinkta kanalöppna tillstånd, mellanöppet och aktiverat-öppet. Reglering av de två öppna tillstånden ligger till grund för KCNQ1:s vävnadsspecifika moduleringar, sjukdomspatogenes och farmakologi. KCNQ2 och KCNQ3 är mycket uttryckta i det centrala nervsystemet och är de huvudsakliga bidragsgivarna till M-strömmen, en kritisk kaliumström som modulerar neuronal excitabilitet. Därför är försämrad M-strömsfunktion av medfödda mutationer i KCNQ2 och KCNQ3 vanligtvis förknippad med tidig debut och pediatrisk epilepsi.
"Även om KCNQ-kanaler är mycket lika i sina sekvenser och strukturer, om de neuronala KCNQ-isoformerna också delar samma elektromekaniska kopplingsmekanism eller två öppna tillstånd är oklart", säger Yang, tidningens första författare. "Detta arbete avslöjar viktiga likheter och skillnader mellan dessa kanaler som kan ha viktiga konsekvenser för deras funktion i kardiomyocyter eller neuroner."
Teamet använde en mängd olika metoder för att studera den elektromekaniska kopplingsmekanismen i dessa kaliumkanaler, inklusive att skapa specifika genetiska mutationer i kanalerna, elektrofysiologi och fluorescensoptiska mätningar.
"Att klargöra den molekylära mekanismen för elektromekanisk koppling är ett viktigt steg mot att förstå den spänningsberoende grindningen av kaliumkanaler," sa Cui. "Vi gav funktionella bevis för att de neuronala KCNQ2- och KCNQ3-kanalerna skiljer sig från KCNQ1 där de har ett enda aktiverat-öppet tillstånd men med en konserverad elektromekanisk kopplingsmekanism som är specifik för det aktiverade-öppna tillståndet."
Dessa kanaler är främsta mål för behandlingar för epilepsi, fann forskarna. Teamet identifierade också en uppsättning mutationer i KCNQ2 och KCNQ3 associerade med tidig infantil epileptisk encefalopati, en allvarlig form av barndomsepilepsi, som specifikt stör den elektromekaniska kopplingen av kanalerna. Forskarna drog fördel av en antiepileptisk prototyp av läkemedel retigabin med tanke på dess verkningsmekanism på neuronala KCNQ-kanaler och visade att den elektromekaniska kopplingen direkt kan förbättras för att rädda funktionen hos dessa sjuka mutanter. Deras studier tyder på att den elektromekaniska kopplingsmekanismen i KCNQ-kanaler kan vara ett effektivt mål, vilket presenterar en ny farmakologisk strategi för att utveckla mer effektiva terapier för epilepsibehandling. + Utforska vidare