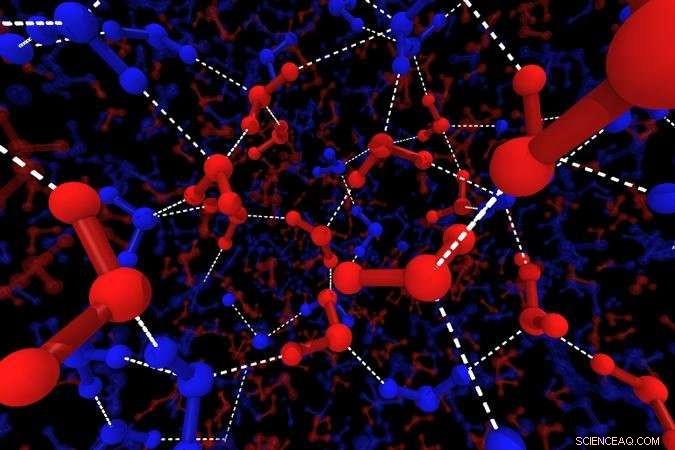
Illustration av vattnets lokala strukturer. De blå linjerna visar H2O -molekylerna i tetraedral struktur, de röda linjerna visar H2O -molekyler med störd struktur. De stora bollarna visar syreatomer, de små bollarna visar väte och de prickade vita linjerna representerar vätebindningar. Upphovsman:2018 Hajime Tanaka, Institute of Industrial Science, University of Tokyo
Ett japanskt forskargrupp som leds av University of Tokyo undersökte den ömtåliga till starka övergången av vatten. Till skillnad från de flesta vätskor, när vattnet kyls, ökningstakten för dess viskositet når ett maximum vid en viss låg temperatur. Teamet visade att modellering av vatten som en temperaturberoende blandning av två tillstånd-stört snabbt vatten och lokalt beställt långsamt vatten-förklarade den bräckliga till starka övergången och undvek de felaktiga förutsägelserna från tidigare teorier baserade på glasartat beteende.
Vatten är konstigt på många sätt. Några av dess kemiska egenskaper är bekanta, som att expandera när det fryser till is. En mindre känd nyfikenhet, som den delar med bara några andra vätskor, är den ömtåliga till starka övergången. Förklarar detta beteende, som avser hur kallt vatten rinner, har länge varit en källa till debatt. Nu, en övertygande förklaring har lagts fram av forskare i Tokyo.
När vätskor svalnar, deras dynamik saktar ner och de blir viskösa. För de flesta vätskor, hastighetsminskningen är konstant som en funktion av temperaturen och dessa är kända som starka vätskor. För ömtåliga vätskor, dock, hastigheten stiger kontinuerligt när temperaturen sjunker. Vatten är ovanligt i detta avseende - det är skört vid rumstemperatur, men stark vid låga temperaturer, där dess hastighet för ökande viskositet når en topp.
Denna ömtåliga till starka övergång är svårfångad, förekommer endast i den överkylda regimen, under vattnets vanliga fryspunkt. Tidiga modeller försökte koppla det till glasartad dynamik, eftersom underkylt vatten är känt för att vara en glasformare. Dock, ett team som leds av University of Tokyos Institute of Industrial Science (IIS) föreslår en tvåstatsteori, i själva verket modellera vatten som en blandning av två samexisterande vätskor.
Matematiskt, den starka/bräckliga skillnaden vilar på Arrhenius -lagen för dynamiska processer - starka vätskor följer denna lag, men för sköra, den snabba ökningen av viskositeten är superarrhenius. Som rapporterats i tidningen PNAS , IIS -teamet ändrade denna uppfattning genom att anse att vatten bestod av två stater, kallas "snabb" och "långsam, "som är strukturellt olika men båda lyder Arrhenius dynamik.
"Vi simulerade vatten genom molekylär dynamik och letade efter strukturella mönster, "förklarar studiens medförfattare Rui Shi." H2O-molekyler samlas alltid i tetraeder, men vi såg att några av dessa lokala strukturer var mycket ordnade, andra mindre. "De störda staterna motsvarar snabbt vatten, och dominerar vid hög temperatur, medan det välordnade långsamma tillståndet tar över när provet kyls.
Avgörande, ekvationerna som härrör från tvåstatsmodellen förutsäger framgångsrikt den ömtåliga till starka överkorsningen. Detta händer långt över glasövergångspunkten - glasartat beteende verkar vara en röd sill när det gäller denna fråga. Det faktum att snabbt vatten har Arrhenius, snarare än maktlag, dynamik löser också felaktiga förutsägelser baserat på tidigare försök att koppla vattnets skörhet till vissa aspekter av dess fasdiagram.
"Bräckligt vatten kan vara en illusion. Den skenbara övergången är en artefakt av den temperaturberoende balansen mellan två starka vätskestatus, "säger huvudförfattaren Hajime Tanaka." Förekomsten av två stater återspeglar vattens tendens att bilda lokala strukturer, vilket är lättare vid låg temperatur. Faktiskt, andra vätskor med en ömtålig till stark övergång, som kiseldioxid, visa även lokal beställning. Vi föreslår att detta, snarare än något glasartat beteende, är det som skiljer dem från sanna bräckliga vätskor. "