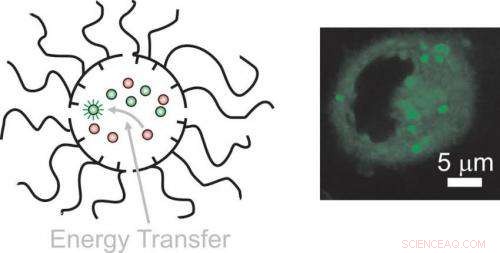
Den sekventiella transporten av donatorer och acceptorer över cellmembran med oberoende och dynamiska nanobärare möjliggör energiöverföring uteslutande i det intracellulära utrymmet med åtföljande fluorescensaktivering. Kredit:Francisco Raymo
Med det fortsatta behovet av mycket små enheter i terapeutiska tillämpningar, det finns en växande efterfrågan på utveckling av nanopartiklar som kan transportera och leverera läkemedel till målceller i människokroppen.
Nyligen, forskare skapade nanopartiklar som under rätt förhållanden, självmontera – fångar in komplementära gästmolekyler i sin struktur. Som små ubåtar, dessa mångsidiga nanobärare kan navigera i den vattniga miljön som omger celler och transportera sina gästmolekyler genom membranet av levande celler för att sekventiellt leverera sin last.
Även om transporten av molekyler inuti celler med nanopartiklar tidigare har uppnåtts med olika metoder, forskare har utvecklat nanopartiklar som kan leverera och utbyta komplementära molekyler. För praktiska tillämpningar, dessa nanobärare är mycket önskvärda, förklarar Francisco Raymo, professor i kemi vid University of Miami College of Arts and Sciences och ledande utredare för detta projekt.
"Förmågan att leverera distinkta arter inuti celler oberoende och tvinga dem att interagera, uteslutande i den intracellulära miljön, kan utvecklas till en värdefull strategi för att aktivera läkemedel inuti celler, säger Raymo.
De nya nanobärarna är 15 nanometer i diameter. De är supramolekylära konstruktioner som består av byggstenar som kallas amfifila polymerer. Dessa nanobärare håller gästmolekylerna inom gränserna för deras vattenolösliga inre och använder deras vattenlösliga yttre för att resa genom en vattenhaltig miljö. Som ett resultat, dessa nanovehicles är idealiska för att överföra molekyler som annars skulle vara olösliga i vatten, över en flytande miljö.
"Väl inne i en levande cell, partiklarna blandas och byter ut sin last. Denna interaktion möjliggör energiöverföring mellan de internaliserade molekylerna, säger Raymo, chef för UM:s laboratorium för molekylär fotonik. "Om de kompletterande energigivarna och -acceptorerna laddas separat och sekventiellt, överföringen av energi mellan dem sker uteslutande inom det intracellulära utrymmet, " säger han. "När energiöverföringen äger rum, acceptorerna avger en fluorescerande signal som kan observeras med ett mikroskop."
Väsentliga för denna mekanism är de icke-kovalenta bindningarna som löst håller ihop de supramolekylära konstruktionerna. Dessa svaga bindningar finns mellan molekyler med komplementära former och elektroniska egenskaper. De är ansvariga för supramolekylernas förmåga att samlas spontant i flytande miljöer. Under rätt förutsättningar, reversibiliteten hos dessa svaga icke-kovalenta kontakter tillåter de supramolekylära konstruktionerna att utbyta sina komponenter såväl som sin last.
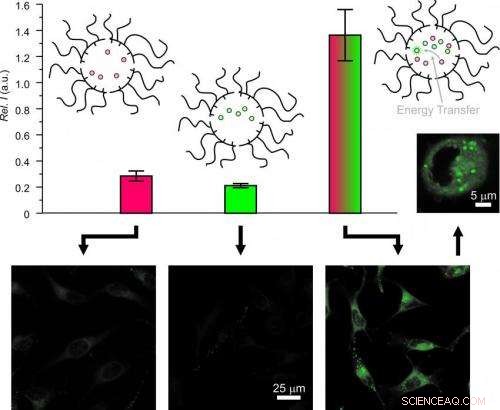
Den sekventiella transporten av donatorer och acceptorer över cellmembran med oberoende och dynamiska nanobärare möjliggör energiöverföring uteslutande i det intracellulära utrymmet med åtföljande fluorescensaktivering. Kredit:Francisco Raymo
Experimenten utfördes med cellkulturer. Det är ännu inte känt om nanopartiklarna faktiskt kan färdas genom blodomloppet.
"Det skulle vara drömmen, men vi har inga bevis för att de faktiskt kan göra det, " säger Raymo. "Men, det är den riktning vi är på väg."
Nästa fas av denna undersökning innebär att visa att denna metod kan användas för att utföra kemiska reaktioner inuti celler, istället för energiöverföringar.
"Storleken på dessa nanopartiklar, deras dynamiska karaktär och det faktum att reaktionerna äger rum under normala biologiska förhållanden (vid omgivningstemperatur och neutral miljö) gör dessa nanopartiklar till en idealisk vehikel för kontrollerad aktivering av läkemedel, direkt inuti cellerna, säger Raymo.
Den aktuella studien har titeln "Intracellulärt gästutbyte mellan dynamiska supramolekylära värdar." Den är publicerad i Journal of the American Chemical Society .
Andra författare är John F. Callan, medförfattare till studien, från School of Pharmacy and Pharmaceutical Sciences vid University of Ulster; Subramani Swaminathan och Janet Cusido från UM:s Laboratory for Molecular Photonics, Institutionen för kemi i College of Arts and Sciences; och Colin Fowley och Bridgeen McCuaghan, School of Pharmacy and Pharmaceutical Sciences vid University of Ulster.