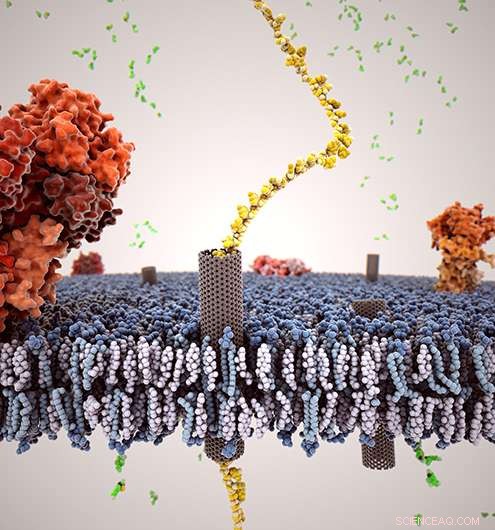
Avbildning av kolnanorör (grå) insatt i ett cellmembran, med en enda DNA -sträng (guld) som passerar genom nanoröret. Kredit:Lawrence Livermore National Laboratory
För första gången, spontant införande av kolnanorör (CNT) i naturliga såväl som syntetiska cellmembran för att bilda porer som efterliknar biologiska kanaler har visats. Trots deras extremt enkla struktur, dessa CNT-membranporer replikerar de huvudsakliga funktionella beteendena hos poriner (proteinbaserade biologiska kanaler), såsom selektiv transport av protoner, vatten, joner, och små molekyler.
Den prediktiva designen och skapandet av robusta syntetmembran som replikerar de mycket effektiva och selektiva transportprocesserna för biologiska kanaler är ett utmanande mål. CNT -poriner som utvecklats här är lovande biomimetiska plattformar för nanofluidiska studier, bygga bioelektroniska gränssnitt och syntetiska celler, och fungerar som nyckelkomponenter för energieffektiva membranbaserade separationssystem.
För första gången, en process för att spontant sätta in kolnanorör (CNT) i cellmembranen, både naturliga såväl som syntetiska, att bilda porer som efterliknar biologiska kanaler har visats. Robust, syntetiska membran som replikerar de mycket effektiva och selektiva transportprocesserna för biologiska kanaler är mycket eftertraktade men har inte realiserats än. CNT tros vara de bästa kandidaterna för att efterlikna biologisk transport på grund av likheten mellan deras inre porstruktur och de stora biologiska kanalerna och möjligheten att, baserat på beräkningsmodellering, CNT kunde självinföras i biologiska membran. Dock, skapandet av sådana hybridmembranstrukturer har förblivit en enastående utmaning.
Nu, ett team ledd av forskare vid Lawrence Livermore National Laboratory och inklusive forskare från Lawrence Berkeley National Laboratory, University of California i Berkeley, och universitetet i Baskien i Spanien har bildat ett hybridmembran genom att skapa membrankanaler från korta CNT. De fann att CNT:er funktionaliserade med lipid (fettiga) molekyler som spontant sätts in i cellmembran, både naturligt och syntetiskt. Viktigt, införande av de små CNT i levande cellväggar gjorde det möjligt för dem att samverka direkt med ett verkligt biologiskt system, något som inte är möjligt med långa CNT.
Detta gränssnitt gjorde det möjligt att undersöka den grundläggande fysiken för nanoportransport med hjälp av en modell som närmare närmade sig en jonkanal och som efterliknar transport i biologiska porer. Trots deras extremt enkla struktur, dessa membranporer reproducerar det huvudsakliga funktionella beteendet hos biologiska kanaler, såsom selektiv transport av protoner, vatten, joner, och små molekyler. CNT påverkar inte membranets integritet. Elektronmikroskopi avslöjade att insättning inte är selektiv för en viss nanorörlängd. Vidare, en nästan vinkelrät orientering av CNT:erna i membranet är starkt föredragen, i motsats till tidigare simuleringsbaserade förutsägelser.
Trots betydande CNT-längdvariationer, transportegenskaperna hos dessa hybridmembran, kallad "CNT-poriner" (där termen poriner hänvisar till proteinbaserade biologiska kanaler), är mycket väldefinierade, föreslår starkt att transport genom CNT -porerna endast styrs av barriärerna vid porutgången och -inträdet. Dessutom, nanoskala begränsning av joner i den smala hydrofoba kanalen ger upphov till jonströmssvängningar, efterliknar on-off-gating-processen för jontransport som sker i biologiska kanaler. Kumulativt, dessa resultat pekar på att hybridmaterialen har användbara membranapplikationer. Dessa applikationer inkluderar att tillhandahålla en plattform för nanofluidstudier, bygga bioelektroniska gränssnitt och artificiella celler, och fungerar som nyckelkomponenter för energieffektiva membranseparationssystem.