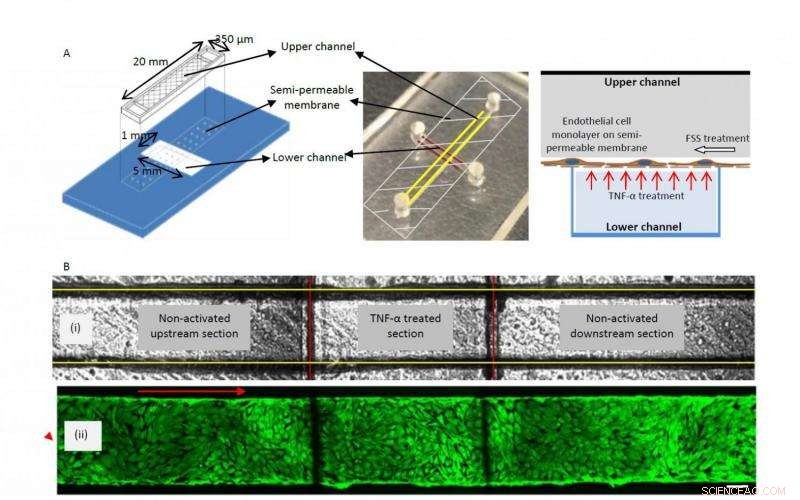
En grafisk schematisk (vänster) och fotografi (mitten) av tvåskiktsanordningen som visar den övre (markerade med gula linjer) och nedre (markerade med röda linjer) kanalen åtskilda av ett semipermeabelt membran. Schemat till höger visar odlingen av ett monolager av endotelceller på det semipermeabla membranet och det sätt på vilket TNF-a-behandling utförs från den nedre kanalen. B, (i) Ljusfältsbild av den övre (markerade med gula linjer) och nedre (markerade med röda linjer) kanal som definierar uppströms, TNF-α aktiverade och nedströms sektioner, (ii) Fluorescensmärkta F-aktin cytoskelett (FITC falloidin) bilder av sammanflytande BAOEC skikt anpassat till flöde (12 dyn/cm2 FSS under 24 timmar). Cellerna odlas på det semipermeabla membranet i anordningens övre kanal. Pilen visar flödesriktningen (Skalstång:100 μm) Kredit:Yaling Liu
Nanoteknik har lett till bättre diagnostiska tekniker och effektivare behandlingar för en mängd olika sjukdomar. Små apparater som mäter mellan 1 och 100 mikrometer – en mikrometer är lika med en miljondels meter – gör det möjligt för forskare att observera cellaktivitet och leverera läkemedel till enskilda celler – ett genombrott som är på gränsen till att revolutionera precisionsmedicin för behandling av sjukdomar som t.ex. cancer.
Ett hinder för att uppfylla nanomedicinens löfte är oförmågan att observera cell till cell interaktioner på nanoskala i en miljö som nära simulerar den dynamiska miljön inuti kroppen. En mikrovätskemiljö som efterliknar blodflödet är nyckeln till att lära sig hur celler skadas av sjukdomstillstånd - och hur de kan återhämta sig som svar på behandling.
Nu har ett team av forskare vid Lehigh University och University of Pennsylvania utvecklat en teknik för att observera cell till cell interaktion på nanoskala under mikrovätskeförhållanden. De har framgångsrikt tillämpat tekniken för att studera blodkärlsinflammation, ett tillstånd som sätter scenen för hjärtsjukdomar, den främsta dödsorsaken i USA och globalt. Deras resultat har publicerats i Biomikrofluidik .
"Vi har visat att vår teknik framgångsrikt kan tillämpas på studier av inflammation och arbetar på ett sätt att på liknande sätt observera och ingripa i reparationen av tumörceller, sa Yaling Liu, docent i maskinteknik och mekanik, Bioteknik vid Lehigh och en medförfattare på studien.
Nuvarande in vitro drogtester är kostsamt, tidskrävande och relativt dålig på att förutsäga läkemedelsprestanda in vivo. PharmaFlux-teknologin är en testtjänst för mikroenheter för läkemedelskandidater i mikromiljöer med efterliknade sjukdomar. Kredit:Yaling Liu
Efterliknar den dynamiska överföringsprocessen
Kronisk, låggradig inflammation är starkt förknippad med dysfunktionella endotelceller, som bildar det inre slemhinnan i blodkärlen. Utseendet av intercellulär adhesionsmolekyl-1 (ICAM-1) på ytan av endotelceller, avgörande för att reglera cell till cell interaktion som en del av kroppens immunsystemsvar, är ett säkert tecken på att inflammation och sjukdom finns. Därför, Att observera aktiveringen av endotelceller under sjukdomstillstånd är väsentligt för att förstå hur hjärtsjukdomar utvecklas och hur man stoppar den.
Det bästa sättet att observera dessa förändringar är inuti kroppen. Dock, det är väldigt svårt att göra detta. Att observera sjukdomen i en statisk cellkultur - genom att ta bort och odla celler i en artificiell miljö som en petriskål - är begränsad i sin förmåga att exakt skildra de dynamiska interaktionerna under blodflödesförhållanden.
Förutom Liu, teamet från Lehigh inkluderar Linda Lowe-Krentz, Professor, Biologi; H. Daniel Ou-Yang, Professor, Fysik; och Ph.D. elev Antony Thomas. De samarbetade med Vladimir R. Muzykantov, Professor i farmakologi vid Penn för att utveckla ett blodkärl på ett chip för att studera dynamiken hos ICAM-1 på ytan av endotelceller aktiverade under sjukdomstillstånd.
"Vi kunde härma och observera den dynamiska överföringsprocessen - det ögonblicket när den intercellulära adhesionsmolekylen-1-antikroppsbelagda nanopartiklarna binder till cellen som signalerar inflammationsuppreglering av endotelceller - på ett chip. Vi kunde också exakt kontrollera flödet av vätska, ", sa Liu. "Denna pålitliga och relativt enkla metod simulerar de förhållanden under vilka endotelceller existerar i kroppen, gör det möjligt att observera cellulär patologi i realtid, och analysera skillnader i cellernas svar på behandling."
En idealisk miljö för drogtester
Eftersom denna nya teknik skapar en plattform för att fokusera på en viss sjuk region, Liu och hans kollegor anser att den är idealisk för att testa nya sjukdomsbehandlingar.
Friska celler finns på samma chip som sjuka celler, vilket möjliggör mer lokal kontroll för att testa ett visst läkemedel. Detta, i kombination med den simulerade blodflödesmiljön, gör det också möjligt för forskare att samla in en mycket mer robust datauppsättning än de skulle kunna genom att använda en statisk kultur.
Teamets användning av antikroppsbelagda nanopartiklar som avbildningssonder för att bedöma cellers egenskaper är en annan viktig fördel med den nya tekniken. Genom att använda nanopartikelsonderna elimineras behovet av att använda radioisotopmärkta ICAM-1-antikroppar för att spåra cellulära interaktioner - en teknik som är fylld av regulatoriska och säkerhetsmässiga utmaningar. Det är också väldigt dyrt.
"Vårt system ger en säkrare, ett mindre kostnadskrävande sätt att testa ett nytt läkemedel i en miljö som ligger nära en sjuk regions miljö, sa Liu.
En "bro" till precisionsmedicin
Teamets innovativa plattform ger också en avgörande tidig inblick i ett nytt läkemedels effektivitet och säkerhet – ett särskilt viktigt steg med tanke på riskerna och kostnaderna förknippade med kliniska prövningar på människor.
En studie från 2012 som lämnades in till U.S. Department of Health and Human Services detaljerade kostnaderna för kliniska läkemedelsprövningar. Författarna till "Examination of Clinical Trial Costs and Barriers for Drug Development" uppskattade att kostnaden för att slutföra kliniska prövningar för ett nytt läkemedel är mellan cirka 50 miljoner dollar och 115 miljoner dollar beroende på det terapeutiska området – andningsorgan och onkologi är bland de dyraste .
Studien identifierade också kostnader för kliniska prövningar som en möjlig orsak bakom en nedgång i ansökningar om nya läkemedelsgodkännanden. Mellan 2003 och 2012, antalet FDA-godkännanden av nya läkemedel per år sjönk från det föregående decenniets genomsnitt på 30 till 25,7. Det genomsnittliga årliga antalet anmälningar har också minskat något under samma tidsperiod. Författarna säger:"En minskning av pipeline för läkemedelsansökningar innebär färre nya behandlingar under kommande år."
Tekniken som utvecklats av Lehigh och UPenn-teamet ger läkemedelsföretag möjligheten att tidigt få en titt på effektiviteten och säkerhetsprofilen för en ny behandling innan de bestämmer sig för kliniska prövningar, därmed mindre risk och lägre kostnader. Enligt Liu, detta tidiga utseende skulle kunna fungera som en "bro" mellan utvecklingen av ett läkemedel och försök på människor. I slutändan – och viktigast av allt – kan tillhandahållandet av denna "bro" resultera i utvecklingen av fler nya sjukdomsbehandlingar som når konsumenterna snabbare.
Genom att direkt odla patientceller i deras biomimetiska chip och testa under liknande förhållanden som observerats in vivo, det kan ge insikter för precisionsmedicin som är skräddarsydd för en specifik patient under en patientspecifik miljö.
Liu, tillsammans med branschmentorn Ira Weisberg (VD för Amherst Pharmaceuticals) och entreprenörsledaren Christopher Uhl (Bioengineering Ph.D.-student vid Lehigh) har fått ett NSF Innovation Corp-bidrag och har arbetat med Lehigh Universitys Office of Technology Transfer för att kommersialisera tekniken under firmanamnet PharmaFlux.
"När vi fortsätter att utveckla plattformen bortom studiet av inflammation, "Liu säger, "vi hoppas kunna ge ett betydande bidrag till accelerationen av riktad läkemedelsleverans och hjälpa till att inleda en ny tid av bättre medicin."