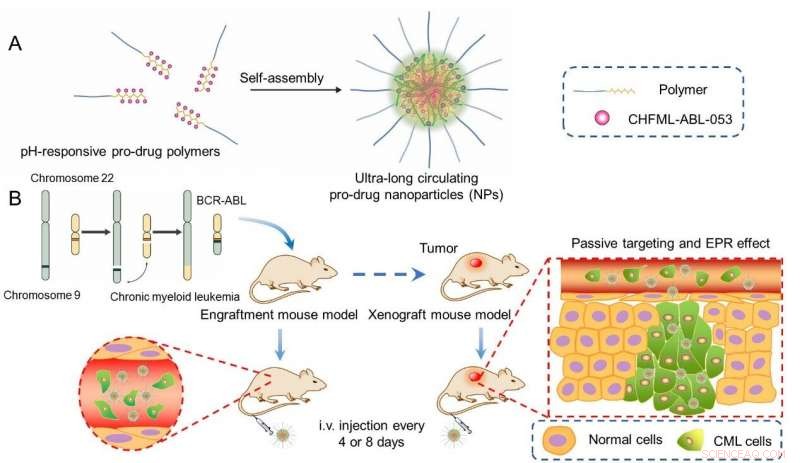
(A) Självmontering av NP och (B) deras inriktning på CML på två modeller. Kredit:FU Liyi, ZOU Fengming, LIU Qingsong och LIU Jing
Ett ultralångt cirkulerande nanomaterial har utvecklats av forskare genom konjugering av CHMFL-ABL-053 till en amfifil polymer och efterföljande självmontering till en nanopartikel (NP) med hög belastning.
Utvecklad av Drs. Fu Liyi och Zou Fengming, och leds av profs. Liu Qingsong och Liu Jing från Institute of Health &Medical Technology, Hefei Institutes of Physical Science, beredningen kunde avsevärt förbättra dess löslighet och drastiskt förlänga dess cirkulationshalveringstid.
Kronisk myeloisk leukemi (KML) är en klonal hematopoetisk myeloproliferativ stamcellssjukdom, som främst orsakas av den kromosomala translokationen mellan Abelson (ABL)-genen och BCR-genen (breakpoint cluster region). Även om de FDA-godkända BCR-ABL-hämmarna, såsom Imatinib och Dasatinib etc. kan avsevärt förbättra 10-årsöverlevnaden för patienterna, deras utanför mål, som DDR1/2 och c-kit, kan leda till minskning av mastceller, vaskulära biverkningar och andra oönskade biverkningar.
Tidigare relaterad forskning utfördes av Prof. Liu Qingsong och Prof. Liu Jings grupp. Och BCR-ABL-hämmaren CHMFL-ABL-053 hade en bättre selektivitet mot målet för BCR-ABL jämfört med andra proteinkinaser. Dock, som alla av denna klass av inhibitorer, det måste behandlas oralt varje dag på grund av dess korta halveringstid, vilket inte bara skulle öka patienternas ekonomiska börda, men också leda till kumulativa toxiciteter.
Den här gången, teamet drivit sitt arbete vidare för att göra en modifiering baserad på deras tidigare arbete. I 150 dagars långsiktiga engraftment-modellexperiment, långa intravenösa doseringsintervall av NPs (var 4:e eller 8:e dag) uppvisade mycket bättre överlevnad och försumbar toxicitet jämfört med daglig oral administrering av inhibitorn.
NPs visade utmärkt hämning av tumörtillväxt i den subkutana xenograftmodellen. Den utmärkta anti-leukemiska effekten av NP i den långa injektionscykeln på båda modellerna kan ge en ny, effektiv och säker terapeutisk strategi för BCR-ABL-positiv KML.