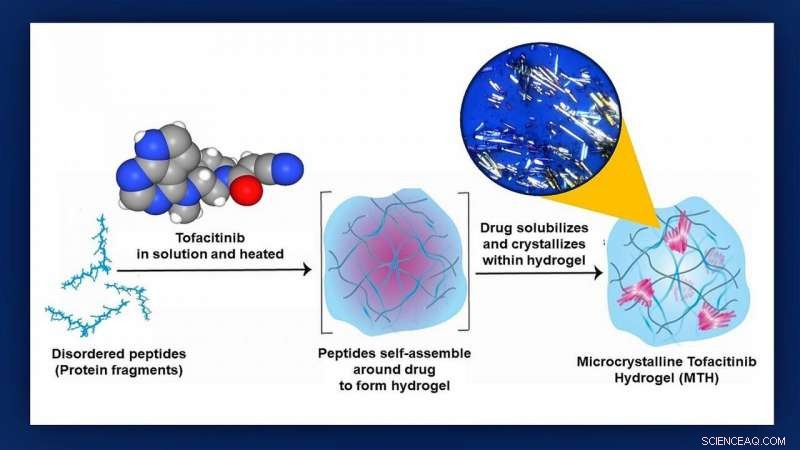
Forskare från Johns Hopkins Medicine och NCI Frederick har på möss visat att de enkelt kan leverera en lovande anti-avstötningsterapi direkt till ett transplanterat hjärta genom att förpacka det i en liten proteingelkokong känd som en hydrogel. Stegen för att konstruera hydrogelen och inkapsla läkemedlet, tofacitinib, illustreras i den här bilden. Insättningen i det övre högra hörnet är ett verkligt mikrofotografi av tofacitinib-kristallerna på plats Kredit:Grafik skapad av M.E. Newman, Johns Hopkins medicin, med hjälp av en originalillustration av Poulami Majumder och tofactinib molekylär modell med tillstånd av National Center for Biotechnology Information
För patienter som får en hjärttransplantation inom en snar framtid, det gamla ordspråket, "Bra saker kommer i små förpackningar, " kan bli ord att leva efter. I en nyligen genomförd studie, forskare vid Johns Hopkins Medicine och National Cancer Institute (NCI) visade på möss att de enkelt kan leverera ett lovande läkemedel mot avstötning direkt till området kring ett ympat hjärta genom att förpacka det i en liten tredimensionell, proteingelkokong känd som en hydrogel. Bäst av alla, forskarna säger att frisättningen av läkemedlet sprids över tiden, vilket gör det mycket reglerbart och eliminerar behovet av daglig medicinering för att hålla avstötningen i schack.
Resultaten presenteras den 18 augusti, 2020, nummer av tidskriften Små .
Att förhindra avstötning av ett transplanterat hjärta har ofta varit en Catch-22-situation. Om du ger en organmottagare stora mängder immundämpande läkemedel, det kan finnas allvarliga biverkningar, inklusive njurskador, högt blodtryck, obalanser i blodsocker och till och med lymfom. Att sänka dosen kan vara säkrare för den allmänna hälsan men ökar risken för att avstötningen inte kontrolleras ordentligt och det transplanterade hjärtat går förlorat.
"Vad som behövdes var en metod för tillförsel av läkemedel som skulle få medicin mot avstötning endast där det behövdes; skydda läkemedlet från för tidig nedbrytning; och upprätthålla en hög koncentration under den tid som behövs för att träna om immunsystemet, " säger studiens medförfattare Giorgio Raimondi, M.Sc., Ph.D., biträdande professor i plastik och rekonstruktiv kirurgi vid Johns Hopkins University School of Medicine.
"Två tidigare studier använde hydrogelmetoden för att framgångsrikt leverera konventionella immunsuppressiva läkemedel till andra platser, och detta fick oss att testa det för transplanterade hjärtan, " Raimondi förklarar. "Dessutom, arbete av ett team vid NCI Frederick National Laboratory for Cancer Research under Joel Schneider [Ph.D., en studie medförfattare] visade att hydrogel-läkemedelsförpackningar kan administreras med spruta."
Läkemedlet som dessa forskare ville leverera till transplanterade hjärtan är tofacitinib, en hämmare av den process genom vilken celler varnar deras mottaglighet för bindning med inflammationsinducerande proteiner som kallas cytokiner. I normala immunsvar mot främmande inkräktare i kroppen, cytokiner spelar en avgörande roll för att varna specialiserade vita blodkroppar – T-lymfocyter – att attackera och ta bort de hotande bakterierna eller virusen. Dock, cytokiner i närvaro av ett transplanterat hjärta kan styra immunsystemet att förstöra transplantatet.
För att se om en hydrogelkurir kan användas för att leverera tofacitinib, forskarna ympade först mushjärtan i halsen på mottagarmöss för att skapa en djurmodell av en mänsklig transplantation. Nästa, de blandade tofacitinib med en lösning av små proteinfragment som samlades runt läkemedlet under en 24-timmars inkubationsprocess som Raimondi liknar med "gör din egen kristall"-satser som är populära bland barn.
"Vi fann att att göra tofacitinib till en kristall bäst kontrollerade hur läkemedlet sprider sig från hydrogelen, " säger studiens huvudförfattare Poulami Majumder, Ph.D., tidigare NCI vid Frederick postdoktor. "Den resulterande 'mikrokristallina tofacitinib-hydrogelen, ' eller MTH, var extremt stabil, bevarade det inkapslade läkemedlet i perfekt skick och kunde injiceras på transplantationsstället helt enkelt med hjälp av en spruta."
Forskarna testade MTH-leveranssystemet i sin musmodell tillsammans med ett andra immunsuppressivt läkemedel, CTLA4-Ig, som injicerades separat. Detta var första gången som denna specifika kombinationsterapi hade prövats.
För att avgöra om platsen för MTH-leverans var viktig, forskarna injicerade den förpackade medicinen lokalt, på transplantationsplatsen, och på avstånd, nära musens svans. Som förväntat, endast gruppen möss med lokala injektioner visade en signifikant ökning av transplantatets överlevnadstid.
"Den genomsnittliga överlevnaden för de transplanterade hjärtan i den lokalt injicerade gruppen var cirka 125 dagar jämfört med bara 35 dagar för möss injicerade med MTH långt från transplantationen, ", säger Raimondi. "Vi testade också plasman från den förra gruppen och hittade endast minimalt detekterbara spår av tofacitinib – vilket betyder att MTH-tillförsel håller läkemedlet nära transplantationsstället och gör det möjligt att verka synergistiskt med CTLA4-Ig för att ge förbättrat och varaktigt skydd av orgeln."
Utan tofactinib/CTLA4-behandling, Raimondi säger, de transplanterade mushjärtan slutade slå inom 10 dagar.
Raimondi säger att bland fördelarna med att använda MTH som ett läkemedelslevereringssystem är att hydrogelen släpper ut sitt innehåll långsamt, under en period av 5 till 20 dagar, och orsakar inte andra komplikationer eftersom det är biokompatibelt, icke-inflammatorisk och biologiskt nedbrytbar. Han och hans kollegor tror att genom att använda kristallteknik för att ytterligare förbättra hydrogelkapseln, mer kontroll över frisättningshastigheten kan erhållas – ett kritiskt mål att uppnå innan försök på människor kan göras – eller, kapseln kan göras "avstämbar" för att leverera läkemedel endast när det transplanterade hjärtat attackeras av immunsystemet.
Forskarna anser också att med ytterligare forskning och testning, MTH-leveranssystemet skulle kunna användas för att bekämpa avstötning av andra transplanterade organ än hjärtat och vid behandling av autoimmuna sjukdomar.