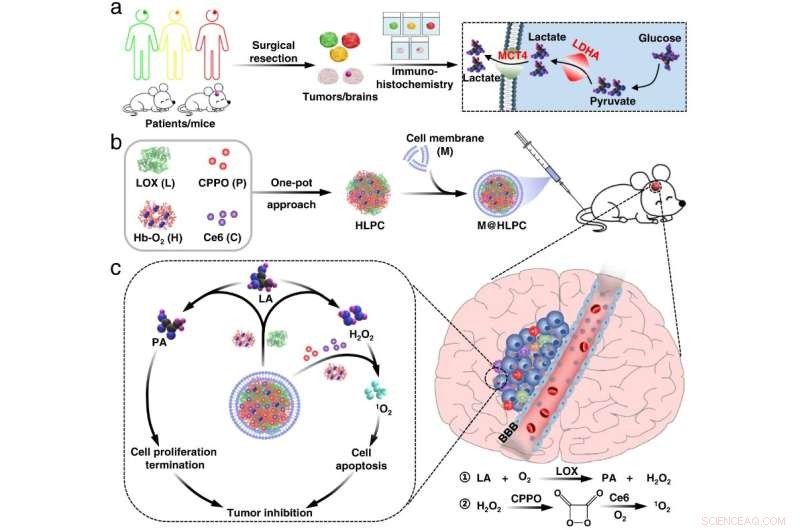
Fig. 1 Framställning av biomimetisk formulering och tumörinhiberingsmekanism. Kredit:Lu Guihong
Glioblastoma multiforme (GBM) är en aggressiv hjärncancer med dålig prognos och få behandlingsalternativ. Nya och effektiva metoder för GBM-behandling behövs därför akut.
Baserat på observation av förhöjt laktat i resekerat GBM, har forskare från Institute of Process Engineering (IPE) vid den kinesiska vetenskapsakademin och Shenzhen Second People's Hospital utvecklat en biomimetisk formulering som använder riktade tillförselmedel för laktatmetabolismbaserad synergistisk terapi mot GBM.
Studien publicerades i Nature Communications den 21 juli.
Inriktning på laktatmetabolism är en attraktiv tumörterapeutisk strategi. Det finns dock inga rapporter som direkt utnyttjar laktatmetabolismen för GBM-behandlingar. En begränsning är förekomsten av blod-hjärnbarriären, som hindrar de flesta läkemedelsmolekyler (inklusive de som stör laktatmetabolismen) från att nå hjärnan.
Dessutom, med tanke på komplexiteten och infiltrerande egenskaper hos GBM, är det mycket osannolikt att laktatmetabolisk monoterapi effektivt eliminerar GBM-celler. Därför är det viktigt att utveckla synergistiska strategier för att förbättra den terapeutiska effektiviteten av laktatmetabolisk terapi.
I denna studie samlade forskarna gliomprover från en stor kohort av patienter och kvantifierade de metaboliska laktatindikatorerna LDHA och MCT4 och en representativ spridningsmarkör Ki67.
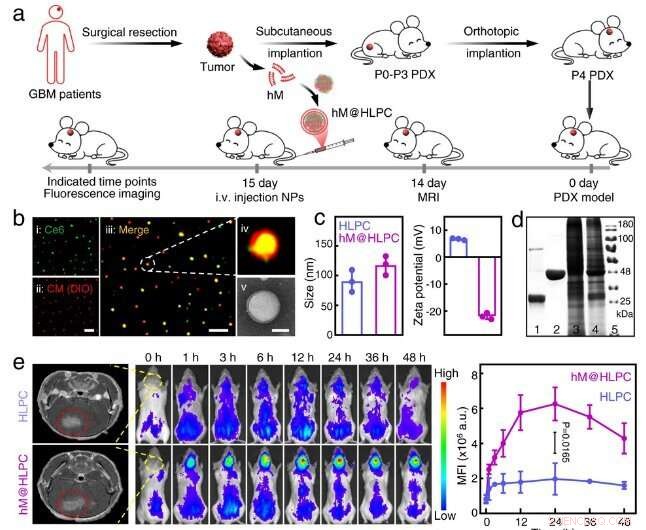
Fig. 2 Utvärdering av den synergistiska terapeutiska effekten av personlig biomimetisk formulering i PDX-modell. Kredit:Lu Guihong
"Vi observerade en positiv korrelation mellan metaboliska laktatindikatorer och omfattningen av gliomproliferation", säger professor Li Weiping från Shenzhen Second People's Hospital. Således föreslogs en effektiv metabolismbaserad synergistisk terapi som direkt skulle utnyttja det förhöjda laktatet i GBM.
Forskarna tillverkade självmonterande nanopartiklar (NP) bestående av hemoglobin (Hb), laktatoxidas (LOX), bis[2,4,5-triklor-6-(pentyloxikarbonyl)fenyl]oxalat (CPPO) och klor e6 (Ce6) ) med en enpottsmetod. De inkapslade därefter dessa självmonterade NP:er med membranmaterial framställda från U251-gliomceller för att generera det biomimetiska M@HLPC-systemet. Detta designkoncept kunde uppnå målinriktad leverans för kombinationsterapi.
"Efter intravenös injektion kunde M@HLPC passera blod-hjärnbarriären via transcytos från integrin och vaskulär cell-adhesion-protein-medierad igenkänning och sedan ackumuleras i GBM genom homotypisk igenkänning baserat på celligenkänning-funktion-associerade proteiner, " sa prof. Wei Wei från IPE.
I tumörer omvandlade LOX i NP laktat till pyrodruvsyra och väteperoxid (H2 O2 ). Pyrodruvsyran hämmade cancercelltillväxt genom att blockera histonuttryck och inducera cellcykelstopp. Parallellt med H2 O2 fungerade som ett lokalt bränsle för att reagera med den levererade CPPO för att frigöra energi, som sedan kunde användas av den medlevererade fotosensibilisatorn Ce6 för generering av cytotoxiskt singlettsyre för att döda gliomceller.
Potent terapeutisk effekt bekräftades i både cellinje-härledda xenograft och patient-derived xenograft (PDX) tumörmodeller.
"Med tanke på formuleringens säkerhet och de potenta terapeutiska effekterna mot den matchade PDX-modellen, har vår personliga biomimetiska formulering potential att översättas till klinisk tillämpning", säger Prof. Ma Guanghui från IPE. + Utforska vidare