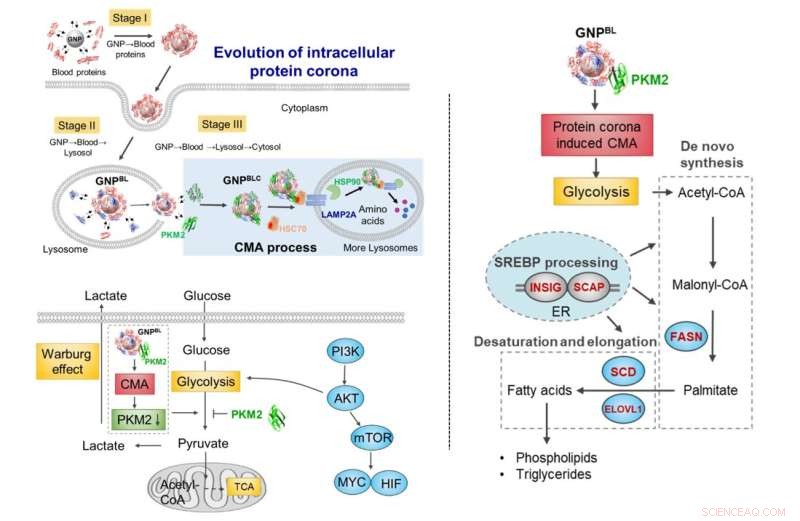
Utveckling av nanoproteinets korona under celltransport. Under transport från blod-lysosomal-cytoplasman utlöser utbytet av komponenter i proteinkorona med intracellulära proteiner (chaperoneproteiner, metaboliska kinaser) en ökning av chaperonproteinmedierad autofagiaktivitet och omformar selektivt cellmetabolism. Kredit:Chen Chunying et al.
En forskargrupp ledd av professor Chen Chunying från National Center for Nanoscience and Technology (NCNST) vid den kinesiska vetenskapsakademin (CAS) har nyligen undersökt utvecklingen av nanoproteinets korona under endocytos och dess störning av proteinhomeostas och cellceller ämnesomsättning. Deras resultat publicerades i PNAS .
När nanopartiklar kommer in i biologiska system binder biomolekyler av biologisk vätska snabbt till nanopartiklarnas yta. Nanoproteinkoronan som bildas genom att interagera med proteinmolekyler i blodet som ett startsteg har en enorm inverkan på nanopartiklarnas transport och öde. Hur bildandet av nanoproteinet corona påverkar igenkännandet, transporten, distributionen, funktionen och biologiska effekterna av nanopartiklar i vävnader och celler i olika barriärsystem är en "svart låda" för medicinsk tillämpning av nanomaterial, vilket inte bara begränsar leveransen effektiviteten av nanomedicin, men påverkar också allvarligt effektiviteten och säkerheten.
En viktig utmaning inom detta område är komplexiteten hos nanoproteinet corona, som påverkas av mångfalden av biomolekyler i olika vävnader och organ, samt fysiologiska och patologiska tillstånd. För närvarande finns det ett akut behov av att förstå hur proteinets sammansättning och strukturella egenskaper hos proteinkorona utvecklas inom biologiska mikromiljöer.
För att lösa detta problem har forskarna avslöjat det dynamiska utvecklingsmönstret för proteinsammansättningen av nanoproteinkorona i processen för celltransport genom den innovativa tillämpningen av multidimensionella multiomics (proteomics, metabolomics, lipidomics), intermolekylära interaktioner och in situ masspektrometriavbildning.
Med guldnanopartiklar som modell studerades den dynamiska evolutionsprocessen av proteinkorona från blodsystemet till intracellulärt (blod-lysosomalt-cytoplasma). När nanopartiklarna endocyterades in i lysosomen från blodmiljön och sedan flydde från lysosomen in i cytoplasman, skulle proteinsammansättningen på ytan av nanopartiklarna förändras dramatiskt. De flesta ersattes av intracellulära proteinmolekyler, som bara behöll en del av proteinkoronakomponenterna som bildas i blodmiljön.
Därefter störde intracellulär utveckling av nanoproteinkorona inte bara intracellulär proteinhomeostas (proteostas), utan utlöste också anrikningen av chaperoneproteiner (HSC70, HSP90) och pyruvatkinas M2 (PKM2) på ytan av den intracellulära nano-corona, och stimulerade chaperonförmedlad autofagi. Det påverkade ytterligare cellglykolysen, vilket orsakade förändringar i cellens energimetabolism och reglerade celllipidmetabolismen.
Den här studien belyser det evolutionära mönstret för nanopartiklar från blod till en subcellulär mikromiljö och identifierar specificiteten hos den intracellulära mikromiljön av nanoproteinkorona, och omformar därigenom cellmetabolism. Det ger också teoretiskt stöd för en fördjupad förståelse av de komplexa biologiska effekterna av nanomaterial och nanobiotisk gränssnittsreglering. + Utforska vidare