Multiresistenta bakterieinfektioner som inte kan behandlas med några kända antibiotika utgör ett allvarligt globalt hot. Publicering i tidskriften Angewandte Chemie International Edition , har ett kinesiskt forskarlag nu introducerat en metod för utveckling av nya antibiotika för att bekämpa resistenta patogener. Läkemedlen är baserade på proteinbyggstenar med fluorhaltiga lipidkedjor.
Antibiotika skrivs ofta ut alldeles för lätt. I många länder distribueras de utan recept och administreras i fabriksjordbruk:profylaktiskt för att förhindra infektioner och förbättra prestanda. Som ett resultat ökar resistensen – i allt högre grad även mot reservantibiotika. Utvecklingen av innovativa alternativ är avgörande.
Det är möjligt att dra lärdom av mikroberna själva. Lipoproteiner, små proteinmolekyler med fettsyrakedjor, används i stor utsträckning av bakterier i deras kamp mot mikrobiella konkurrenter. Ett antal lipoproteiner har redan godkänts för användning som läkemedel.
De vanligaste faktorerna bland de aktiva lipoproteinerna inkluderar en positiv laddning och en amfifil struktur, vilket betyder att de har segment som stöter bort fett och andra som stöter bort vatten. Detta gör att de kan binda till bakteriemembran och tränga igenom dem till insidan.
Teamet som leds av Yiyun Cheng vid East China Normal University i Shanghai syftar till att förstärka denna effekt genom att ersätta väteatomer i lipidkedjan med fluoratomer. Dessa gör lipidkedjan samtidigt vattenavvisande (hydrofob) och fettavvisande (lipofob). Deras särskilt låga ytenergi stärker deras bindning till cellmembran medan deras lipofobicitet stör membranets sammanhållning.
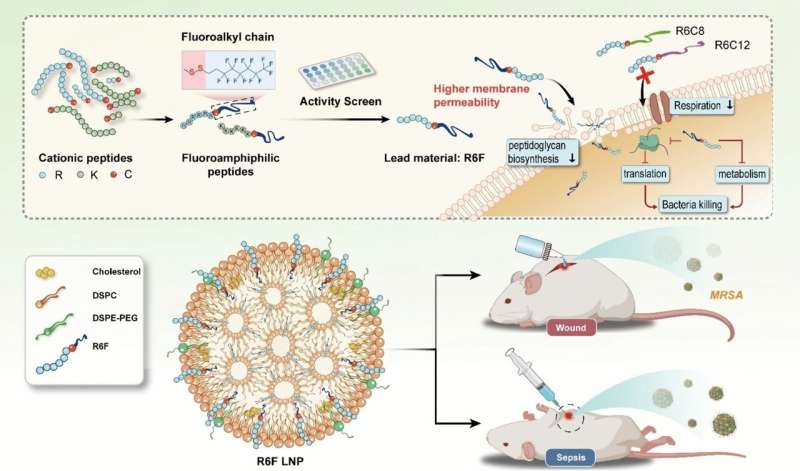
Teamet syntetiserade ett spektrum (substansbibliotek) av fluorhaltiga lipopeptider från fluorerade kolväten och peptidkedjor. För att länka samman de två delarna använde de aminosyran cystein, som binder samman dem via en disulfidbrygga.
Forskarna screenade molekylerna genom att testa deras aktivitet mot meticillinresistenta Staphylococcus aureus (MRSA), en utbredd, mycket farlig bakteriestam som är resistent mot nästan alla antibiotika. Den mest effektiva föreningen de hittade var "R6F", en fluorhaltig lipopeptid gjord av sex argininenheter och en lipidkedja gjord av åtta kolatomer och 13 fluoratomer. För att öka biokompatibiliteten var R6F innesluten i fosfolipidnanopartiklar.
I musmodeller visades R6F nanopartiklar vara mycket effektiva mot sepsis och kroniska sårinfektioner av MRSA. Inga toxiska biverkningar observerades.
Nanopartiklarna verkar attackera bakterierna på flera sätt:de hämmar syntesen av viktiga cellväggskomponenter, vilket främjar kollaps av väggarna; de tränger också igenom cellmembranet och destabiliserar det; stör andningskedjan och ämnesomsättningen; och öka den oxidativa stressen samtidigt som den stör bakteriens antioxidantförsvarssystem.
I kombination dödar dessa effekter bakterierna - andra bakterier såväl som MRSA. Inget motstånd verkar utvecklas.
Dessa insikter ger utgångspunkter för utvecklingen av högeffektiva fluorhaltiga peptidläkemedel för att behandla multi-läkemedelsresistenta bakterier.
Mer information: Jingjing Hu et al, A Fluorous Peptide Amphiphile with Potent Antimicrobial Activity for Treatment of MRSA-induced Sepsis and Chronic Wound Infection, Angewandte Chemie International Edition (2024). DOI:10.1002/anie.202403140
Journalinformation: Angewandte Chemie International Edition
Tillhandahålls av Wiley