För patienter med vissa typer av cancer har CAR T-cellsterapi inte varit något mindre än livsförändrande. Utvecklad delvis av Carl June, Richard W. Vague professor vid Perelman School of Medicine, och godkänd av Food and Drug Administration (FDA) 2017, mobiliserar CAR T-cellsterapi patienters eget immunsystem för att bekämpa lymfom och leukemi, bland annat andra cancerformer.
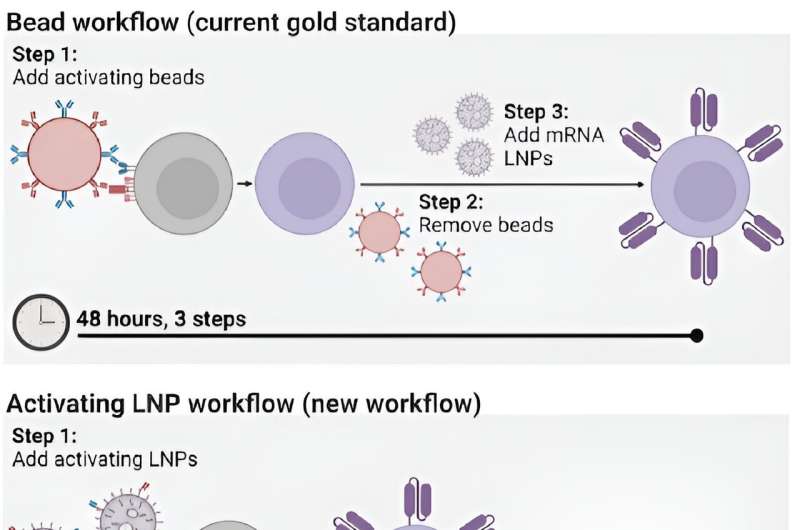
Processen för att tillverka CAR T-celler själva är dock tidskrävande och kostsam och kräver flera steg över dagar. Processen innebär att man extraherar patienternas T-celler och sedan aktiverar dem med små magnetiska pärlor, innan man ger T-cellerna genetiska instruktioner för att göra chimära antigenreceptorer (CAR), de specialiserade receptorer som hjälper T-celler att eliminera cancerceller.
Nu har Penn Engineers utvecklat en ny metod för att tillverka CAR T-celler, en som tar bara 24 timmar och kräver bara ett steg, tack vare användningen av lipidnanopartiklar (LNP), de potenta leveransfordon som spelade en avgörande roll i Moderna och Pfizer-BioNTech COVID-19-vacciner.
I en ny artikel publicerad i Advanced Materials beskriver Michael J. Mitchell, docent i bioteknik, skapandet av "aktiverande lipidnanopartiklar" (aLNPs), som kan aktivera T-celler och leverera de genetiska instruktionerna för CAR i ett enda steg, mycket förenkla tillverkningsprocessen för CAR T-celler.
"Vi ville kombinera dessa två extremt lovande forskningsområden", säger Ann Metzloff, doktorand och doktorand i Mitchell-labbet och tidningens huvudförfattare. "Hur skulle vi kunna applicera lipidnanopartiklar på CAR T-cellsterapi?"
På vissa sätt fungerar T-celler som en militär reservenhet:I tider av hälsa förblir de inaktiva, men när de upptäcker patogener, mobiliserar de, snabbt utökar sitt antal innan de vänder sig för att möta hotet. Cancer utgör en unik utmaning för denna försvarsstrategi. Eftersom cancerceller är kroppens egna, behandlar T-celler inte automatiskt cancer som farligt, därför måste man först "aktivera" T-celler och leverera cancerupptäckande CAR i CAR T-cellsterapi.
Fram till nu har det mest effektiva sättet att aktivera T-celler varit att extrahera dem från en patients blodomlopp och sedan blanda dessa celler med magnetiska pärlor fästa vid specifika antikroppar – molekyler som provocerar fram ett immunsvar. "Pärlorna är dyra", säger Metzloff. "De måste också tas bort med en magnet innan du kliniskt kan administrera T-cellerna. Men när du gör det förlorar du faktiskt många av T-cellerna också."
Gjorda huvudsakligen av lipider, samma vattenavvisande molekyler som utgör hushållsfetter som smör och olivolja, har lipidnanopartiklar visat sig vara oerhört effektiva för att leverera känsliga molekylära nyttolaster. Deras kapselliknande form kan innesluta och skydda mRNA, vilket ger instruktioner för celler att tillverka proteiner. På grund av den utbredda användningen av covid-19-vaccinerna, säger Metzloff, "Säkerheten och effekten av lipidnanopartiklar har visats i miljarder människor runt om i världen."
För att införliva LNPs i produktionen av CAR T-celler undrade Metzloff och Mitchell om det kunde vara möjligt att fästa de aktiverande antikropparna som används på de magnetiska pärlorna direkt till ytan av LNP:erna. Att använda LNP på detta sätt, trodde de, skulle kunna göra det möjligt att helt och hållet eliminera behovet av att aktivera pärlor i produktionsprocessen. "Det här är nytt", säger Metzloff, "eftersom vi använder lipidnanopartiklar inte bara för att leverera mRNA som kodar för CAR, utan också för att initiera ett fördelaktigt aktiveringstillstånd."
Under loppet av två år optimerade Metzloff noggrant utformningen av aLNP:erna. En av de främsta utmaningarna var att hitta rätt förhållande mellan en antikropp och en annan. "Det fanns många val att göra", minns Metzloff, "eftersom detta inte hade gjorts tidigare."
Genom att fästa antikropparna direkt till LNP:er kunde forskarna minska antalet steg som var involverade i processen att tillverka CAR T-celler från tre till en, och halvera tiden som krävs, från 48 timmar till bara 24 timmar. "Detta kommer förhoppningsvis att ha en transformativ effekt på processen för tillverkning av CAR T-celler", säger Mitchell. "Det tar för närvarande så mycket tid att göra dem, och därför är de inte tillgängliga för många patienter runt om i världen som behöver dem."
CAR T-celler tillverkade med hjälp av aLNP:er har ännu inte testats på människor, men i musmodeller hade CAR T-celler skapade med den process som beskrivs i artikeln en betydande effekt på leukemi, vilket minskade storleken på tumörer, och visade därmed teknikens genomförbarhet. .
Metzloff ser också ytterligare potential för aLNP. "Jag tror att aLNPs skulle kunna utforskas mer brett som en plattform för att leverera andra laster till T-celler", säger hon. "Vi demonstrerade i detta dokument en specifik klinisk tillämpning, men lipidnanopartiklar kan användas för att kapsla in många olika saker:proteiner, olika typer av mRNA. aLNP:erna har bred potentiell användbarhet för T-cellcancerterapi som helhet, utöver detta ena mRNA CAR T-cellsapplikation som vi har visat här."
Mer information: Ann E. Metzloff et al, Antigen Presenting Cell Mimetic Lipid Nanoptics for Rapid mRNA CAR T Cell Cancer Immunotherapy, Avancerade material (2024). DOI:10.1002/adma.202313226
Journalinformation: Avancerat material
Tillhandahålls av University of Pennsylvania