Åldrande befolkningar och tendensen att leda en mer stillasittande livsstil i många delar av världen tros dramatiskt öka antalet människor som lever med flera kroniska tillstånd. Dessutom fortsätter klimatförändringarna, liksom förändrade mönster i markanvändning och resor, att öka risken för infektionssjukdomar som kan uppstå och spridas lokalt och globalt.
Att kunna diagnostisera förekomsten av och förloppet av alla dessa sjukdomar utgör snabbt en växande utmaning för hälso- och sjukvårdssystemen – en utmaning som endast kan mötas med hjälp av effektiva diagnostiska tester från vårdcentralen (POC) bortom läkarmottagningen och avancerad medicinsk faciliteter.
POC-tester gav många fördelar för människor under covid-19-pandemin, men detta tillvägagångssätt måste bli tillämpbart mycket mer brett och göra det möjligt för läkare och patienter att undersöka djupare in patologiska tillstånd. Nuvarande POC-diagnostiska teknologier mäter bara en enda sjukdomsbiomarkör eller ibland flera biomarkörer som tillhör samma klass av molekyler, såsom olika RNA, proteiner eller antikroppar.
Men att mäta flera biomarkörer från olika molekylklasser skulle kunna informera mer omfattande om tillståndet en sjukdom befinner sig i, dess svårighetsgrad och progression över tid, och till och med ta hänsyn till skillnader från person till person i hur den utvecklas.
Elektrokemiska biosensorer, som omvandlar en kemisk signal i form av en biomarkör som finns i ett litet prov av biovätska, såsom blod, saliv eller urin, till en elektrisk signal som i styrka motsvarar den detekterade mängden av biomarkören, skulle kunna ge svar på många POC diagnostiska problem.
I princip kan flera sensorer för olika biomarkörmolekyler kombineras i multiplexade sensorarrayer, och, viktigare, kampen mot "bioförorening", den tidigare oundvikliga förstörelsen av elektrodytor av ospecifika biologiska molekyler som finns i prover, har blivit undvikbar genom konstruktion av tunna antifouling-beläggningar var banbrytande vid Wyss Institute vid Harvard University.
Nu har forskargruppen vid Wyss Institute, tillsammans med flera samarbetande institut i Korea, flyttat elektrokemisk diagnostisk avkänning ett kritiskt steg längre mot dess bredare tillämpning genom att utveckla en ny porös antifouling-beläggning av nanokomposit som har en tjocklek på en mikrometer – diametern på en bakterie – som är ungefär 100 gånger tjockare än tidigare beläggningar.
Beläggningens ökade tjocklek och ett konstruerat poröst nätverk inom den gjorde det möjligt att införliva mycket högre antal biomarkördetekterande prober i sensorer, och därmed upp till 17 gånger högre känslighet än tidigare klassens bästa sensorer samtidigt som de gav överlägsna antifouling-egenskaper .
I sin proof-of-concept-studie har forskarna byggt sensorer som kombinerar förmågan att detektera COVID-19-specifika nukleinsyra-, antigen- och värdantikroppsbiomarkörmål i kliniska prover med hög känslighet och specificitet. Deras resultat publiceras i Nature Communications .
"Vår nya tjocka porösa emulsionsbeläggning riktar sig direkt mot kritiska hinder som för närvarande förhindrar den utbredda användningen av elektrokemiska sensorer som centrala komponenter i omfattande POC-diagnostik för många tillstånd", säger sist-författaren och Wyss grundare Donald Ingber, M.D., Ph.D. .
"Men om man går långt utöver det kan det också öppna upp nya möjligheter för att utveckla säkrare och mer funktionella implanterbara enheter och andra övervakningssystem för hälsovård vid flera sjukdomsfronter. Att övervinna problem med biologisk förorening och känslighet är utmaningar som påverkar många av dessa ansträngningar."
Ingber är också Judah Folkman-professor i kärlbiologi vid Harvard Medical School och Boston Children's Hospital och Hansjörg Wyss professor i bioinspirerad teknik vid Harvard John A. Paulson School of Engineering and Applied Sciences.
2019 publicerade Wyss Institutes elektrokemiska sensorprojekt sitt första landmärkepapper som rapporterade om den första bottenfärgsbeläggningen med oöverträffad bioavkänningskapacitet.
I en serie kritiska uppföljningsstudier växte teamet potentialen för elektrokemisk avkänning genom att ytterligare utveckla beläggningarnas nanokemi för att göra elektroderna ännu känsligare mot biomarkörer, lägga till viktiga multiplexeringsmöjligheter och utveckla kostnadsreducerande tillverkningsmetoder.
De mest avancerade biosensorerna som teamet konstruerade i Wyss eRapid-plattform hade en uppsättning funktioner som redan möjliggör översättning av dem till vissa kliniska miljöer.
Beläggningsmetoden som teamet använde exponerade dock hela sensorchipset för nanokompositlösningen och tillät endast en relativt tunn beläggning på cirka 10 nanometer att bildas på hela sensorytan, vilket begränsade sensorernas funktionalitet på flera sätt.
Till exempel begränsade beläggningens tunna diameter den maximala mängden sond som kunde laddas in i den, vilket blir särskilt kritiskt i större multiplexade sensorer som fortfarande behöver arbeta med små provvolymer och ännu mer i ansträngningar att miniatyrisera multiplexade sensorer för deras användning i bärbara POC-diagnostikenheter.
"I denna nya studie kom vi fram till en helt ny lösning för detta problem som resulterade i en 100 gånger tjockare beläggning. Vårt nya tillvägagångssätt utnyttjar en bläckstråleutskriftsmetod som gör att vi kan applicera denna tjocka beläggning mycket lokalt på individuella sensorer element", säger tidigare Wyss Senior Scientist Pawan Jolly, Ph.D., som var avgörande för att utveckla eRapid-plattformen.
"Detta öppnar för nya möjligheter:för det första kan vi inkludera mycket större mängder av biomarkördetekterande prober i beläggningen och i framtiden kan sensorerna i komplexa arrayer adresseras individuellt genom att applicera nanokompositkemi på dem som är specifikt inriktade på specifika biomarkörmodaliteter."
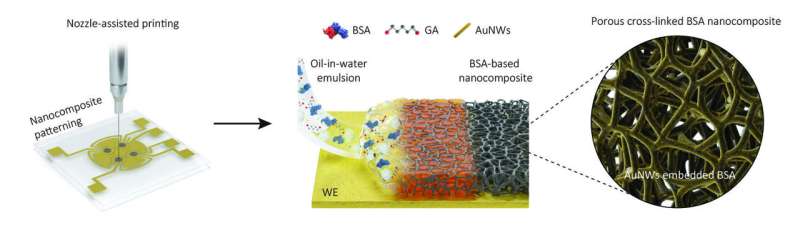
Istället för att bokstavligen doppa elektrokemiska elektroder i en beläggningslösning, som de gjorde för sin tidigare generation av sensorer, tryckte forskare ett lager av en tät olja-i-vatten-emulsion genom ett fint munstycke på elektroder. Efter att ha avdunstat de små oljebubblorna återstod en 1 mikrometer tjock beläggning på elektrodytan som bestod av tvärbundna polymera molekyler av blodproteinet albumin och innehöll sammankopplade porer och elektronledande guldnanotrådar.
"Det porösa nätverket i denna nanokompositbeläggning ökar dramatiskt ytan som kan användas för att fästa specifikt konstruerade biomarkördetekterande prober till, och som samtidigt är tillgänglig för provvätskor. Som ett resultat av detta ökar detektionskänsligheten avsevärt." förklarade förstaförfattaren Jeong-Chan Lee, Ph.D., en postdoktor i Ingbers team.
"Dessutom tillåter munstycksutskrift oss att mönstra emulsionen uteslutande på den biomarkördetekterande arbetselektroden samtidigt som den närliggande referenselektroden som finns i varje sensor hålls fri från den, vilket minskar ospecifikt elektriskt brus och förbättrar specificiteten för våra mätningar."
Teamet återupprättade en tidigare utvecklad kombination av detektionsreagenser för tre COVID-19-relaterade biomarkörer för att mönstra en sensorelektroduppsättning med deras nyutvecklade beläggningsteknik:en CRISPR-aktiverad sensor för ett SARS-CoV-2 RNA, en sensorspecifik för ett SARS-CoV-2-kapsidantigen och en sensor för en virusriktad värdantikropp.
Testad med en samling patientprover producerade den nya sensorn 3,75 till 17 gånger förbättrad detektionskänslighet jämfört med en tidigare tillverkad med samma detektionssystem och teamets bästa icke-porösa, mycket tunnare beläggning. Den skiljde även positiva från negativa prover med 100 % noggrannhet (specificitet).
"Elektrokemiska sensorer med denna nästa generations beläggning skulle vara idealiska för att övervaka virusutbrott, vaccinationssvar och förstå sambanden mellan olika biomarkörer under loppet av virusinfektioner, och i framtiden skulle de kunna användas för andra sjukdomar också." sa Lee.
Mer information: Jeong-Chan Lee et al, Mikrometertjock och porös nanokompositbeläggning för elektrokemiska sensorer med exceptionella antifouling och elektriskt ledande egenskaper, Nature Communications (2024). DOI:10.1038/s41467-024-44822-1
Journalinformation: Nature Communications
Tillhandahålls av Harvard University