I en studie publicerad i MedComm—Biomaterials and Applications Professor Changyang Gong och hans Ph.D. Student Shiyao Zhou utvecklar mekanismen för CRISPR/Cas9-systemet. CRISPR/Cas9-systemet består av Cas9-protein och enkelsträngat styrande RNA (sgRNA).
I närvaro av protospacer adjacent motiv (PAM) leder sgRNA Cas9-endonukleaset exakt till målregionerna, där det orsakar DNA-dubbelsträngsbrott (DSB), vilket resulterar i platsspecifik genomisk förändring. Endogen DNA-reparation kan äga rum efter skapandet av en DSB via två primära genomredigeringsvägar:nonhomologous end joining (NHEJ) eller homology-directed repair (HDR).
Genom att använda de biologiska egenskaperna hos Cas9 som riktar in sig på specifika DNA-sekvenser under ledning av sgRNA, har forskare vidareutvecklat geninriktningsaktivering och geninriktningsinhiberingsverktyg baserade på dCas9, kallade CRISPRa respektive CRISPRi.
I uppsatsen beskrivs egenskaperna hos tre former av CRISPR/Cas9-laster. Tre leveransformer av CRISPR/Cas9-systemet är plasmider, mRNA/sgRNA och ribonukleoproteinkomplex (RNP), som var och en har sina egna fördelar och nackdelar.
Icke desto mindre, oavsett nyttolastform, är det utmanande för CRISPR/Cas9 att penetrera målceller. Därför är det viktigt att utveckla en effektiv nanoteknikstrategi för CRISPR/Cas9-leverans.
Nanoteknologibaserade leveranstekniker för dessa tre kategorier för att behandla cancer sammanfattas i artikeln. Även om virala vektorer är de mest använda leveransvektorerna för CRISPR/Cas9-systemet, har deras tillämpningar varit begränsade på grund av nackdelar som begränsad förpackningskapacitet, hög immunogenicitet och brist på vävnadsinriktning.
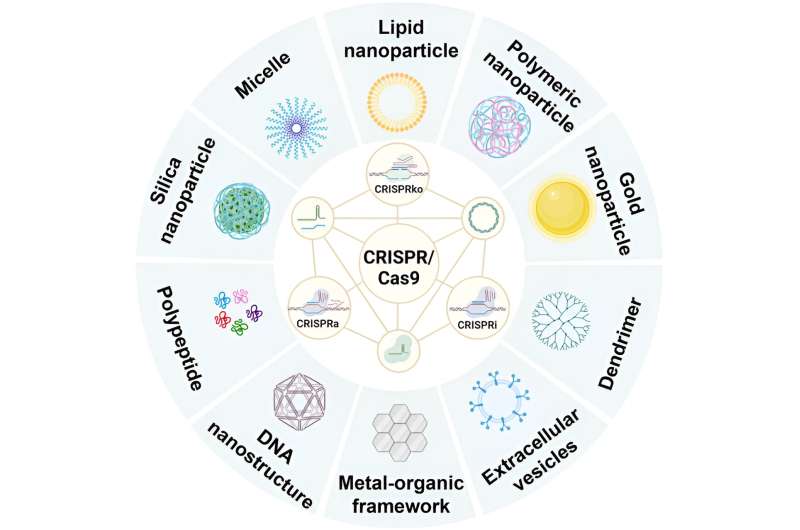
Nanobärare, avslutande katjoniska lipidbaserade nanopartiklar, katjoniska polymer/polypeptidbaserade nanopartiklar, oorganiska nanomaterial, DNA-nanostrukturer, guldbaserade nanopartiklar och exosomer eller extracellulära vesiklar, är för närvarande hoppfulla leveransmetoder för CRISPR/Cas9-system.
Med katjoniska lipidbaserade icke-virala vektorer som exempel kan katjoniska lipidvektorer ladda CRISPR/Cas9-systemet via elektrostatiska interaktioner. Dessutom kan målinriktningen av vektorer förbättras genom ligandmodifiering eller strukturell modifiering för att främja cellulärt upptag och förbättra leveranseffektiviteten.
Utlöst av specifika intracellulära miljöer eller extracellulära signaler kan responsiva nanobärare också uppnå specifik frisättning av CRISPR/Cas9 för spatiotemporalt kontrollerbar genredigering. Dessa nanoteknologibaserade smarta leveranssystem förbättrar avsevärt den tumörterapeutiska förmågan hos CRISPR/Cas9-systemet och minskar anmärkningsvärt dess effekter utanför målet.
Forskarna ger nya insikter om framtida forskningsriktningar inom den nanoteknikbaserade CRISPR/Cas9-systemleveransen. Genredigering med CRISPR/Cas9 nanoteknologi är en ny gryning inom cancerterapiområdet. Den kontinuerliga optimeringen och förbättringen av CRISPR/Cas9 leverans icke-virala vektorer visar dess stora potential för forskning och tillämpning inom området onkologisk terapi.
Ändå är majoriteten av forskningen fortfarande i sin tidiga fas. CRISPR/Cas9 har många olösta problem på molekylär nivå. Sammanfattningsvis kan personlig riktad terapi baserad på CRISPR/Cas9 vara framtiden för tumörterapi och ge nytt hopp för tumörbehandling.
Mer information: Shiyao Zhou et al, Nanoteknikbaserat CRISPR/Cas9 leveranssystem för genomredigering vid cancerbehandling, MedComm—Biomaterials and Applications (2024). DOI:10.1002/mba2.70
Tillhandahålls av Sichuan International Medical Exchange and Promotion Association