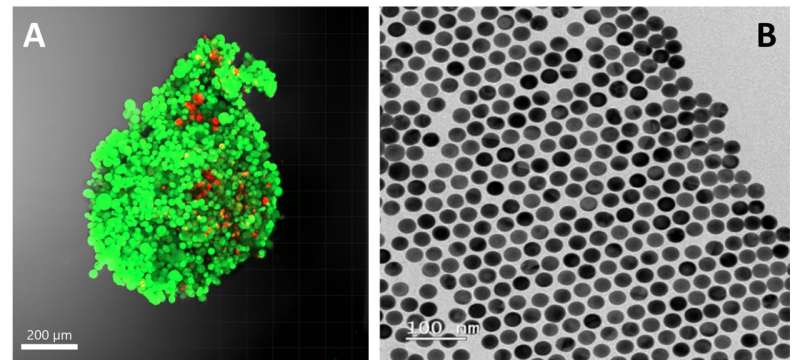
En ny studie utförd av pre-Ph.D. forskaren Pablo S. Valera visar potentialen hos ytförstärkt Raman-spektroskopi (SERS) för att utforska metaboliter som utsöndras av cancerceller i cancerforskning.
Studien, som leddes av Ikerbaskiska forskningsprofessorerna Luis Liz-Marzán (från CIC biomaGUNE) och Arkaitz Carracedo (från CIC bioGUNE) och där andra forskare från båda centra – även medlemmar av Networking Biomedical Research Center (CIBER) – har deltagit ger också värdefull information för att vägleda mer specifika experiment för att avslöja funktionen hos sådana metaboliter som utsöndras i tumörens mikromiljö eller miljö, vilket kan leda till nya terapeutiska strategier.
Verket publiceras i tidskriften Proceedings of the National Academy of Sciences .
Tumörmikromiljön är ett komplext ekosystem som bildas av interaktioner mellan tumörer och friska celler. Det är ett dynamiskt pseudoorgan som bestämmer utvecklingen och utvecklingen av cancer. Även om uppmärksamheten traditionellt har fokuserat på intercellulär kommunikation förmedlad av proteinbudbärare, har uppmärksamheten nyligen vänts mot metaboliter (eller små föreningar) som utsöndras av tumörer till det extracellulära utrymmet.
Traditionella tekniker för att spåra dessa metaboliter i komplexa cellulära sammanhang är begränsade, men ytförstärkt Raman-spektroskopi (SERS) har dykt upp som ett lovande alternativ på grund av dess enkelhet i drift.
I denna studie föreslår en SERS-baserad strategi "att undersöka metaboliter som utsöndras av tumörceller som saknar metyltioadenosinfosforylas (en vanlig genetisk händelse förknippad med dålig prognos vid olika typer av cancer, såsom bröstcancer och glioblastom)," förklarade Valera. SERS "är en spektroskopisk teknik som använder guldnanopartiklar för att detektera molekyler i en biovätska. Det är en ganska snabb teknik, där ingen förbehandling av proverna krävs", tillade han.
Med hjälp av SERS upptäckte forskarna att dessa celler utsöndrar purinmetaboliter, som kan metaboliseras av friska celler, vilket ger upphov till molekylära förändringar i överensstämmelse med cancer aggressivitet; detta förklarar omprogrammeringen, som aldrig har setts tidigare, av tumörmiljön i cancer med metyltioadenosinfosforylasundertryckning.
"Vi kunde detektera denna metabolit, inte bara i tumörceller utan även i resten av de friska cellerna som är i kontakt med tumörcellerna. Så vi upptäckte att det finns ett samband mellan tumörceller och friska celler med hjälp av detta metabolit, och att det också åstadkommer en förändring i beteendet hos friska celler så att de i viss utsträckning hjälper tumören att utvecklas, säger Valera.
Det är värt att påpeka att "att reda ut komplexiteten i sådana interaktioner hos cancerpatienter kan i sin tur bana väg för nya terapeutiska tillvägagångssätt," tillade han.
Den framgångsrika tillämpningen av SERS i denna studie visar att denna teknologi kan påskynda förmågan att snabbt fånga metaboliska interaktioner i komplexa miljöer. Faktum är att den enkla, snabba inhämtningen av signaler i SERS, tillsammans med dess höga känslighet, uppfyller kraven för att vara ett frontlinjeverktyg som sedan kan styra mer specifika analyser.
En fullständig bild av tumörmikromiljöns metaboliska status kan erhållas genom övervakning med kompletterande tekniker. Det är också viktigt att betona att en effektiv synergi mellan SERS och andra analysmetoder har visats.
Mer information: Pablo S. Valera et al, SERS-analys av cancercellsutsöndrade puriner avslöjar en unik parakrin överhörning i MTAP-bristtumörer, Proceedings of the National Academy of Sciences (2023). DOI:10.1073/pnas.2311674120. doi.org/10.1073/pnas.2311674120
Journalinformation: Proceedings of the National Academy of Sciences
Tillhandahålls av Elhuyar Fundazioa