Två olyckliga fakta om kemoterapi:Det kan skada såväl friska celler som cancerceller, och många terapeutiska mål stannar inom cancercellerna, vilket gör dem svårare att nå.
Binghamton Universitys biomedicinska ingenjörer är bland dem som forskar om användningen av cellhärledda nanovesiklar för att leverera terapeutiska medel till det inre av cancerceller med bättre noggrannhet och effektivitet. De små säckarna med proteiner, lipider och RNA som celler utsöndrar som en metod för intercellulär kommunikation skulle kunna modifieras för att bära mediciner.
"Dessa nanobärare har några utmärkta egenskaper", säger Yuan Wan, biträdande professor vid Thomas J. Watson College of Engineering and Applied Sciences institution för biomedicinsk teknik. "De kan till exempel skördas från mänskliga cellstammar, så immunsvaret är mycket lågt. Det möjliggör optimal biokompatibilitet, så de undviker immunclearance och har en förlängd blodhalveringstid. Tiden för cirkulation runt kroppen är kanske 45 sekunder, så de läkemedelsladdade nanovesiklarna kan säkert resa till tumörerna många gånger och läkemedlen har fler chanser att tas upp av cancerceller jämfört med läkemedel som fritt introduceras i kroppen.
"Stora mängder inkapslade läkemedel kan skyddas väl och hållas kvar av nanovesiklarnas lipidmembran. När cancerceller väl tar upp dessa nanovesiklar dödar höga läkemedelskoncentrationer i tumörmikromiljön effektivt cancerceller. I jämförelse kan fria läkemedel diffundera snabbt och sedan rengöras Endast en mycket liten mängd läkemedel når tumörerna, vilket gör behandlingens effektivitet mycket låg. Du kan öka dosen, men en högre dos resulterar också i hög systematisk toxicitet
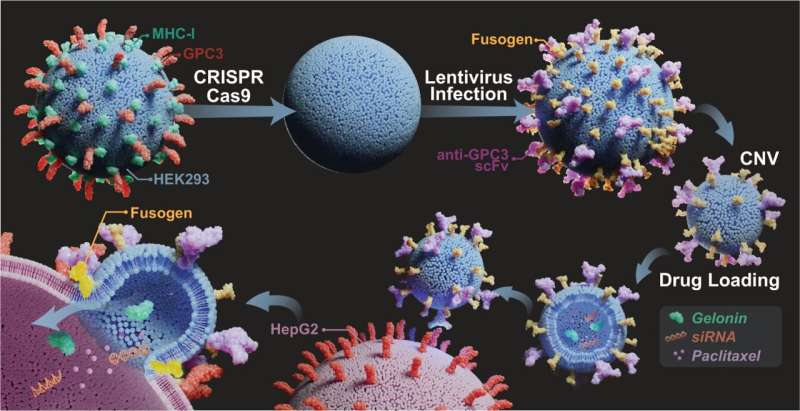
I deras nya studie, publicerad i Nature Communications , experimenterade Binghamton-teamet med inriktningsgrupper och konstruerade virala fusogener, som är proteiner som underlättar cancerinriktning och fusion av cellmembran.
Genom att identifiera överuttryckta eller cancerspecifika antigener som förekommer i maligna celler och använda inriktningsdelar och fusogen-samutrustade nanovesiklar, injiceras inkapslade läkemedel i cancerceller samtidigt som friska celler lämnas ifred.
"Människor använder i stor utsträckning nanobärare kända som polymerdekorerade liposomer, och de är redan godkända av FDA," sa Wan. "Men de är inte perfekta, eftersom de inte har någon cancerinriktad effekt och kan ha mycket allvarliga immunogenicitetsproblem [utlöser ett svar från immunsystemet]."
År 2021 genomförde Wan forskning för att testa plasmahärledda extracellulära vesiklar för att diagnostisera om ensamma lungknölar som finns i mänskliga lungor är godartade eller maligna. Andra metoder för att fastställa malignitet tar antingen för lång tid eller är mer invasiva.
Genom att utnyttja den kunskapen utnyttjar denna aktuella men separata forskning nanovesiklar så att de fungerar för oss och är specifika i vad de påverkar. Helst skulle läkare kunna förbereda dessa målgrupper och fusogen-samutrustade nanovesiklar för användning i säkrare vaccintillförsel och genteknik.
Vad som kommer härnäst, sade Wan, "Vi måste visa deras behandlingseffektivitet i stora djurmodeller och visa att vi inte behöver en stor mängd av dessa vesiklar eftersom vi kommer att ha membranfusionsfunktionen. Om du sänker antalet vesiklar och läkemedel du behöver, sänker du kostnaden för behandlingen och biverkningarna."
Mer information: Lixue Wang et al, Bioinspirerad konstruktion av fusogen och målgruppsutrustade nanovesiklar, Nature Communications (2023). DOI:10.1038/s41467-023-39181-2
Journalinformation: Nature Communications
Tillhandahålls av Binghamton University