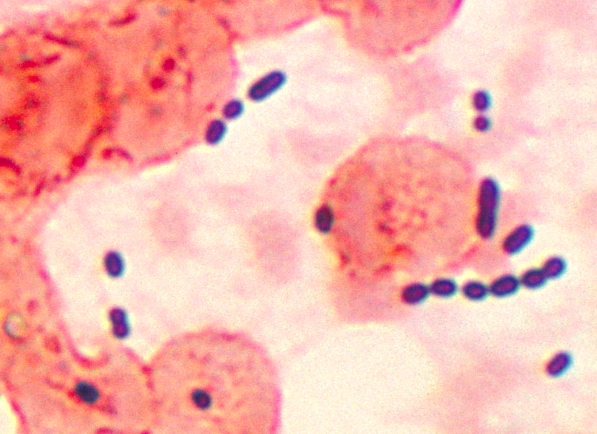
Denna mikrofotografi avslöjar kockformade Enterococcus sp. bakterier tagna från en lunginflammationspatient. Enterococcus sp. är en vanlig, grampositiv bakterie som normalt finns i tarmen och kvinnliga könsorgan. Dessa bakterier kan spridas genom fekal-oral överföring, kontakt med infekterade kroppsvätskor eller kontakt med förorenade ytor. Upphovsman:CDC/public domain
Antibiotikaresistens är ett av världens mest akuta hot mot folkhälsan. Bara i USA, tiotusentals dödsfall orsakas varje år av läkemedelsresistenta stammar av vanliga bakterier som Staphylococcus aureus och Enterococcus faecium, vilket kan orsaka praktiskt taget obehandlade sjukhusförvärvade infektioner. Farligt få nya klasser av antibiotika utvecklas för att bekämpa infektioner som har blivit resistenta mot traditionella behandlingar, och att få ut nya läkemedel på marknaden kan ta decennier.
Forskare vid UC San Francisco hanterar antibiotikaresistens med ett annat tillvägagångssätt:omforma befintliga antibiotikamolekyler för att undvika en bakteries resistensmekanismer. Genom att ta fram en uppsättning molekylära LEGO -bitar som kan ändras och sammanfogas för att bilda större molekyler, forskarna har skapat det de hoppas är den första av många "ombyggnader" av läkemedel som hade lagts på grund av antibiotikaresistens. Forskningen publicerades 23 september, 2020, i Natur.
"Målet är att återuppliva klasser av läkemedel som inte har kunnat uppnå sin fulla potential, särskilt de som redan visat sig vara säkra hos människor, "sade Ian Seiple, Ph.D., en biträdande professor vid UCSF School of Pharmacys avdelning för farmaceutisk kemi och Cardiovascular Research Institute (CVRI), och huvudförfattare på tidningen. "Om vi kan göra det, det eliminerar behovet av att ständigt komma med nya klasser av läkemedel som kan överträffa resistenta bakterier. Att designa befintliga läkemedel kan vara ett viktigt verktyg i detta arbete. "
I arbetet beskrivs i det nya Natur papper, Seiple och hans medarbetare James Fraser, Ph.D. professor vid farmaceutiska högskolans institution för bioingenjör och terapeutiska vetenskaper vid UCSF School of Pharmacy, har visat detta tillvägagångssätt med en klass av antibiotika som kallas streptograminer. Tills nyligen, streptograminer var mycket effektiva mot S. aureus -infektioner, tills bakterierna utvecklat en smart motståndsmekanism.
Streptograminer inaktiverar bakterier genom att gumma upp verken i bakteriell ribosom, vilket gör det omöjligt för bakterierna att göra proteiner. Men bakterier som är resistenta mot streptograminer producerar proteiner som kallas virginiamycin acetyltransferases (Vats), som känner igen dessa antibiotika när de kommer in i bakteriecellen. Vats tar tag i läkemedlet och inaktiverar det kemiskt innan det kan binda till ribosomen, gör det värdelöst.
Streptograminer, som de flesta andra antibiotika, härrör från naturligt förekommande antibiotika föreningar som produceras av andra organismer (vanligtvis bakterier) som sedan finjusteras för att optimera deras prestanda i människokroppen. Seiple tänkte att det också måste finnas ett sätt att göra ytterligare ändringar av läkemedelsmolekylen som skulle göra det möjligt att undvika fångst av Vat -proteinerna.
Seiple bestämde sig för att bygga nya streptograminer från grunden, snarare än att ändra befintliga strukturer. För att göra byggprocessen enklare, Qi Li, Ph.D., en postdoktor i Seiple-labbet och medförfattare på tidningen, skapat sju molekylära moduler som kan justeras efter behov för att bygga en uppsättning variationer på streptograminmolekylen.
"Detta system gör att vi kan manipulera byggstenarna på sätt som inte skulle vara möjliga i naturen, "sa Seiple." Det ger oss en effektiv väg att konstruera om dessa molekyler från grunden, och vi har mycket mer utrymme att vara kreativa med hur vi modifierar strukturerna. "
När Seiple och Li hade sina byggstenar, nästa steg var att få en molekylär uppfattning om kemin som är inblandad för att bättre förstå hur man kan modifiera och sätta ihop dessa molekylära LEGO.
För det, Seiple samarbetade med Fraser, som specialiserat sig på att skapa visuella modeller av biologiska molekyler.
"Mitt labbs bidrag var att säga, 'Nu när du har de sju bitarna, vilken av dem ska vi ändra och på vilket sätt? "sa Fraser, vars arbete med projektet stöddes av det inledande Sanghvi-Agarwal Innovation Award.
För att få svar på den frågan, Jenna Pellegrino, en doktorand i Fraser-gruppen och medförfattare till papperet, använde två kompletterande tekniker, kryo-elektronmikroskopi och röntgenkristallografi, att skapa tredimensionella bilder av läkemedlet med nära atomupplösning, liksom dess mål bakteriell ribosom, och dess fenomen, Vat -proteinet.
Med hjälp av modellerna, Li, Pellegrino, Seiple, och Fraser kunde se vilka delar av streptograminmolekylen som är väsentliga för antibiotikans funktion. Sedan var Li fritt att busa med läkemedlets icke-väsentliga regioner för att hitta modifieringar som hindrade Vats från att interagera med läkemedlet samtidigt som det låter det binda till dess ribosomala mål och inaktivera bakterien.
Teamet fann att två av de sju byggstenarna tycktes erbjuda potentiellt intressanta platser för modifiering. De gjorde variationer av läkemedlet som innehöll tweaks i dessa regioner och fann att dessa variationer hade aktivitet i dussintals stammar av patogena bakterier. Forskarna testade också sin mest lovande kandidat mot streptograminresistenta S. aureus hos infekterade möss, och fann att det var över 10 gånger mer effektivt än andra streptograminantibiotika.
Seiple påpekar att kunskapen från dessa samarbetsförsök kan tillämpas på att modifiera många andra antibiotika.
"Vi lärde oss om mekanismer som andra klasser av antibiotika använder för att binda till samma mål, "sa han." Dessutom Vi etablerade ett arbetsflöde för att använda kemi för att övervinna resistens mot antibiotika som inte har nått sin potential. "
Seiple kommer att fortsätta att förfina dessa syntetiska streptograminer och hoppas sedan kunna flytta arbetet till den privata sektorn där de nyutvecklade antibiotika kan vidareutvecklas och testas i mänskliga försök. Han och Fraser planerar att fortsätta arbeta tillsammans för att återuppliva andra antibiotika som har skrinlagts på grund av mikrobiell resistens, förfina en uppsättning verktyg som kan hjälpa forskare att ligga ett steg före bakteriell utveckling.
"Det är ett oändligt vapenlopp med bakterier, "sade Fraser." Men genom att studera de inblandade strukturerna - innan motståndet uppstår - kan vi få en uppfattning om vad de potentiella motståndsmekanismerna kommer att vara. Den insikten kommer att vara en vägledning för att göra antibiotika som bakterier inte kan motstå. "