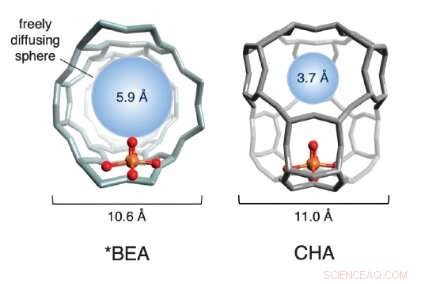
En illustration av burstrukturerna för två järnbaserade zeoliter som används i studien. De röda och guldkulorna (representerar syre och järn, respektive) utgör den aktiva webbplatsen. Buren struktur, i grått, är gjord av kisel, aluminium och syre. Den blå sfären kvantifierar storleken på den största molekylen som kan diffundera fritt in och ut ur den aktiva platsens bur (diametern på metan är ~ 4,2 Å). Upphovsman:Benjamin Snyder
Ett team av forskare från Stanford University och University of Leuven i Belgien har ytterligare belyst en spännande process som kan vara ett viktigt steg mot en metanolbränsleekonomi med mycket metan som råvara, ett framsteg som i grunden kan förändra hur världen använder naturgas.
Metanol - den enklaste alkoholen - används för att tillverka olika produkter, som färg och plast, och som tillsats till bensin. Rik på väte, metanol kan driva nya åldersbränsleceller som kan ge betydande miljöfördelar.
Om naturgas, varav metan är den primära komponenten, kan omvandlas ekonomiskt till metanol, det resulterande flytande bränslet skulle mycket lättare lagras och transporteras än naturgas och rent väte. Det skulle också avsevärt minska utsläppen av metan från bearbetningsanläggningar och rörledningar för naturgas. I dag, rymde metan, en växthusgas som är många gånger starkare än koldioxid, nästan förnekar miljöfördelarna med naturgas framför olja och kol. Teamets nya studie i den aktuella upplagan av Vetenskap är deras senaste för att främja ett lågenergimetod för att producera metanol från metan.
"Denna process använder vanliga kristaller som kallas järnzeoliter som är kända för att omvandla naturgas till metanol vid rumstemperatur, "förklarar Benjamin Snyder, som tog sin doktorsexamen vid Stanford och studerade katalysatorer för att ta upp viktiga aspekter av denna utmaning. "Men, detta är extremt utmanande kemi att uppnå på praktisk nivå, eftersom metan envist kemiskt är inert. "
När metan infunderas i porösa järnzeoliter, metanol produceras snabbt vid rumstemperatur utan extra värme eller energi som krävs. Som jämförelse, den konventionella industriella processen för att tillverka metanol från metan kräver temperaturer på 1000 ° C (1832 ° F) och extremt högt tryck.
"Det är en ekonomiskt spännande process, men det är inte så lätt. Betydande hinder förhindrar att denna process skalas upp till industriella nivåer, "sa Edward Solomon, Stanford professor i kemi och fotonvetenskap vid SLAC National Accelerator Laboratory. Solomon är seniorförfattare till den nya studien.
Hålla zeoliterna på
Tyvärr, de flesta järnzeoliter inaktiveras snabbt. Det går inte att bearbeta mer metan, processen petar ut. Forskare har varit angelägna om att studera sätt att förbättra järnzeolitets prestanda. Den nya studien, medförfattare av Hannah Rhoda, en doktorand i Stanford i oorganisk kemi, använder avancerad spektroskopi för att utforska den fysiska strukturen hos de mest lovande zeoliterna för metan-till-metanolproduktion.

Hannah Rhoda med resonans Raman spektroskopi utrustning, som skjuter in en laser i ett prov för att få vibrationsinformation från den exakta platsen som studeras. Forskare i den aktuella studien använde denna teknik för att tilldela Fe (III) -OH och Fe (III) OCH3-förgiftade platser, som belyste mekanismen. Upphovsman:Hannah Rhoda
"En nyckelfråga här är hur man får ut metanolen utan att förstöra katalysatorn, Sa Rhoda.
Väljer två attraktiva järnzeoliter, laget studerade den fysiska strukturen hos gallren runt järnet. De upptäckte att reaktiviteten varierar dramatiskt beroende på storleken på porerna i den omgivande kristallstrukturen. Teamet kallar det "burseffekten, "som inkapslande gitter liknar en bur.
Om porerna i burarna är för stora, den aktiva platsen avaktiveras efter bara en reaktionscykel och återaktiveras aldrig igen. När poröppningarna är mindre, dock, de samordnar en exakt molekylär dans mellan reaktanterna och de järnaktiva platserna - en som direkt producerar metanol och regenererar den aktiva platsen. Utnyttja denna så kallade 'bur-effekt', 'teamet kunde återaktivera 40 procent av de inaktiverade platserna upprepade gånger-ett betydande konceptuellt framsteg mot en katalytisk process i industriell skala.
"Katalytisk cykling - den kontinuerliga återaktiveringen av regenererade platser - kan en dag leda till kontinuerlig, ekonomisk metanolproduktion från naturgas, sa Snyder, nu en postdoktor vid UC-Berkeley vid Institutionen för kemi under Jeffrey R. Long.

Benjamin Snyder (till höger) och hans tidigare doktorandrådgivare, Edward Solomon, en professor i kemi vid Stanford och fotonvetenskap vid SLAC. Upphovsman:Linda A. Cicero
Detta grundläggande steg framåt i grundvetenskapen kommer att hjälpa belysa för kemister och kemiska ingenjörer processen järnzeoliter använder för att producera metanol vid rumstemperatur, men mycket arbete återstår innan en sådan process kan industrialiseras.
Nästa upp på Snyders lista:tackla att uppnå processen inte bara vid rumstemperatur utan att använda omgivande luft snarare än någon annan syrekälla, såsom lustgas som används i dessa experiment. Hanterar ett kraftfullt oxidationsmedel som syre, vilket är notoriskt svårt att kontrollera i kemiska reaktioner, kommer att vara ytterligare ett betydande hinder längs vägen.
Tills vidare, Snyder var både glad och förvånad över de illustrativa krafterna hos den sofistikerade spektroskopiska instrumenten i Salomons laboratorier som utnyttjades för denna studie. Dessa var ovärderliga för hans förståelse av kemin och de kemiska strukturerna som är involverade i metan-till-metanolprocessen.
"Det är häftigt hur du kan få en mycket kraftfull insikt på atomnivå, som burseffekten, från dessa verktyg som inte var tillgängliga för tidigare generationer av kemister, "Sa Snyder.