
Forskare producerade färgade bilder på odlingsplattor genom att använda rött, grön, och blått ljus för att kontrollera pigmentet som produceras av bakterier med "flerfärgsseende". Bilden har färgkorrigerats i Photoshop för att förbättra kontrasten. Kredit:Felix Moser
MIT-forskare har konstruerat bakterier med "flerfärgsseende" - E. coli som känner igen rött, grön, eller blått (RGB) ljus och, som svar på varje färg, uttrycker olika gener som utför olika biologiska funktioner.
För att visa upp tekniken, forskarna producerade flera färgade bilder på odlingsplattor - varav en stavar "MIT" - genom att använda RGB-ljus för att kontrollera pigmentet som produceras av bakterierna. Utanför labbet, tekniken kan också visa sig användbar för kommersiella, farmaceutisk, och andra applikationer.
E. coli är programmerad med ett protein- och enzymbaserat system, analogt med ett datorchip, med flera olika moduler för att bearbeta ljusinsläppet och producera en biologisk uteffekt. När det gäller datorer, en "sensor array" aktiveras först i närvaro av antingen rött, grön, eller blått ljus, och en "krets" bearbetar signalen. Sedan, en "resursallokator" kopplar den bearbetade informationen till "aktuatorer" som implementerar motsvarande biologiska funktion.
Tänk på den nya E. coli som mikrobiella marionetter, med färgat ljus istället för docksnören som får bakterierna att agera på ett visst sätt, säger MIT professor i biologisk teknik Chris Voigt, medförfattare till en artikel i Nature som beskriver tekniken. "Använda olika färger, vi kan kontrollera olika gener som uttrycks, " han säger.
Tidningens medförfattare är tidigare postdoktorer Jesus Fernandez-Rodriguez, Felix Moser, och Miryoung Song.
Syntetisk-biologisk innovation går samman
Under 2005, Voigt, som är meddirektör för Synthetic Biology Center vid MIT, och andra forskare banade väg för en "bakteriell kamera" genom att programmera en ljussensor till en stam av E. coli, tillsammans med en gen som producerade svart pigment. När ljus sken genom en stencil på en bakteriebelagd platta, mikroberna bildade svartvita bilder. Just då, denna bedrift krävde bara fyra gener och tre promotorer – DNA-regioner som initierar gentranskription – för att få jobbet gjort.
Nya verktyg för syntetisk biologi, såsom genomredigeringssystemet CRISPR, har dykt upp sedan dess, öppna bredare möjligheter för forskare. Till skillnad från 2005 års system, det nya RGB-systemet – det första att använda tre färger – består av 18 gener och 14 promotorer, bland annat, samt 46, 000 baspar DNA.
Men med större komplexitet kommer större utmaningar. Eftersom forskarna hade att göra med en sensoruppsättning som kunde detektera tre separata färger, till exempel, de var tvungna att inkludera i det mikrobiella programmet ett protein som förhindrar gentranskription av de två oanvända sensorerna.
När det gäller datorer, detta kallas en "NOT gate, "en krets som producerar en utsignal - i detta fall, genrepression – endast när det inte finns en signal på dess ingång. Med bakterier under rött ljus, till exempel, NOT-porten skulle släppa lös det genundertryckande proteinet på de gröna och blå sensorerna, stänga av dem.
För ungefär fem år sedan, Voigt ledde ett team som konstruerade mikrober för att svara på rött och grönt ljus. Att lägga till en tredje sensor var en stor utmaning för den nya forskningen. "Inne i cellen, alla nya proteinsensorer du lägger till stör varandra, eftersom det är alla molekyler som stöter runt cellen, och de kräver alla att hålla cellen vid liv och glad. Med varje ytterligare sensor du lägger till, som blir exponentiellt svårare, " han säger.
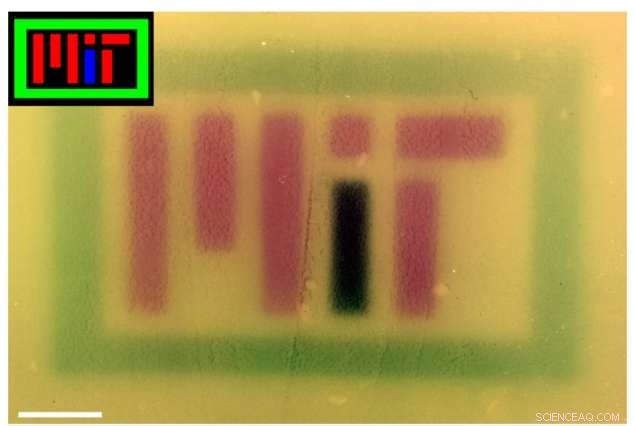
Färgade bilder (infällningar) projicerades på plattor av bakterier som innehöll RGB-systemet för att stava "MIT". Bilden har färgkorrigerats i Photoshop för att förbättra kontrasten. Kredit:Felix Moser
I det avseendet, Voigt tillägger, systemets resursfördelare, en ny funktion, fungerar också som en strömbrytare, stänga av sensorerna om alla tre slås på samtidigt, överbelasta cellen.
Ur ett genteknikperspektiv, konfigurationen med fyra delsystem var "den största effekten av detta arbete, " säger Voigt. Varje delsystem – sensoruppsättningen, kretsar, resursställdon, och ställdon – designades, byggd, och optimeras isolerat innan de sätts ihop till en slutlig struktur. Detta förenklade, modulära processer kan bana väg för mer komplex biologisk programmering i framtiden, enligt forskarna.
Generellt, Voigt ser det nya systemet som en kulmen på ett decennium av syntetisk-biologiska innovationer. "Det är en representation av var vi är för närvarande, och alla delarna som behövde gå ihop under det senaste decenniet för att skapa system av denna skala och komplexitet, " han säger.
Att göra "disco-bakterier"
För att göra de nya färgbilderna, forskarna programmerade bakterier att producera samma pigment som det röda, grön, eller blått ljus lyste på dem. I en inkubator, forskarna täckte en petriskål med bakterier som är genetiskt identiska. "Du kan tänka på det som outvecklad film, där du har petriskålen med bakterier på, " säger Voigt, "och kameran är inkubatorn."
På toppen av inkubatorn finns ett hål, där en stencilerad bild projiceras på plattan. Över tid, bakterierna växer, producerar ett enzym som producerar ett pigment som motsvarar vilken RBG-färg de än belyses av. Förutom MIT-logotypen, forskarna tog fram bilder av olika mönster, mångfärgad frukt, och tv-spelsfiguren Super Mario.
De konstruerade bakterierna kan också användas för att snabbt starta och stoppa mikrobers kemiska reaktioner i industriella fermenteringsprocesser, som används för att tillverka läkemedel och andra produkter. I dag, att kontrollera sådana kemiska reaktioner kräver att olika kemiska tillsatser dumpas i stora jäsningskärl, vilket är tidskrävande och ineffektivt.
I deras tidning, forskarna demonstrerade detta "kemikalier on-demand"-koncept i liten skala. Genom att använda CRISPR-genredigeringsverktyg, de modifierade tre gener som producerar acetat - en ibland oönskad biprodukt av olika bioprocesser - för att producera mindre av kemikalien som svar på RGB-ljus.
"Individuellt, och i kombination med varandra, ljusets olika färger minskar acetatproduktionen utan att offra biomassaackumulering, " skrev forskarna i sin uppsats.
Voigt har myntat ett roligt namn för dessa industriella mikrober. "Jag refererar till dem som 'disco-bakterier, '" han säger, "eftersom lampor i olika färger blinkar inuti jäskärlet och kontrollerar cellerna."
En framtida ansökan, Voigt tillägger, kan vara i att kontrollera celler för att bilda olika material och strukturer. Forskare, inklusive några på MIT, har börjat programmera celler för att sätta ihop till levande material som en dag skulle kunna användas för att designa solceller, självläkande material, eller diagnostiska sensorer.
"Det är fantastiskt när man tittar på världen och ser alla olika material, " säger Voigt. "Saker som cellulosa, sidenproteiner, metaller, nanotrådar, och levande material som organ – alla dessa olika saker i naturen får vi från celler som växer till olika mönster. Du kan föreställa dig att använda olika färger av ljus för att berätta för cellerna hur de ska växa som en del av att bygga det materialet."
Den här historien återpubliceras med tillstånd av MIT News (web.mit.edu/newsoffice/), en populär webbplats som täcker nyheter om MIT-forskning, innovation och undervisning.