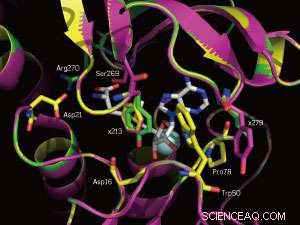
En närbild av SAM-bindningsställena för det inhemska enzymet (gult) och två mutanter (magenta och grönt). De muterade positionerna 213 och 279 är märkta. Kredit:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Organiska molekyler som innehåller en fluoratom används ofta i materialen, agrokemisk och läkemedelsindustri. Dock, syntetisering av kol-fluorbindningen använder typiskt giftiga metallkatalysatorer och kräver vattenfria förhållanden och höga temperaturer. Nu har ett internationellt team utvecklat en mildare, mer effektiv enzymbaserad metod för att skapa denna bindning.
Denna enzymatiska metod fungerar i vattenhaltiga förhållanden och vid milda temperaturer och utvecklades av ett konsortium som inkluderade forskare från A*STAR och andra institutioner. "Dessa förhållanden är verkligen mycket attraktiva, " förklarar teammedlemmen Yee Hwee Lim från A*STAR Institute of Chemical and Engineering Sciences.
Teamet använde ett av de mycket specifika fluorinasenzymerna som finns i naturen - FlA1. Dessa enzymer katalyserar bildandet av en kol-fluorbindning i S-adenosylmetionin (SAM) med användning av oorganisk fluorid via en substitutionsmekanism.
Enzymet, medan det är utmärkt att katalysera fluoreringsreaktioner med denna naturliga molekyl, fungerade inte bra på icke-naturliga molekyler. Dessutom, ansträngningar för att ändra enzymernas strukturer och, Således, funktion hade varit en kamp – fram till nu.
"Vi visade för första gången att fluorinasenzymet kan konstrueras, och att ingenjörskonsten kan förbättra sin enzymatiska aktivitet även på icke-naturliga molekyler, " säger Lim.
Teamet använde den etablerade tekniken som kallas "riktad evolution" som efterliknar naturligt urval för att utveckla enzymer så att de kan reagera bra med icke-naturliga molekyler.
"Riktad evolution har aldrig framgångsrikt tillämpats på detta enzym, tills nu, " säger Lim. "Detta är ett svårt enzym att arbeta med och vi stod inför många utmaningar inklusive problem med produktnedbrytning."
Teamet använde radiomärkningen av 5'-klor-5'-deoxiadenosin (5'-CIDA) för att visa upp sin förmåga. I denna tvåstegsreaktion, radiomärkt 5'-CIDA omvandlas till SAM, och fluorerades sedan för att bilda 5'-fluor-5'-deoxiadenosin (5'-FDA). Denna märkta 5'-FDA-produkt kan potentiellt användas för en medicinsk diagnosprocedur som kallas positronemissionstomografi (PET).
"Vi visar att en trefaldig förbättring av ett enzyms aktivitet kan öppna upp för fler applikationer, " säger Lim. "De naturliga enzymerna har använts tidigare för att försöka märka PET-medel men reaktionstiderna var långa, ibland timmar. Med hjälp av vårt enzym kunde vi göra reaktionen på 30 minuter, en mer rimlig tidslinje med tanke på att Fluor-18:s halveringstid är mindre än två timmar. "
Lims team undersöker nu hur en mutation av enzymets struktur förändrar dess interaktion med 5'-CIDA och SAM. "Jag skulle vilja engagera beräkningsbiologer för att bättre förstå mer om de mutationer som vi har gjort och hur de korrelerar med våra reaktioner."