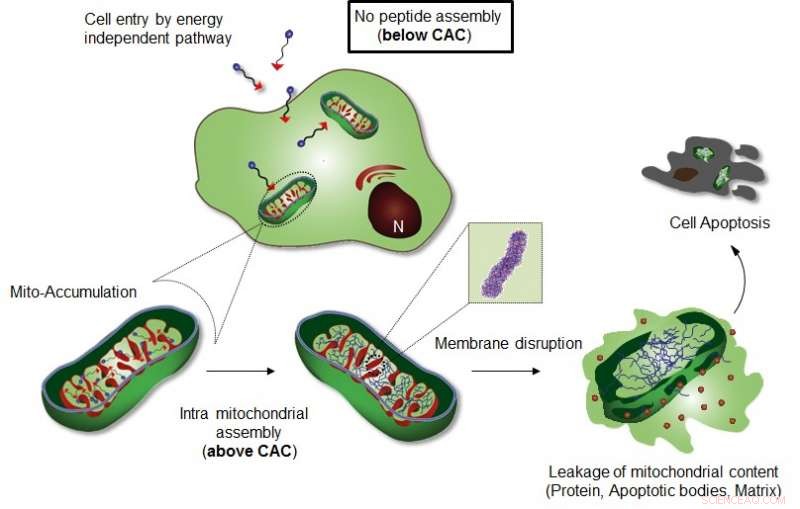
Figur visar Intra-mitokondriell montering av Mito-FF. Upphovsman:UNIST
Montering på plats av amfifila peptider med åtföljande cellulära funktioner inuti en levande cell (dvs. intracellulär montering) och deras interaktion med cellulära komponenter har framträtt som en mångsidig strategi för att kontrollera cellulärt öde. Dock, uppnå spatiotemporal kontroll (dvs. inuti cellulära organeller eller andra underfack) över självmontering av syntetiska molekyler inuti cellen är utmanande på grund av svårigheten att studera deras beteenden i den komplexa intracellulära miljön.
En ny studie, anslutet till UNIST har utvecklat en ny metod för att rikta mitokondrier hos en cancercell. Forskargruppen förväntar sig att deras studie kan bana väg för en ny generation av läkemedel mot cancer.
Denna forskning har letts av professor Ja-Hyoung Ryu i kemi vid UNIST i samarbete med Sang Kyu Kwak för energi och kemiteknik vid UNIST och professor Eunji Lee från Graduate School of Analytical Science and Technology vid Chungam National University. Resultaten av studien har visats i den 21 april upplagan av Naturkommunikation.
I studien, den gemensamma forskargruppen har infört, för första gången, den organellokaliserade självmonteringen av en peptidamfifil som en kraftfull strategi för att kontrollera cellulärt öde.
Självmontering är en jämviktsprocess mellan de enskilda byggnadsenheterna och deras aggregerade tillstånd, och koncentrationen av molekylerna bör vara över det kritiska värdet för att inducera montering (dvs. den kritiska aggregeringskoncentrationen (CAC). I levande celler, uppnå CAC krävs också för att bilda sammansättningar av enskilda molekyler, men har en begränsning eftersom cellmiljöernas kemiska komplexitet stör interaktioner mellan syntetiska byggnadsenheter.
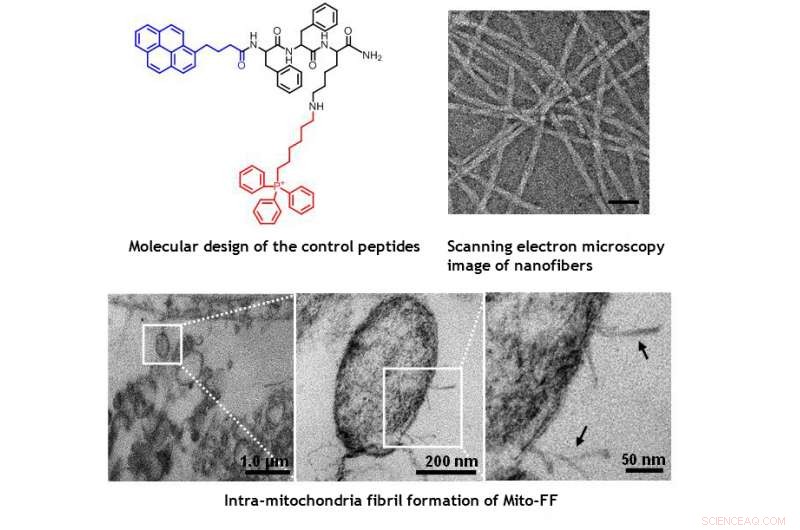
TEM-bilder av mitokondrier i HeLa-cellen som visar den morfologiska skadan som orsakas av Mito-FF. Upphovsman:UNIST
Intracellulär självmontering, Således, kräver en högre koncentration av molekylerna än CAC, vilket kan begränsa de praktiska implementeringarna av självmonterande molekyler. Transformation av molekylstrukturen från hydrofila till hydrofoba enheter inuti cellen (eller pericellulärt utrymme) genom yttre stimuli (kemisk, eller fysisk) är en kraftfull strategi för att minska CAC genom att öka benägenheten för självmontering. Dock, kemiska och fysiska stimuli (t.ex. ljus, temperatur, pH, och redox) är inte relevanta för intracellulär montering eftersom de orsakar allvarlig cellskada.
Professor Ryus forskargrupp introducerade ett specifikt cellulärt organell-lokaliseringsinducerat supramolekylärt självmonteringssystem (OLISA) kan vara en allmän strategi för att framkalla självmontering genom att höja lokala koncentrationer av de självmonterande molekylerna utan ytterligare behandling. De små molekylerna diffunderar lätt genom cellmembranet, nå till målstället (organell eller subcellulärt fack beroende på målgruppen), och sedan genomgår de självmontering inuti den riktade organellen till följd av ökad lokal koncentration. Ackumuleringen av molekyler inuti en organell som mitokondrier är ~ 500-1, 000 gånger högre än för extracellulärt utrymme.
"OLISA är en mer allmän och direkt strategi för att uppnå intracellulär montering och är helt ny, det är ett lovande tillvägagångssätt för att kontrollera det cellulära ödet som apoptos, cellproliferation etc. och är en användbar strategi för deras djupgående undersökningar, säger professor Ryu.
Designen består av mitokondrier-ackumulerande amfifil peptid (Mito-FF), som består av difenylalanin som en β-arkbildande byggsten, TPP som en mitokondriell målgrupp, och pyren som en fluorescerande sond. Mito-FF ackumulerades positivt i mitokondrier hos cancerceller på grund av den höga negativa membranpotentialen och den ökade koncentrationen fick Mito-FF att självmonteras till en fibrös struktur, medan brist på fibrillbildning observerades i normala celler. De styva Mito-FF-fibrillerna förstörde mitokondriemembranet och aktiverade den inneboende apoptotiska vägen mot cancerceller. Detta OLISA -system erbjuder ett nytt tillvägagångssätt för riktad cancerkemoterapi.
M.T. Jeena of Chemistry på UNIST, huvudförfattaren till studien förväntar sig att den nya metoden ska lägga grunden för en ny serie behandlingar som kan maximera läkningsprocessen samtidigt som biverkningar minimeras.