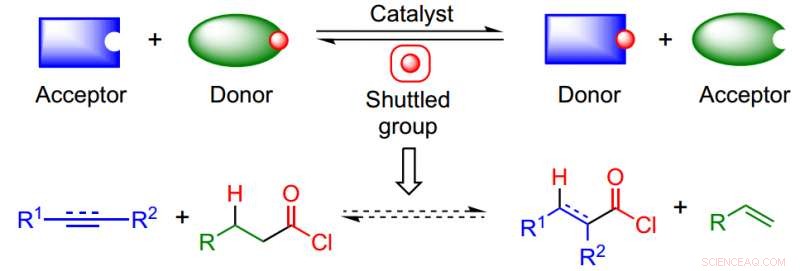
Tillvägagångssättet drar fördel av en isodesmisk skyttelkatalysprocess för att undanröja behovet av CO och HCl och övervinna den termodynamiska utmaningen att göra högreaktiva produkter. Kreditera: Naturkemi (2017). DOI:10.1038/nchem.2798
(Phys.org) —Syntesen av karboxylsyraderivat från omättade kolföreningar är viktig för att tillverka kemikalier som används i läkemedel, kosmetika, polymerer, och jordbrukskemikalier. Inom industrin utförs denna reaktion med användning av högtryckskolmonoxid tillsammans med lämplig katalysator för jobbet. Även om detta kan vara möjligt i vissa anläggningar, användningen av en giftig gas är inte genomförbar i laboratoriemiljö. Dessutom, eftersom dessa reaktioner ofta kräver en skräddarsydd katalysator, processen är begränsad till endast de substrat som arbetar med katalysatorn.
Forskare vid Max Planck -institutet har utvecklat en syntes som är mycket bredare och undviker användning av högtrycks -CO och frätande HCl -gas. Xianjie Fang, Bastien Cacherat, och Bill Morandi utvecklade en ny one-pot-syntes som ger en mängd olika karboxylsyror samt amider och tioestrar. Deras syntes använder en katalytisk skyttel som donerar CO och HCl som behövs för att producera en syrakloridmellanprodukt som sedan omvandlas till den önskade produkten. Deras arbete dyker upp i Naturkemi .
Shuttle -katalys eliminerar behovet av att använda farliga reagenser och öppnar dörren till användning av nukleofiler som inte var tillgängliga under andra reaktionsförhållanden (dvs. Reppe -karbonylering) Enligt Dr. Morandi, "Katalysatorn fungerar effektivt som en skyttel för transport av en kemisk grupp mellan en molekyl (donator) och en annan molekyl (acceptor) på ett reversibelt sätt."
I det här pappret, författarna kombinerade en syrakloriddonator och ett omättat substrat för att producera den önskade syrakloriden som sedan kan omvandlas till ett stort antal användbara funktionella grupper. Deras buss var Pd/xantphos, ett katalytiskt system som har använts i andra typer av alkenreaktioner.
Nyckeln till deras syntes var att hitta en lämplig CO- och HCl -donatormolekyl. Som en modellreaktion, Fang et al. använd cyklododecyn, en inre alkyn, och provade olika lågmolekylära alifatiska syraklorider som givarmolekyler. De bestämde att butyrylklorid var deras bästa kandidat eftersom det är billigt, har en låg molekylvikt, och har god reaktivitet.
De undersökte sedan omfattningen av deras reaktionsmekanism. Flera av de inre alkynerna som de undersökte krävde bara lite mer än en ekvivalent butyrylklorid och producerade den önskade syrakloridprodukten med bra utbyte. Vidare, eftersom reaktionen är känslig för steriska effekter, produkterna visade ett överskott av en regio -produkt och reagerade selektivt vid den distala positionen i fall där det fanns mer än ett alternativ för reaktion.
Reaktionsbetingelserna fungerade också för terminala alkyner. För denna reaktion, cirka fyra ekvivalenter butyrylklorid krävdes och den grenade isomeren isolerades från reaktionen för att ge den önskade produkten i gott utbyte. Författarna noterade att de kunde isolera alkylakrylatprodukter, som är viktiga föreningar för polymerkemi. De testade också sin reaktion med halogener, skyddade alkoholer, estrar, en keton, en nitril, och ftalimider, som alla tolererades väl i denna reaktion.
Fang et al. testade också hur denna reaktion gick med alkener. De producerade cykelsyraklorider från ansträngda alkener i bra utbyten. Terminalalkener gav motsvarande syraklorid i tillräckliga utbyten.
Nästa steg i deras procedur var att göra en en-gryts syntes genom att omvandla syrakloriden till motsvarande karboxylsyra, tioester, eller amid. De började med att titta på nukleofiler som vanligtvis är otillgängliga när de görs med tidigare rapporterade reaktioner. Dessa inkluderade en bulkyl -tertiär alkohol och tokoferol. De testade också indol och en tertiär tiol. De kunde också konjugera cinchonin och estron, två bioaktiva molekyler.
Till sist, deras en-gass syntes testades för att se om den kunde användas för att göra andra karbonylföreningar. Dessa krävde att använda olika initiala substrat och en andra katalysator. Dessa inkluderade Friedel-Crafts-reaktioner samt andra kopplingsreaktioner för att göra ketoner.
När det gäller de bredare konsekvenserna av deras arbete, Dr Morandi sa att "detta arbete visar att skyttelkatalys inte bara är en värdefull metod för att undvika användning av giftiga gaser, men också ett kraftfullt verktyg för att upptäcka ny reaktivitet som är utmanande att få annars "
© 2017 Phys.org