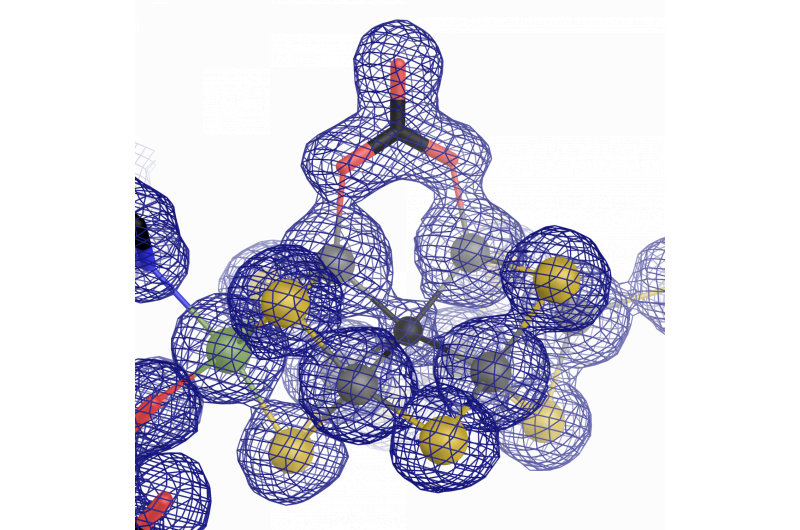
Det katalytiska centrumet för vanadinnitrogenas:en järn-vanadin-kofaktor med en ovanlig karbonatligand. Kredit:Oliver Einsle
Forskargruppen av prof. Dr. Oliver Einsle vid University of Freiburgs Institute of Biochemistry har länge undersökt hur nitrogenas fungerar. Nu introducerar gruppen den första tredimensionella strukturanalysen av enzymvarianten som innehåller vanadin. Inom ramen för att förbereda sin doktorsavhandling, Daniel Sippel lyckades producera och kristallisera vanadinnitrogenas. Med detta som sin grund, han använde röntgendiffraktionsexperiment för att belysa dess rumsliga struktur på nivån av atomär upplösning. Teamets långsiktiga mål är att göra nitrogenas biotekniskt användbart för att utveckla alternativ till industriella kemiska processer. Forskarna har presenterat sina resultat i den vetenskapliga tidskriften Naturens kemiska biologi .
Grundämnet kväve (N) är en nyckelkomponent i alla organiska makromolekyler. Dess tillgänglighet i biosfären begränsas av det faktum att den globala förekomsten av kväve till stor del är begränsad till gasen N2 i atmosfären. Stabiliteten hos N2 gör den dessutom otillgänglig för nästan alla organismer. Biologiskt tillgängligt kväve för jordbruksgödsel har tillverkats sedan 1906 med Haber-Bosch-processen. Denna industriella process omvandlar atmosfäriskt kväve (N2) till ammoniak genom en reaktion med väte. Dess betydelse är så viktig idag eftersom livsmedelsproduktion för mer än hälften av världens människor endast kan garanteras med hjälp av kvävegödselmedel. I naturen, endast ett enzym - bakteriellt nitrogenas - kan uppnå samma reaktion, men utan att släppa ut överskott av kväveföreningar i miljön, eller med andra ord, urlakning av nitrater till grundvatten. Ändå tills nu, funktionen av detta komplex, metallinnehållande enzymsystem som innehåller metall har endast delvis förklarats.
Einsles team har redan tagit ett betydande steg mot större förståelse för nitrogenas. Forskarna kunde hämma enzymets aktivitet med hjälp av den giftiga gasen kolmonoxid (CO) för att visa hur hämmaren binder till järnmolybdenkofaktorn (FeMoco). Känd som kärnan i nitrogenas, den har fått sitt namn efter de element den innehåller. FeMoco kan katalysera reaktionen av kväve och väte i en naturlig version av Haber-Bosch-processen. Samtidigt var det känt att en variant av nitrogenas innehållande vanadin snarare än molybden i sitt aktiva centrum och därför kallas FeVco också kan omvandla kolmonoxid. Produkterna från denna reaktion är reducerade kolföreningar i form av korta kolkedjor. Denna reaktion är den enzymatiska versionen av en andra betydande kemisk process - Fischer-Tropsch-syntes av kolväten som kan användas i stor skala för att syntetisera bränslen från industriella avfallsgaser, till exempel.
Vanadinnitrogenas som finns i jordbakterier kan i sin naturliga miljö utföra samma syntes som endast är möjlig i industriella processer med hjälp av extrema tryck och höga temperaturer. Haber-Bosch- och Fischer-Tropsch-processerna används årligen för att omvandla hundratals miljoner ton av respektive gaser - N2 och CO - vilket gör möjligheten till en hållbar, biologiskt alternativ av stort vetenskapligt intresse.
Under forskningsarbetet har det blev uppenbart att de flesta delar av enzymets arkitektur liknade det "original" innehållande molybden. Ändå, det finns en viktig skillnad som skiljer dem åt - atomstrukturen hos den katalytiska kofaktorn. Sippel och Einsle fann att en vanadinjon ersätter molybdenjonen i FeVco, och inkluderar en ytterligare ersättning av en överbryggande sulfidjon med en kemiskt mycket annorlunda karbonatanjon (μ-1, 3 karbonat-överbryggande ligand). Det som från början verkar vara en liten skillnad har långtgående effekter på kofaktorns geometriska och elektroniska struktur.
Forskningen finansieras av European Research Council (ERC) och German Research Foundation (DFG) inom ramen för forskarutbildningsgruppen 1976 "Functional Diversity of Cofactors" vid University of Freiburg och Priority Programme "Iron-Sulphur for Liv."