Kreditera: European Journal of Organic Chemistry
Fluorerade strukturer utgör mer än 20 procent av moderna läkemedel, men godartade och snabba fluoreringsscheman är knappa. I en studie publicerad i European Journal of Organic Chemistry , Forskare har nu kombinerat dynamisk kinetisk upplösning och nukleofil fluorering för den asymmetriska syntesen av florfenikol, ett veterinärmedicinskt antibiotikum. Efter enzymatisk upplösning av racematet, två olika fluoreringsstrategier visade sig båda effektiva och snabba. En är särskilt intressant för industriell produktion.
Fluorsubstituenter har många välkomna effekter i läkemedel. Ofta, fluorerade föreningar är mer lipofila, tränger lättare in i cellerna, och enzymer kan få svårare att bryta ner dem. Till exempel, det fluorerade antibiotikumet florfenikol är mer aktivt än tiamfenikol, till vilken den är relaterad av en terminal fluor istället för en hydroxigrupp. Florfenikol och tiamfenikol, som båda är varianter av kloramfenikol, används mot konjunktivit och luftvägssjukdomar hos nötkreatur.
Trots relevansen av fluorering, många industriella fluoreringsstrategier involverar fortfarande aggressiva och skadliga reagens. När det gäller florfenikol, inte bara är fluoreringsmedlet dyrt och frätande, men beredningen av de två stereocentralerna ger också en stor mängd avfall. Dessa problem fick Fuli Zhang från China State Institute of Pharmaceutical Industry, Shanghai, Kina, och hans kollegor, att leta efter mer miljövänliga processer. För att syntetisera florfenikol, de var tvungna att konstruera två intilliggande stereocenter av cis-1, 2-aminoalkohol och inför en terminal fluoratom.
Forskarna valde att installera fluoret som en sista, separat steg eftersom de två asymmetriska kolatomerna bekvämt kan framställas genom dynamisk kinetisk upplösning. Kinetisk upplösning innebär att två enantiomerer kan separeras enligt deras olika reaktivitet. Processen kallas "dynamisk" när de två enantiomererna kan racemisera, det är, interkonvertera. Sedan, den snabbare reagerande enantiomeren kan isoleras med maximalt utbyte.
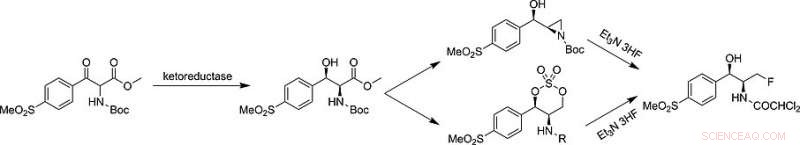
Zhang och hans kollegor designade en dynamisk reduktiv kinetisk upplösning med användning av ketoreduktasenzymer som biokatalysatorer och glukos som hydridkälla. Efter att ha etablerat de två stereocentra genom denna bioenzymatiska väg, de undersökte möjliga fluoreringsreaktioner. Två vägar för nukleofil fluorering visade sig vara särskilt övertygande, och båda vägarna använder aminhydrofluorid som fluoreringsreagens, som är mild och selektiv och kan hanteras i glasutrustning.
För industriell tillverkning, författarna har också en favorit. Vägen som involverade en cyklisk sulfatintermediär konkurrerade ut den andra som innehöll en intermediär aziridin, en treledad kvävehaltig ring. Den kemo-enzymatiska sulfatvägen producerade florfenikol i endast fem steg och visade högt utbyte och flexibilitet samt acceptabel miljö- och hälsosäkerhet. Nästa steg kommer att vara ytterligare utforskning av reduktasenzymer i andra dynamiska bioreduktionssynteser, anmärker författarna.