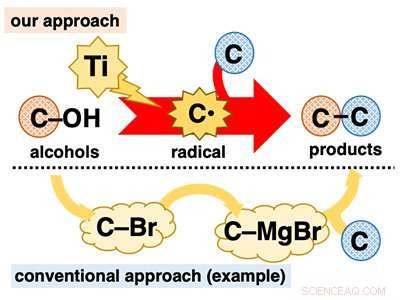
Direkt användning av alkoholer för C-C-bindningsreaktioner. Kredit:Kanazawa University
Alkoholer spelar en avgörande roll för organisk syntes eftersom de är allestädes närvarande och kan användas i en mängd väletablerade transformationer. Dock, i C-C-bindningsreaktioner, trots att det är centralt för organisk syntes, alkoholer används oftast på ett indirekt sätt. Många alkoholbaserade reaktioner kräver tråkig förvandling av hydroxigruppen (C-OH) till andra funktionella grupper, såsom halogener (t.ex. C-Br) före C-C-bindningsbildning (Figur 1).
Utvecklingen av enstegs-C-C-bindningsbildningsreaktioner med användning av alkoholer är mycket önskvärd eftersom den inser applicering av allestädes närvarande material utan bördan av ett flerstegsförfarande. Ett sätt att uppnå detta mål är att direkt omvandla alkoholer till kända reaktiva mellanprodukter som omedelbart genomgår C-C-bindningsreaktioner. Vi föreställde oss att vi skulle kunna uppnå detta med lågvärdiga titanreagenser. Lågvalent titan är en enelektronreduktant och en mycket oxofil art. På grund av dessa funktioner, det förväntas att lågvalent titan kan extrahera en syreatom från alkohol, klyvning av C-O-bindningen i en en-elektronreduktion för att generera motsvarande kolradikal (C*). Kolradikalen är en extremt reaktiv mellanprodukt som lätt genomgår olika reaktioner, inklusive C-C-bindningsbildning.
Resultat
Behandling av 2-naftalenmetanol med ett lågvärdigt titanreagens gav en blandning av två C-O-klyvda produkter från hydrering och dimerisering (Figur 2). Dessa reaktioner i sig var inte särskilt användbara; dock, de var båda bevis på genereringen av bensylradikalarter. Med detta preliminära resultat, vi förväntade oss att tillsats av radikalfångande medel skulle ge kopplingsprodukterna mellan bensylradikalen och infångningsmedlen, avbryta hydrerings- och dimeriseringsreaktionerna. Verkligen, tillsatsen av akrylnitril som ett fångsmedel gav kopplingsprodukten mellan bensylradikalen och akrylnitril som den dominerande produkten.
Det bästa resultatet erhölls när det lågvärdiga titanreagenset framställdes av TiCl4(kollidin) och manganpulver. Denna alkoholbaserade direkta C-C-bindningsbildningsreaktion applicerades framgångsrikt på en serie bensylalkoholderivat. Anmärkningsvärt, både bensylalkoholer med elektrondonerande och -avdragande substituenter på den aromatiska ringen var lämpliga för denna reaktion. Vidare, förutom primära alkoholer, sekundära och tertiära alkoholer var också lämpliga trots den avsevärda ökningen av steriskt hinder. Flera elektrondefekta alkener förutom akrylnitril var också bra reaktanter. När det gäller det praktiska, denna reaktion är kostnadseffektiv och lätt att genomföra, åtminstone i laboratorieskala. TiCl 4 (kollidin) är stabil under lagring, tolerant mot kort exponering för luft, och kostar bara cirka 10 JPY/mmol.
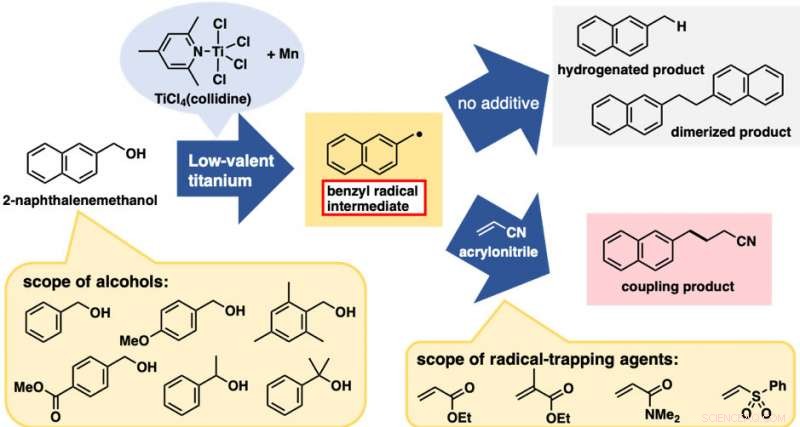
Alkoholbaserade direktradikala C-C-bindningsbildningsreaktioner. Övre pil:reaktioner utan fångsmedel. Nedre pil:reaktioner med radikalfångande medel (elektronbristande alkener). Upphovsman:Kanazawa University
Betydelse och framtidsutsikter
Betydelsen av denna metod är att den möjliggör direkt användning av alkoholer som kolradikalekvivalenter. Vi har kopplat allestädes närvarande alkoholer med ackumulerad kunskap om radikala reaktioner. Vi tror att detta arbete kommer att föranleda forskning om andra alkoholbaserade radikala reaktioner inom en snar framtid.