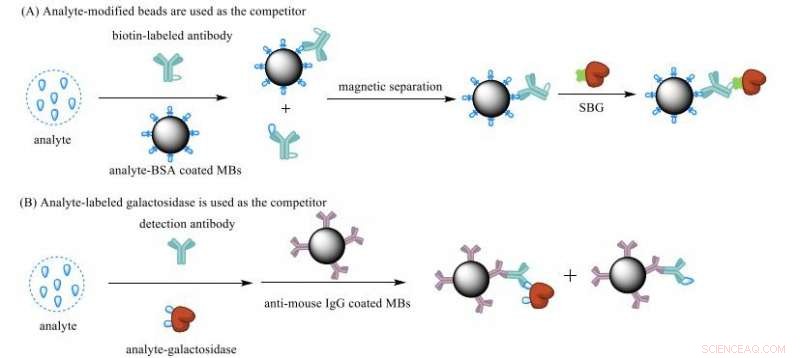
Schematisk illustration av kompetitiva Simoa-analyser med användning av analytmodifierade MBs (A) och analytmärkt β-galaktosidas som konkurrent (B). Kredit:(c) Journal of the American Chemical Society (2018). DOI:10.1021/jacs.8b11185
När medicinsk vetenskap har kommit att förstå att människokroppen styrs på molekylär nivå av olika proteiner, hormoner, läkemedel, och andra ämnen, teknologier har utvecklats för att upptäcka nivåer av dessa molekyler för att övervaka hälsa och diagnostisera sjukdomar. Dock, många av dessa molekyler är så små att de inte kan detekteras med de mest allmänt tillgängliga analysteknikerna, lämnar frågor om viktiga ämnen som aminosyror, sockerarter, och lipider i stort sett obesvarade.
Nu, forskare vid Wyss Institute for Biologically Inspired Engineering vid Harvard University och Brigham and Women's Hospital (BWH) har skapat en ny typ av immunanalys som kan detektera små molekyler med 50 gånger större känslighet än konventionella detektionsmetoder, och kan enkelt integreras i befintliga diagnostiska plattformar. Forskningen beskrivs i Journal of the American Chemical Society .
"Den förbättrade analytiska känsligheten hos vår analys möjliggör mätningar av små molekyler vid extremt låga koncentrationer, och öppnar ett fönster till biologiska fenomen som tidigare var oåtkomliga, " sa seniorförfattaren David Walt, Ph.D., en kärnfakultetsmedlem vid Wyss Institute som också är Hansjörg Wyss professor i biologiskt inspirerad teknik vid Harvard Medical School (HMS) och professor i patologi vid BWH, samt en HHMI-professor.
Det nya tillvägagångssättet är baserat på en typ av analys som kallas en konkurrenskraftig immunanalys, där en känd mängd av en märkt molekyl av intresse och ett prov med en okänd mängd av molekylen båda läggs till en rad antikroppar till vilka de binder. De märkta och omärkta molekylerna "tävlar" sedan om samma antikroppsbindningsställen. Genom att analysera mängden av den märkta molekylen av intresse som är bunden till antikropparna jämfört med det totala antalet tillgängliga antikroppsställen, det är möjligt att dra slutsatsen att de återstående platserna är bundna av den omärkta molekylen från provet, så att koncentrationen av den molekylen kan bestämmas.
Forskarna skapade två typer av konkurrenskraftiga immunanalyser som använde lite olika metoder för att fånga små molekyler av intresse, baserat på Simoa-systemet från Quanterix. Den första metoden använder magnetiska mikropärlor belagda med målmolekylen som konkurrent, medan den andra metoden fäster målmolekylen till enzymet beta-galaktosidas, som sedan binder till de magnetiska pärlorna för att bilda konkurrentkomplexet. Efter att pärlan/antikroppsblandningarna tillåts blandas med ett prov som innehåller en okänd mängd av målmolekylen, pärlorna sköljs för att ta bort eventuella obundna molekyler och läggs sedan till en Simoa-skiva som innehåller tusentals mikrobrunnar, som var och en kan hålla en pärla bunden till en målmolekyl. En reaktion äger sedan rum som gör att varje brunn som innehåller en pärla med den märkta målmolekylen fluorescerar. Ju färre antal fluorescerande brunnar, ju färre märkta målmolekyler är bundna till pärlorna, och därmed desto större koncentration av den omärkta målmolekylen som finns i provet.
Två små molekyler som är viktiga för normal mänsklig kroppsfunktion analyserades:kortisol och PGE2. Kortisol används ofta för att utvärdera binjurens funktion, hypofys, och hypotalamus körtlar, medan PGE2 är en hormonliknande prostaglandinmolekyl som påverkar inflammation, fertilitet, och immunfunktion. De nya konkurrerande metoderna kunde detektera sina mål med upp till 50 gånger större känslighet än en konventionell ELISA (enzymkopplad immunosorbentanalys), inom ungefär en timme.
"Vår plan är att använda denna metod i diagnostik för förbättrad upptäckt av hormoner i blodprover, " sa första författaren Xu Wang, Ph.D., en postdoktor vid BWH och Wyss Institute. "Vi arbetar med att försöka kommersialisera denna teknik för snabb detektering av små molekyler för en mängd olika kliniska och miljömässiga tillämpningar."
"Walt-teamet fortsätter att driva på området för diagnostik med detta framsteg. Genom att känna av molekyler som tidigare inte kunde detekteras inom en timme, de öppnar helt nya metoder för diagnostik och klinisk övervakning som avsevärt borde förbättra människors hälsa. Det är just den typ av translationell innovation vi hoppas möjliggöra och stärka vid Wyss Institute, " sa Wyss Institutes grundare Donald Ingber, M.D., Ph.D., som också är Judah Folkman professor i vaskulär biologi vid HMS och Vascular Biology Program vid Boston Children's Hospital, samt professor i bioteknik vid Harvards School of Engineering and Applied Sciences (SEAS).