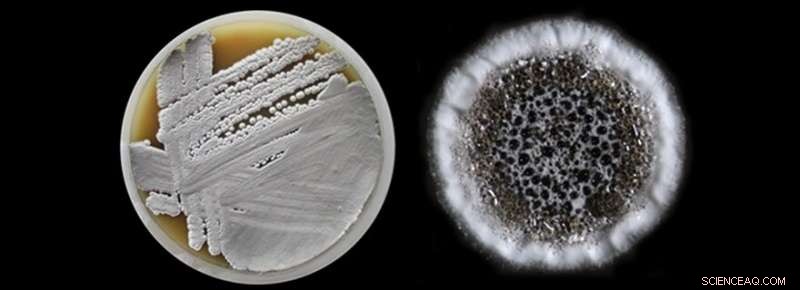
Näringsjord med en producentstam av Streptomyces tillsammans med införandet av en enda koloni. Kredit:Leiden University
Ökad resistens och brist på nya antibiotika är ett allvarligt problem för folkhälsan. Mot denna bakgrund, Gilles van Wezel från Institute of Biology Leiden letar efter nya läkemedel. Tillsammans med tidigare Ph.D. student Changsheng Wu och hans kollegor upptäckte det speciella antibiotikumet lugdunomycin, som de döpte efter Leiden. Upptäckten publicerades nyligen i tidskriften Angewandte Chemie .
Utmattad källa
"Det förutspås att år 2050 kommer cirka 10 miljoner människor världen över att dö av konsekvenserna av antibiotikaresistens, " säger Van Wezel. "Det är lika många som på grund av cancer. Vi står inför en negativ trend där fler och fler bakterier blir resistenta, ofta till flera antibiotika, samtidigt som allt färre nya läkemedel kommer ut på marknaden. Vi vill hitta lösningar på detta." Van Wezel forskar om bakterien Streptomyces. Detta släkte lever i jorden och producerar inte mindre än två tredjedelar av all antibiotika. Eftersom de har använts och screenats så länge, läkemedelsindustrin trodde att allt som kunde erhållas från dessa bakterier redan hade upptäckts. Källan verkade utmattad, säger Van Wezel. Men det visade sig inte vara fallet trots allt.
Sömnantibiotika
I början av 2000-talet, DNA-sekvensering tog fart:en teknik för att visualisera och analysera hela DNA från organismer. "På detta sätt kunde vi också titta på DNA från antibiotikaproducerande bakterier. Sedan visade det sig att de hade mycket mer potential än vi tidigare trodde var möjligt! Modellstammen Streptomyces coelicolor, som producerar himmelsblå (coelicolor på latin) antibiotika, är ett bra exempel. Bakterien producerar så många som fyra olika arter. Tusentals forskare har arbetat med denna stam i femtio år, så man trodde att det inte fanns så mycket mer att hämta. Dock, när stammens fullständiga DNA publicerades 2002, det visade sig att bakteriernas DNA innehåller mycket fler recept på antibiotika än bara för antibiotika de producerar i labbet. Dessa kallas sömnantibiotika.

Strukturen av antibiotikumet lugdunomycin. Kredit:Leiden University
Spara energi
Det tar mycket energi för en bakterie att tillverka antibiotika, " förklarar Van Wezel. "Det är därför de inte gör det när det inte är nödvändigt." Därför, i laboratoriet tillverkar bakterier färre antibiotika än i jorden. Helt enkelt för att labbet saknar nödvändiga ekologiska förutsättningar. "Eller, med andra ord:i jorden, det finns fler fiender mot vilka bakterier behöver antibiotika."
Leiden antibiotika
Antibiotikumet som upptäcktes av Wu, Van Wezel och co-promotor Young Hae Choi är också ett sovande antibiotikum, producerad av en ännu okänd Streptomyces-bakterie från Qinlingbergen i Kina. De kallade det lugdunomycin, efter det latinska namnet för Leiden (Lugdunum batavorum). "Wu har tittat på en stam som inte producerade något vid första anblicken. Men efter att ha imiterat olika odlingsförhållanden, vi såg ändå biologisk aktivitet här. Detta ledde till upptäckten av en kemisk molekyl med en oförutsedd komplex struktur!" Lugdunomycin härrör från en välkänd familj av molekyler med huvudsakligen antitumöraktivitet men genomgick så stora modifieringar att det inte längre ser ut som det. tre extra ringar får det att se ut som en helikopter, " säger Van Wezel. "Vi har aldrig sett det här förut, men det kommer säkert att förekomma oftare i naturen. Men i så små mängder att de måste ha förbisetts tills nu."
Upptäckten av en så radikalt annorlunda kemisk struktur är sällsynt. Nu när Wu, Choi och Van Wezel har publicerat strukturen för lugdunomycin, nästa utmaning är:att få Streptomyces att producera mer av det. De måste också undersöka den exakta aktiviteten hos molekylen, och om det faktiskt är kliniskt tillämpbart. Eventuellt, Leiden-antibiotikumet kommer att kunna fungera som riktig medicin i framtiden. För detta ändamål, Van Wezel startade ett uppföljningsprojekt inom NACTAR-programmet inom NWO-domänen för tillämpad och teknisk vetenskap (TTW). I detta program, forskare och industri samarbetar för att utveckla nya antibiotika. "Tills vidare, åtminstone, vi har upptäckt denna speciella molekyl, vilket är väldigt spännande. Jag tror inte att vi snabbt kommer att upptäcka en annan molekyl med en så spektakulär struktur."