
Solljus experiment. Reaktionerna kan utföras med hjälp av ljuset från solen i en enkel glaskolv. Upphovsman:J. Waser/EPFL
Att upptäcka nya biologiska mål är en kritisk del av vår pågående kamp mot sjukdomar. Över åren, forskare har gjort imponerande framsteg mot förståelsen av biologiska system, ständigt identifiera nya mål. Den strukturella mångfalden av dessa mål kräver ett brett spektrum av olika terapeutiska medel.
"Små syntetiska molekyler är fortfarande viktiga aktörer, men biomolekyler som peptider, proteiner och oligonukleotider har blivit ett viktigt forskningsområde, "säger professor Jérôme Waser, chef för EPFL:s laboratorium för katalys och organisk syntes. Peptider är särskilt intressanta, med cirka 140 utvärderade i kliniska prövningar 2015. Men peptider är ofta inte stabila i blodet och kan inte tränga igenom celler väl, som båda minskar deras potentiella användning som droger.
En lösning för att övervinna dessa svårigheter är att kemiskt modifiera peptidernas naturliga struktur, en process som kallas "funktionalisering". Inom kemi, en molekyl "funktionaliseras" genom att tillsätta kemiska grupper till den, vilket ger den nya funktioner, Förmågor, eller fastigheter, såsom ökad stabilitet i människokroppen. Dock, funktionalisering av peptider är svårt, på grund av deras komplexa struktur.
"Den främsta orsaken är bristen på selektivitet när du försöker modifiera en peptid:den innehåller många positioner som reagerar med kemikalier, resulterar i värdelösa blandningar, "förklarar Waser." Därför, metoder som möjliggör selektiv funktionalisering av en enda position i peptider är aktivt eftertraktade för att få tillgång till mer effektiva myrstabila peptidbaserade läkemedel. "
Detta är vad Waser's lab nu har uppnått, med hjälp av "EBX -reagenser" - en klass av mycket reaktiva organiska föreningar som utvecklats av gruppen och nu är kommersiellt tillgängliga. Med dessa reagenser, forskarna konverterade den C-terminala karboxylsyran av peptider till en kol-kol trippelbindning-en alkyn (i kemisk jargong en "dekarboxylativ alkynylering"). Alkyndelen är en mycket värdefull funktionell grupp som kan användas för att ytterligare modifiera peptiderna. Det har använts i stor utsträckning vid upptäckt av läkemedel, materialvetenskap och kemisk biologi.
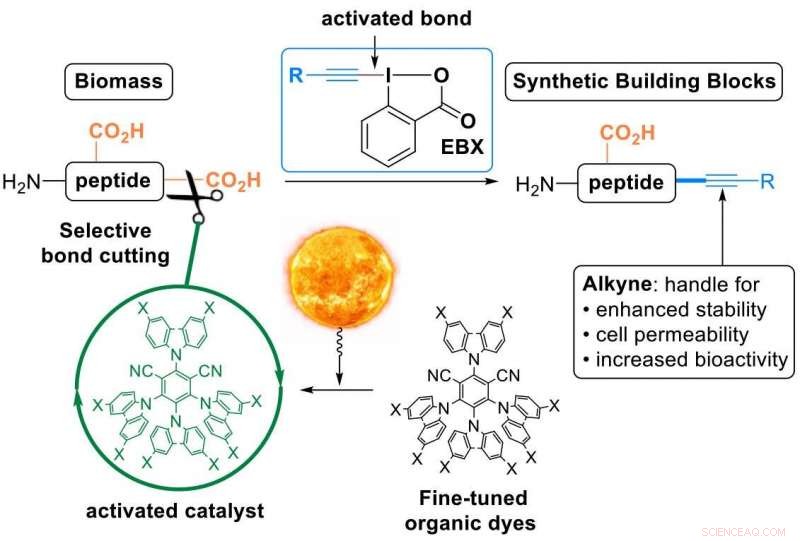
Att överbrygga den naturliga och den syntetiska världen i ett steg:Modifiering av peptider med hjälp av organiska färgämnen som exciteras med synligt ljus och EBX-reagenser. Upphovsman:J. Waser/EPFL
Peptider reagerar inte spontant med EBX -reagenser, så forskarna var tvungna att använda en katalysator. För att aktivera den, forskarna vände sig mot ljus eller, i mer tekniska termer, "fotoredoxkatalys":synligt ljus absorberas av katalysatorn, som sedan selektivt aktiverar en bindning i de reagerande molekylerna. "Att använda ljus som en förnybar energikälla för att utföra organiska reaktioner möjliggör en tidsmässig och rumslig upplösning med mycket milda reaktionsförhållanden, säger Waser.
Forskarna gjorde två innovationer:För det första, de utformade nya finjusterade organiska färgämnen som fotoredoxkatalysatorer. Detta var viktigt eftersom ljusmedierade reaktioner vanligtvis baseras på sällsynta, giftiga och dyra övergångsmetallkatalysatorer.
Andra, forskarna uppnådde denna första "dekarboxylativa alkynylering" på nativa peptider. Detta är en särskilt attraktiv omvandling av en naturlig förening till ett syntetiskt derivat i ett steg eftersom det erbjuder en plattform för att modifiera de fysikaliska och kemiska egenskaperna hos peptiden genom en enda, lätt att utföra manipulation (alla "ingredienser" behöver bara blandas ihop och låt stå i naturligt ljus).
Metoden kan användas med nästan alla aminosyror som finns på peptiderna, med bibehållen fullständig selektivitet mot den C-terminala positionen över peptidsidokedjorna.
Med sin nya metod, forskarna kunde också få derivat från den värdefulla bioaktiva peptiden GRGDNP som hindrar celler från att binda sig till fibronektin, en viktig process vid vasodilatation av blodkärl, vilket kan vara mycket användbart i studien av hjärt -kärlsjukdom.