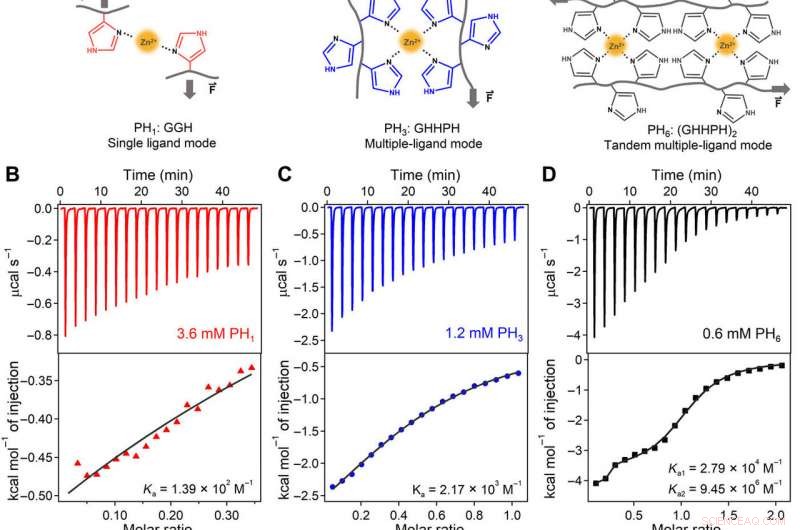
Kooperativitetsteknik, bindningskonstanter, och molekylär mekanism för metalljonens koordinationsinteraktioner på molekylär nivå för lastbärande. (A) Metalljonkoordinationskomplexen bildade av enkla ligander (PH1, vänster) är dynamiska och svaga. När man bildar ett metallkeleringsställe gjord av flera ligander (PH3, mitten), metalljonbindningen blir mycket starkare och mindre dynamisk än den för enstaka ligander. Vidare, när man arrangerar två metallkeleringsställen i tandem (PH6, höger), den bindande affiniteten, mekanisk styrka, och associationshastigheten kan förbättras på grund av samverkan mellan de två platserna. (B till D) ITC -titreringsdata för PH1 (vänster), PH3 (mitten), och PH1 (höger) peptider med ZnCl2 i 1 M tris buffert (pH 7,60, innehållande 300 mM KCl) vid 25°C. (E) Zn2+-bindande konstanter (Ka) för PH3 och muterade PH3-peptider. De muterade aminosyrorna är markerade i rött. Felstaplarna representerar anpassningsfelen. (F) Zn2+-bindande konstanter för PH6 och muterade PH6-peptider. Vänster och höger panel motsvarar Ka1 och Ka2 för de två bindningsställena för PH6. Endast PH6- och (GHHGH) 2 -peptider uppvisade två bindningskonstanter. Resten av peptiderna visade singelställsbindningsegenskaper. Felstaplarna representerar passningsfelen. (G till J) CD-spektra av (G) PH1:GGH; (H) PH3:GHHPH; (I) PH6:(GHHPH)2; och (J) (GHHGH)2-peptider i frånvaro och närvaro av Zn2+-joner. Det relativa innehållet av PPII-strukturer för PH1 och PH3 är 9,6 och 34,2 % baserat på höjden på den stora CD-toppen vid 205 nm, förutsatt att PH6-Zn2+ -komplexet uppvisar 100% PPII-spiralformad struktur. (K) Schematisk illustration av den kooperativa Zn2+-bindande mekanismen för PH6. Den konformationella förändringen av det första koordinationsstället leder till strukturella förändringar av det andra till en konformation som mer gynnar Zn2+-bindning. N/A, inte tillämpbar. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Belastande vävnader som muskler och brosk uppvisar vanligtvis hög elasticitet, seghet och snabb återhämtning. Dock, Att kombinera sådana mekaniska egenskaper i labbet för att bygga syntetiska biomaterial är i grunden utmanande. I en ny studie nu publicerad på Vetenskapens framsteg , Wenxu Sun och ett forskarlag i fysik, ingenjörsmekanik och smarta enheter i Kina, utvecklat en stark, tuff och snabbt återhämtande hydrogel. Teamet konstruerade materialet med hjälp av tvärbindare med samverkande dynamiska interaktioner. De designade en histidinrik dekapeptid (10 aminosyror kedja) innehållande två tandem (på varandra följande) zink (Zn) bindande motiv för att underlätta termodynamisk stabilitet, starkare bindningsstyrka och snabbare bindningshastighet för konstruktionen, jämfört med enkelbindande proteinmotiv eller isolerade ligandproteiner. De konstruerade hybridnätverkshydrogelerna med peptidzinkkomplexet uppvisade hög stabilitet, seghet och snabb återhämtning på några sekunder. Forskargruppen förväntar sig att byggnadsställningarna effektivt ska hantera lastbärande vävnadstekniska tillämpningar och fungera som byggstenar för mjuk robotik. De nya resultaten ger en allmän väg för att ställa in mekaniska och dynamiska egenskaper hos hydrogeler på molekylär nivå.
När vi går, våra muskler, brosk och senor är föremål för betydande mekaniska belastningar, men biologiska vävnader kan återhämta sig snabbt för att fungera tillförlitligt under många mekaniska cykler. Bioingenjörer har utforskat mjuka hydrogeler med muskelliknande mekaniska egenskaper som biomekaniska ställdon, syntetiskt brosk, konstgjorda muskler, jonisk hud och i mjuk robotik. De har ägnat många ansträngningar för att förbättra den mekaniska styrkan och segheten hos hydrogeler genom att introducera speciella energiavledningsmekanismer. Snabb återhämtning är också en unik egenskap för bärande mjukvävnad, förutom mekanisk styrka och seghet, men syntetiska hydrogeler saknar fortfarande en mekanism för snabb återhämtning. Till exempel, traditionella dubbelnätverk (DN) eller hybridnätverk (HN) hydrogeler med korta polymerkedjor som offernätverk kan vanligtvis inte återhämta sig snart - ofta tar det några minuter till dagar.
Styrkan hos en hydrogel beror på livslängden för dess tvärbindare, där långsam bindnings-/avbindningskinetik leder till starka hydrogeler, medan snabba växelkurser ger mjuka. För att erhålla hög hållfasthet och seghet måste tvärbindarna vara långsamma, men för att uppnå snabb återhämtning, tvärbindarna måste vara dynamiska med höga associerings- och dissociationshastigheter. För att övervinna denna motsägelse, naturligt förekommande lastbärande material har använt samverkan av svaga interaktioner. I det här arbetet, Sun et al. liknande manipulerade hybridnätverk (HN) hydrogeler med ett specifikt utformat peptid-metallkomplex som fysisk tvärbindare. Teamet bildade effektiva metallbindningsställen i en peptidsekvens för att konstruera hydrogeler med de nödvändiga egenskaperna.
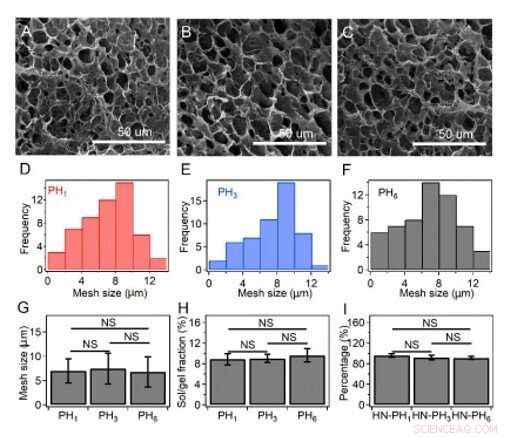
Maskstorlek, sol/gelfraktioner, och den faktiska procenten av peptider som införlivas i hydrogelnätet. (A-C) SEM-bilder av HN-PH1-gelen (A), HN-PH3-gelen (B) och HN-PH3-gelen (C) innan Zn2+-joner tillsattes. (D-F) Maskstorleksfördelningar för HNPH1-gelen (D), HN-PH3-gel (E) och HN-PH6-gel (F) uppskattade från SEM-bilderna med hjälp av programvaran ImageJ. (G) Genomsnittlig maskstorlek för HN-PHn-geler i frånvaro av Zn2+-joner. (H) Sol/gel-fraktioner av olika HN-PHn-geler före tillsats av zink. (I) Procentandelen peptider som införlivas i hydrogelnätverket. De initiala peptidkoncentrationerna var 0,3 M, 0,10 M, och 0,05 M för PH1, PH3, och PH6, respektive. Procentandelen av peptiderna som införlivades i hydrogelerna var liknande, som uppskattas genom att subtrahera fraktionen av eluerade peptider från den totala mängden som används. Felstaplar indikerar medelvärdet ± S.D. NS:p> 0,05. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Teamet designade först tre korta histidinrika peptider (HR-peptider) som ligander för att binda med zinkjoner (Zn 2+ ) och konstruera HN -hydrogeler. De betecknade peptidsekvenserna som PH 1 , PH 3 och PH 6 baserat på antalet länkade histidiner. Sun et al. syntetiserade peptiderna med hjälp av peptidsyntes i fast fas och renade den med högpresterande vätskekromatografi. De observerade bildandet av Zn 2+ histidinkoordineringskomplex med hjälp av ultraviolett (UV) och Raman -spektroskopi. Den specifikt utformade peptidsekvensen möjliggjorde synergistiskt och kooperativt Zn 2+ bindande affinitet, jämfört med peptider med slumpmässiga histidinrester på sina sekvenser. Forskarna studerade den molekylära mekanismen för kooperativ zinkjonbindning till PH 6 använder cirkulär dikroism, resultaten tyder på konforma förändringar av den första koordinationsplatsen för PH 6 att vara kritisk för kooperativ bindning och visade hur strukturella förändringar gynnade ytterligare Zn 2+ bindande.
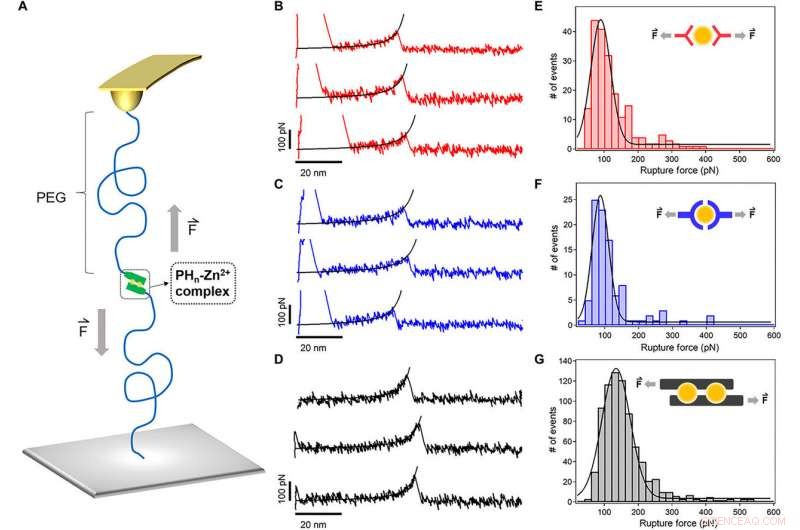
Enkelmolekylkraftspektroskopi av metalljonkoordinationskomplexen. (A) Schematiskt diagram av AFM-baserade enkelmolekyl kraftspektroskopi experiment. Peptidliganderna länkades till den fribärande spetsen och substratet via en PEG-linker (MW, 5 kDa). (B till D) Typiska kraftförlängningskurvor för brott av PH1-Zn2+ (röd), PH3-Zn2+(blå), och PH6-Zn2+ (svarta) komplex vid en draghastighet av 1000 nm s−1. Maskliknande kedjemontering av kraftförlängningskurvorna (svarta linjer) bekräftade att toppen vid en förlängning på ~ 50 nm motsvarar brottet av en enda metalljon-kelatbindning. (E till G) Brottkraftshistogrammen för PH1-Zn2+ (röd), PH3-Zn2+(blå), och PH6-Zn2+ (svart), respektive. Gausskopplingen visar de genomsnittliga brottkrafterna på 90 ± 29, 87 ± 24, och 135 ± 41 pN, respektive. De föreslagna Zn2+-jonbindningssätten för de tre peptiderna visas i insättningarna. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
Sun et al. använde avancerade tekniker som atomkraftsmikroskopi (AFM)-baserad enkelmolekylkraftspektroskopi (SMF) för att mäta den mekaniska stabiliteten hos HR-peptiden-Zn 2+ komplex, dvs tvärbindare av hydrogelen på molekylär nivå. De genomsnittliga brottkrafterna var mycket högre för PH 6 jämfört med andra typer av hydrogeler, bekräftar hydrogelens seghet. Resultaten visade att den mekaniska stabiliteten hos metall-ligandkomplexen kunde förbättras avsevärt baserat på bindningsställena.
The team explored if changes to the intrinsic properties of crosslinkers could alter macroscopic mechanical properties of the hydrogel by preparing a series of hybrid network (HN) hydrogels. They used HR-peptide-Zn 2+ as sacrificial crosslinkers and covalent bonds as permanent crosslinkers in the constructs and named the resulting hydrogels as HN-PH 1 , HN-PH 3 , and HN-PH 6 , based on the peptide sequence used. The network structures were similar in all three hydrogels but the HN-PH 6 gel was more compressible compared to the others, while functioning effectively under stressful mechanical environments. Intressant, the scientists could even twist the HN-PH 6 hydrogel into a spiral shape and compress the material with a sharp blade without causing it permanent damage.

Compressing the HN-PH6 hydrogel using a sharp blade does not damage the material. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
The team conducted tensile mechanical tests on the gels and correlated the results on the bulk level with those at the molecular level, to show remarkably higher break strain, Young's modulus and toughness for the HN-PH 6 gels. Sun et al. then examined the recovery property of the material based on loading-unloading cycles and found HN-PH 6 gels to almost totally recover its macroscopic mechanical properties in minutes. However, if they cut up the HN-PH 6 gels into pieces, the hydrogel could not self-heal since covalent crosslinkers do not reform after fracture. To understand the experimental outcomes, the research team also conducted theoretical analyses and proposed cooperative zinc binding on PH 6 to be an important factor, among other factors to form strong and tough hydrogels with fast recovery rates.
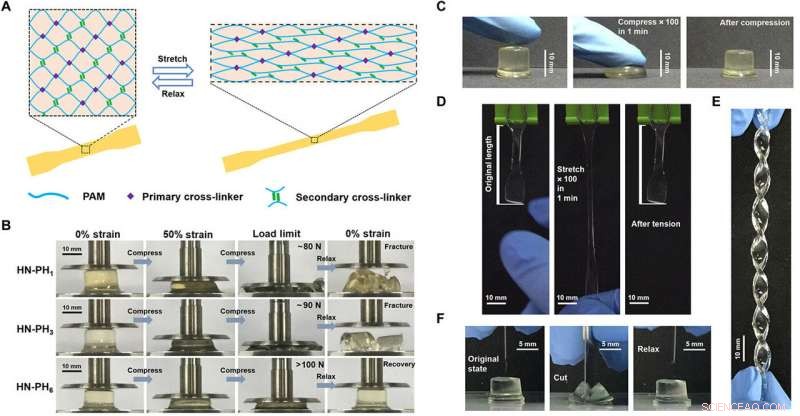
Structure and properties of HN-PHn HN hydrogels cross-linked by the peptide-Zn2+ coordination complexes. (A) Schematic illustration of the network structure of HN-PHn hydrogels. The network comprises covalent bonds as the primary cross-linkers and ligand-metal interactions as the secondary cross-linkers. (B) Optical images of the HN-PH1 (top), HN-PH3 (middle), and HN-PH6 (bottom) hydrogels under a compression-relaxation cycle. The HN-PH1 and HN-PH3 gels were fractured, whereas the HN-PH6 gel was almost fully recovered. (C) Optical images of the HN-PH6 gel under an extreme compressive condition (compressed to>70% strain for 100 times at 1.6 Hz). (D) Optical images of the HN-PH6 gel under an extreme tensile condition (stretched to>150% strain for 100 times at 1.6 Hz). (E) Optical image of the HN-PH6 gel twisted into a spiral shape. (F) Optical images of the HN-PH6 gel compressed with a sharp blade and relaxed. No detectable cut was observed on the gel. PAM, polyacrylamide. Photo credits:Wenxu Sun, Nanjing University. Kredit:Science Advances, doi:10.1126/sciadv.aaz9531
På det här sättet, Wenxu Sun and colleagues developed a novel hydrogel material, bioinspired by histidine residues found in natural load-bearing materials. Combining such outstanding mechanical properties in the lab has remained a challenge due to the inability to effectively harness the unique metal ion binding properties that are encoded in natural proteins. I det här arbetet, Sun et al. used bioinspired Zn 2+ -binding peptide as crosslinkers to form the desired hydrogels at the molecular level, highlighting the importance of cooperative metal coordination during materials synthesis. They intend to examine additional mechanical features, such as adhesion to other tissues, before conducting practical applications in tissue engineering.
© 2020 Science X Network